
【题目】下列各项叙述中正确的是 ( )
A. 在同一个电子层上运动的电子,其自旋方向肯定不同
B. 杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对
C. 物质的键能越大,该物质本身具有的能量越低
D. 在周期表中原子的族序数等于它的最外层电子数
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
【题目】持续的低温大雪使我国北方地区的“暖宝宝”成为紧俏商品。暖宝宝采用铁的“氧化放热”原理,使其发生原电池反应。已知制作暖宝宝的原料有铁粉、水、活性炭、蛭石、食盐,铁粉在原电池中充当
A.负极 B.正极 C.阴极 D.阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应H2(g)+ ![]() O2(g)=H2O(g)的能量变化如图所示,a、b、c表示能量变化,为正值,单位为kJ,下列说法正确的是 ( )
O2(g)=H2O(g)的能量变化如图所示,a、b、c表示能量变化,为正值,单位为kJ,下列说法正确的是 ( )

A. H2(g)+ ![]() O2(g)=H2O(g) △H=c kJ·mol-1
O2(g)=H2O(g) △H=c kJ·mol-1
B. 2H2O(g)=2H2 (g)+O2 (g) △H=—2(a-b) kJ·mol-1
C. 1 mol氢气与0.5 mol氧气总能量为akJ
D. 2 mol氢气与1 mol氧气完全反应生成2 mol液态水放出的热量小于2(b-a)kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子反应方程式正确的是:( )
A. 过量的二氧化碳通入NaOH溶液中:CO2+OH-==HCO3-
B. 氯气通入水中:Cl2+H2O==Cl-+ClO- +2H+
C. 硫酸亚铁溶液加入过氧化氢溶液Fe2++2H2O2+4H+==Fe3++4H2O
D. 向AlCl3溶液中过量的氨水:Al3+十4NH3·H2O==AlO2-十4NH4+十2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体的叙述中,不正确的是
A. 用半透膜除去淀粉胶体中的Na+、Cl-
B. 胶体中分散质粒子的直径在1nm~100nm之间
C. 利用丁达尔效应可以区分溶液和胶体
D. 用滤纸能分离胶体和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SF6是一种优良的绝缘气体,分子结构中只存在S﹣F键.已知:1mol S(s)转化为气态硫原子吸收能量280kJ,断裂1mol F﹣F、S﹣F键需吸收的能量分别为160kJ、330kJ.则S(s)+3F2(g)═SF6(g)的反应热△H为( )
A.﹣1780kJ/mol
B.﹣1220 kJ/mol
C.﹣450 kJ/mol
D.+430 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)分子式为C5Hl2O并能与金属钠反应放出H2的有机化合物有________种;
(2)下列说法错误的是_____________;
A.有机物均易燃烧
B.苯酚酸性比碳酸弱,故苯酚不能与碳酸钠溶液反应
C.制取乙酸乙酯时,试剂的混合顺序是先加浓硫酸,再加乙醇,然后加乙酸
D.石油分馏得到的汽油是纯净物
(3)分子式为C5H9C1O2的同分异构体甚多,其中能与NaHCO3发生反应产生CO2的同分异构体共有________种;
(4)分子式为C3H6O2的链状有机物,核磁共振氢谱上峰的数目及强度比分别为:①3∶3;②3∶2∶1;③3∶1∶1∶1;④2∶2∶1∶1,则它们可能的结构简式依次为:
①_______________;②______________;
③_______________;④__________________。
(5)苯氧乙酸(![]() )有多种酯类的同分异构体,其中能与FeCl3溶液发生显色反应,且苯环上有2种一硝基取代物的同分异构体是_______________(写出任意2种的结构简式)
)有多种酯类的同分异构体,其中能与FeCl3溶液发生显色反应,且苯环上有2种一硝基取代物的同分异构体是_______________(写出任意2种的结构简式)
(6)按系统命名法,右图化合物的名称是___________
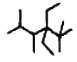
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:

已知:
①海水中溴元素(以Br﹣表示)的浓度0.068g/L;
②Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性.
(1)请写出两种海水淡化的方法:_______________________.
(2)海水中溴离子的物质的量浓度为____________________.
(3)步骤Ⅰ中已获得低溶度的含Br2溶液,步骤Ⅱ中又将Br2还原为Br﹣,步骤Ⅲ又得到Br2,其目的为__________________.
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_________.
(5)工业溴提纯可用蒸馏法,蒸馏时加热方法最好采用_____,蒸馏装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________.
(6)Br2是有机合成工业中的重要原料,甲苯的一溴代物有多种,其中苯环上的一氯代物只有两种的结构简式为_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com