
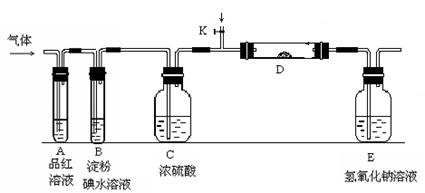
| A.氨水 | B.稀盐酸 | C.稀硝酸 | D.氯化钙 |
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源:不详 题型:填空题
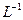 的硫酸100mL。若实验仪器有:
的硫酸100mL。若实验仪器有: 字母);
字母); 中,下列操作不正确的是 (填字母);
中,下列操作不正确的是 (填字母); 用容量瓶前检查其是否漏水。
用容量瓶前检查其是否漏水。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
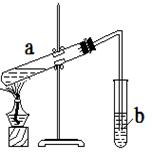
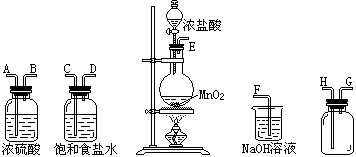
 (2)在下面方框中,A表示有分液漏斗和圆底烧瓶组成的气体发生器,请在虚线框内的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必
(2)在下面方框中,A表示有分液漏斗和圆底烧瓶组成的气体发生器,请在虚线框内的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必 画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如
画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如 下:
下: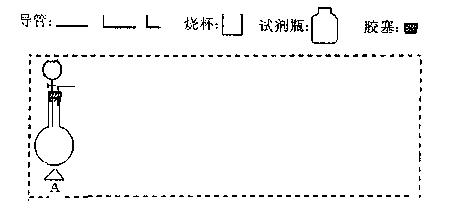
| 仪器符号 | 仪器中所加物质 | 作用 |
| A | MnO2、浓盐酸 | MnO2与浓盐酸生成Cl2 |
| | | |
| | | |
| | | |
| | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
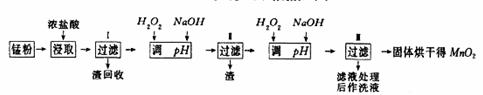
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)2 | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 分子式 | 别名 | 熔点 | 沸点 | 溶解性 | 性状 |
| ClNO | 氯化亚硝酰 | -64.5℃ | -5.5℃ | 溶于浓硫酸 | 红褐色液体或有毒气体,具有刺激恶臭,遇水反应生成氮的氧化物与氯化氢 |
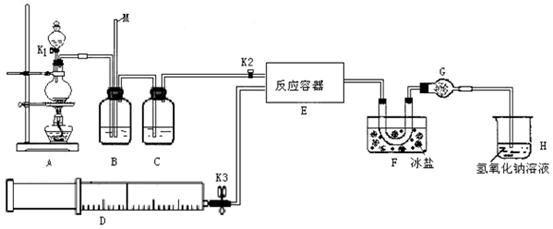
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.加水定容时超过刻度线,又吸出少量水至刻度线; | B.忘记将洗涤液转入容量瓶; |
| C.容量瓶洗涤后内壁有水珠而未作干燥处理; | |
| D.称量碳酸钠粉末时左盘放砝码,右盘放药品; |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com