
【题目】以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如图所示:

下列说法不正确的是
A. 酸溶过程使用的酸也可以是硝酸,且过量
B. 为了防止污染,焙烧过程中产生的SO2要回收利用
C. 通氯气的目的是氧化Fe2+
D. 由FeCl3·6H2O制取无水FeCl3需要在氯化氢的气流中加热
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】某元素的同位素![]() X,它的氯化物XCl2 0.95g溶于水制成溶液后,加入1mol/L的AgNO3溶液20mL,恰好完全反应.若这种同位素原子的原子核内有12个中子,回答:
X,它的氯化物XCl2 0.95g溶于水制成溶液后,加入1mol/L的AgNO3溶液20mL,恰好完全反应.若这种同位素原子的原子核内有12个中子,回答:
(1)Z的值为__________、A的值为__________;
(2)X元素在周期表中的位置为______________
(3)把X的单质放入盐酸中,写出反应的离子方程式:___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在浓度都为1 mol·L-1的(NH4)2SO4、NH4H CO3、NH4HSO4、NH4Cl的四种溶液中,测得c(NH4+)分别为a、b、c、d(单位为mol·L-1)。下列判断正确的是
A. a=2b=2c=2d B. a>b>c> d C. a>c>d>b D. a>c>b>d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况图所示,回答下列问题。
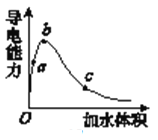
(1)“O”点时液体不能导电,说明醋酸中________离子键(填“含有”或“不含”)。
(2)a、b、c三点醋酸电离程度由大到小的顺序为________;a、b、c三点对应的溶液中c(H+)最大的是________。
(3)要使c点溶液中c(CH3COO-)增大而c(H+)减小,可采取的两种措施是_______________
(4)若实验测得c点处溶液中c(CH3COOH)=0.1 mol·L-1,c(CH3COO-)=0.001 mol·L-1,则该条件下CH3COOH的电离常数Ka=________。电离度是______________。
(5)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是(____)
A.c(H+) B.H+个数
C.CH3COOH分子数 D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,破坏1molH2中的化学键消耗的能量为Q1kJ,破坏1molC12中的化学键消耗的能量为Q2kJ,形成1molHCl中的化学键释放的能量为Q3kJ。下列关系式中,正确的是
A. Q1+Q2>Q3 B. Q1+Q2>2Q3 C. Q1+Q2<2Q3 D. Q1+Q2<Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A(C8H8O2)的核磁共振氢谱有4组峰且面积之比为1:2:2:3,A中含一个苯环且苯环上只有一个取代基,下列有关说法正确的是
A. 符合题中A分子结构特征的有机物只有1种
B. 化合物A属于羧酸类化合物
C. 与A属于同类化合物的同分异构体只有2种
D. A在一定条件下可与4molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知aAn+, bB(n+1)+, cCn-, dD(n+1)-是具有相同的电子层结构的短周期元素形成的简单离子,下列叙述正确的是 ( )
A. 原子半径:C>D>A>BB. 原子序数:b>a>c>d
C. 离子半径:Cn->D(n+1)->An+>B(n+1)+D. 单质还原性:A>B>C>D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com