
【题目】某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置. 
请回答下列问题:
(1)装置F中发生反应的离子方程式为 .
(2)装置A的烧瓶中可装试剂
(3)B装置的名称是 , E装置的作用 .
(4)通入C装置的两根导管左边较长、右边较短,目的是 .
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.写出反应的化学方程式:该反应中氧化剂和还原剂的物质的量之比为 .
【答案】
(1)MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)生石灰(或固体氢氧化钠、碱石灰)
(3)球形干燥管;除去氯气中的氯化氢
(4)使密度大的氯气与密度小的氨气较快地均匀混合
(5)3Cl2+8NH3=N2+6NH4Cl;3:2
【解析】解:(1)装置F中二氧化锰与浓盐酸加热生成氯化锰、氯气和水,反应的离子方程式为:MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O,所以答案是:MnO2+4H++2Cl﹣
Mn2++Cl2↑+2H2O,所以答案是:MnO2+4H++2Cl﹣ ![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2.)装置A中的烧瓶内是制备氨气的装置,氨水滴入后,A中固体溶解放热使氨气放出,该固体可以为碱石灰、生石灰、氢氧化钠固体等,所以答案是:生石灰(或固体氢氧化钠、碱石灰);
(3.)B装置的名称是球形干燥管;制取的氯气中含有杂质氯化氢,氯气不易溶于饱和食盐水,氯化氢极易溶于饱和食盐水,则装置E的作用是用饱和食盐水除去氯气中的氯化氢,所以答案是:球形干燥管;除去氯气中的氯化氢;
(4.)氨气密度比氯气的小,通入C装置的两根导管左边较长(导氨气)、右边较短(导氯气),可以保证二者充分混合,所以答案是:使密度大的氯气与密度小的氨气较快地均匀混合;
(5.)装置C内出现浓厚的白烟并在容器内壁凝结,该产物为NH4Cl,另一生成物是空气的主要成分之一,该产物为N2 , 氯气中0价Cl元素被还原为﹣1价,化合价至少降低2价,氨气中﹣3价N元素被氧化为0价,化合价升高3价,化合价变化的最小公倍数为6,则氯气的计量数为3,氨气的计量数为2,结合质量守恒定律配平该反应的化学方程式为:3Cl2+8NH3=N2+6NH4Cl;该反应中氯气化合价从0将为﹣1被还原,氯气为氧化剂,氨气中﹣3价N元素被氧化物0价氮气,则氨气为还原剂,3mol氯气反应能够生成1mol氮气,则被氧化的氨气为2mol,所以该反应中氧化剂与还原剂的物质的量之比为3:2,所以答案是:3Cl2+8NH3=N2+6NH4Cl;3:2.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】现将浓度相等、体积分别为V1、V2的H2SO4、NaOH溶液混合,测量混合液温度,结果如图(已知:V1+V2=60mL)。下列叙述错误的是 ( )

A. 实验的环境温度低于22℃ B. 混合溶液的导电能力:M>N
C. P点混合溶液呈中性 D. 若将H2SO4改为CH3COOH,P点温度低于28℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。回答下列问题:
(1)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表:
2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表:
t/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5 |
在200℃时,当测得NH3和N2、H2的物质的量分别为1mol和0.5mol、1mol时,则该反应的v(N2)正____v(N2)逆(填写“>”、“=”或“<”)。
(2)结合表中给出的电离常数回答下列问题:
酸或碱 | CH3COOH | HNO2 | HCN | HClO |
电离平衡常数(Ka或Kb) | 1.8×10-5 | 4.6×10-4 | 5×10-10 | 3×10-8 |
①上述四种酸中,酸性最弱、最强的酸分别是_______、____(用化学式表示)。
②下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是____(填序号)。
A.升高温度 B.加水稀释 C.加少量的CH3COONa固体 D.加少量冰醋酸 E.加氢氧化钠固体
③依上表数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下图所示化合物的说法不正确的是( )。

A. 既可以与Br2的CCl4溶液发生加成反应,又可以与Br2发生取代反应
B. 1mol该化合物最多可以与3molNaOH反应
C. 既可以催化加氢,又可以使酸性KMnO4溶液褪色
D. 既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容量瓶是用来配制一定物质的量浓度的溶液的定量仪器,其上标有:①温度 ②浓度③容积 ④压强 ⑤刻度线这五项中的
A. ①③⑤ B. ③④⑤ C. ①②④ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.52g 铜镁合金完全溶解于50mL 密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )。
A. 该合金中铜与镁的物质的量之比是2:1
B. 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L
C. NO2和N2O4的混合气体中,NO2的体积分数是80%
D. 得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体。根据图示回答问题:
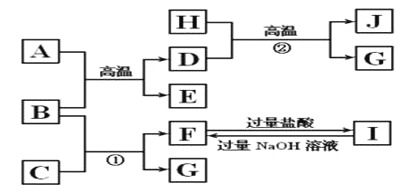
(1)写出下列物质的化学式:A________, I________,
(2)反应反应②的化学方程式是__________________;
(3)如右图所示,将I持续滴加入NaOH中开始没有沉淀生成,后来出现白色沉淀,V1:V2=_________;

(4)3molJ与足量的稀硝酸反应生成____________molNO。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质或该物质性质的应用均正确的是( )
A. 醋酸溶液与醋酸钠溶液中的醋酸根均可以水解,同浓度时前者的水解程度比后者低一些
B. 明矾净水与自来水的杀菌清毒原理是一样的
C. MgO和Al2O3在工业上用于制作耐高温材料,可用电解此两种物质冶炼镁、铝金属
D. 氯化亚铁溶液加热蒸干并灼烧得到三氧化二铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com