
【题目】化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水充足搅拌、过滤。
(1)往滤渣中加入过量 NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是______。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察的现象是__________。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO沉淀质量,以确定碳酸钙的质量分数。
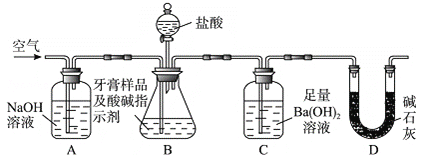
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:________________________________。
(4)C中反应生成沉淀的离子方程式是______________________________。
(5)下列各项措施中,不能提高测定准确度的是____________(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体 b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取10.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g。则样品中碳酸钙的质量分数为__________。
【答案】Al(OH)3+OH-=AlO2-+2H2O或Al(OH)3+OH-=[Al(OH)4]- 通入CO2气体有白色沉淀生成;加入盐酸有气体产生、沉淀溶解 把生成的CO2全部排入C中,使之完全被Ba(OH)2溶液吸收 Ba2++2OH-+CO2=BaCO3↓+H2O c、d 20%
【解析】
Ⅰ.(1)氢氧化铝与NaOH溶液反应生成偏铝酸钠与水;
(2)往(1)所得滤液中先通入过量二氧化碳,发生反应AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,再加入过量稀盐酸,Al(OH)3+3HCl=AlCl3+3H2O、HCO3-+H+=CO2↑+H2O;
Ⅱ.(3)实验通过C装置生成的碳酸钡的质量测定二氧化碳的质量,进而计算牙膏中碳酸钙的质量分数,装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏小;
(4)C中为Ba(OH)2和CO2反应生成碳酸钡沉淀;
(5)a.在加入盐酸之前,应排净装置内的CO2气体,防止空气中二氧化碳进入C被氢氧化钡吸收;
b.滴加盐酸过快,则生成二氧化碳过快,C中二氧化碳不能全部被吸收;
c.BC中均为水溶液,不需要干燥;
d.挥发的HCl进入盛有饱和碳酸氢钠溶液的洗气装置,会生成二氧化碳;
(6)根据碳原子守恒计算。
Ⅰ.(1)氢氧化铝与NaOH溶液反应生成偏铝酸钠与水,反应离子方程式为Al(OH)3+OH-=AlO2-+2H2O;
(2))往(1)所得滤液中先通入过量二氧化碳,发生反应AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,再加入过量稀盐酸,Al(OH)3+3HCl=AlCl3+3H2O,HCO3-+H+=CO2↑+H2O,反应现象是通入CO2气体有白色沉淀生成;加入盐酸有气体产生,沉淀溶解;
Ⅱ.(3)装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏小,持续缓缓通入空气的作用为:把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收;
(4)C中的反应的离子方程式为Ba2++2OH-+CO2=BaCO3↓+H2O;
(5)在加入盐酸之前,应排净装置内的CO2气体可以提高测定的准确度,a不选;滴加盐酸过快,则生成二氧化碳过快,C中二氧化碳不能全部被吸收,滴加盐酸不宜过快,确保生成的CO2被完全吸收,提高实验的精确度,b不选;B中装有溶液,因此气体通入前没有必要干燥,c选;在B—C之间连接盛有饱和NaHCO3溶液的洗气瓶会造成Ba(OH)2溶液还可能吸收由挥发出的氯化氢与NaHCO3反应生成的CO2气体,干扰实验,d选;答案选c、d。
(6)根据碳元素守恒得:BaCO3—CO2—CaCO3,m(CaCO3)=![]() ,CaCO3的质量分数为
,CaCO3的质量分数为![]() 。
。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
A. 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3-3e-+5OH-=![]() +4H2O
+4H2O
C. 放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:
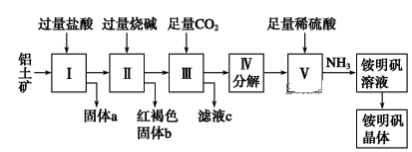
请回答下列问题:
(1)固体a的化学式为________。
(2)写出Ⅱ中加过量的烧碱涉及到的反应离子方程式______________、_____________;Ⅲ中通入足量CO2气体发生反应的离子方程式为_______________。
(3)由Ⅲ中得到滤液c的实验操作为__________,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)________、冷却结晶、过滤洗涤。
(4)将NH4Al(SO4)2溶液和Ba(OH)2溶液,按物质的量比1:2混合,写出离子方程式为_______________。
(5)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如右图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大。
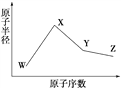
(1)X位于元素周期表中第________周期第________族;W的基态原子核外有_____个未成对电子。
(2)Z的气态氢化物和溴化氢相比,较稳定的是______(写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中有1mol NaHCO3和0.8mol Na2O2,加热充分反应后,容器内残留的固体
A. 0.5molNa2CO3和0.8mol Na2O2 B. 0.5molNa2CO3和1.6molNaOH
C. 0.8molNa2CO3和1molNaOH D. 1molNa2CO3和0.6molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组将SO2通入Na2S和Na2SO3的混合溶液中制备硫代硫酸钠(Na2S2O3)。其装置如下图所示(省略夹持装置),下列说法错误的是
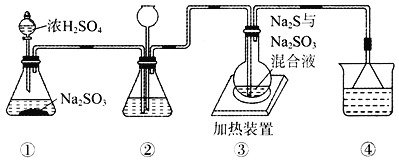
A. 装置②的作用之一是观察SO2的生成速率,其中的液体可以是饱和NaHSO3溶液
B. 为提高产品纯度,使烧瓶中Na2S和Na2SO3恰好完全反应,则![]()
C. 装置④的作用是吸收尾气,同时防止倒吸
D. 装置①也可用于高锰酸钾与浓盐酸反应制备氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠和碳酸氢钠是生活中常见的物质,请回答下列问题。
(1)碳酸氢钠的俗称是_________,其水溶液显_____性。(填“酸”、“碱”或“中”)。
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式____________。等物质的量的碳酸钠和碳酸氢钠分别与足量盐酸反应时生成CO2的量,前者________后者(填“>”、“<”或“=”)。
(3)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为________________________________。
(4)硫酸亚铁是缺铁性贫血的治疗药物,可用于制备铁盐,实验室检验Fe3+的方法是:向溶液中滴入几滴_________________溶液,观察溶液是否变为血红色。向FeSO4溶液中加入NaOH溶液通常得不到白色的Fe(OH)2沉淀,其原因是_________________________(用化学方程式回答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用氯水来制取含有次氯酸的溶液,既要提高溶液中HClO物质的量浓度,又要降低溶液中HCl浓度,下列措施可以采用的是( )
A. 加热挥发HCl B. 加CaSO3
C. 加NaOH中和HCl D. 加CaCO3中和HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 在常温、常压下,11.2 L N2含有的分子数为0.5NA
B. 标准状况下,22.4 L H2和O2的混合气体所含分子数为NA
C. 18 g H2O的物质的量是1mol
D. 标况下,1 mol SO2的体积是22.4 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com