
����Ŀ���Ȼ��������ж��е���ɫ������������Ⱦ�ϡ�Ⱦ���м��塢ӡȾ����ֽ��ҵ����ˮ������ij����С��������·����Ʊ��Ȼ�������̽���Ȼ�������Fe2+���Ļ�ԭ�ԣ�
ijͬѧѡ������װ�����Ȼ����Ʊ������Ȼ�������װ�ò������ظ�ʹ�ã�����������֪���Ȼ�����ˮ����ˮ�⣬�ڼ���������������ԭ�Ȼ�������FeCl2��HCl��
��1��ʵ�鿪ʼǰӦ�ȼ��װ�õ������ԣ�������װ��A�����Լ���ķ�����
��2�������������ң�װ�ýӿ�����˳����a
��3��װ��C�и��������ʢ�Լ��������ǣ� �� �����ǣ�
��4��װ��C�оƾ��Ƶ������ǣ�
��5��Ϊ�˲ⶨ�Ȼ�����������������ijͬѧ����������ʵ�飺
��ȡʵ���Ʊ����Ȼ�������Ʒ5.435g�������Һ����1.00molL��1����KMnO4����Һ�ζ����յ㣮����֪��ԭ��Fe2+��Cl�����ζ���������ʾ��
�ζ����� | ����Һ����� | |
�ζ�ǰ�̶�/mL | �ζ���̶�/mL | |
1 | 1.04 | 25.03 |
2 | 1.98 | 25.99 |
3 | 3.20 | 25.24 |
��д���ζ���������������2�����ӷ���ʽ��
����Ʒ���Ȼ���������������Ϊ
���𰸡�
��1���رջ�������©����עˮ���γ�һ��ˮ����Һ��߶Ȳ��䣬˵��װ������������
��2��b c e f d
��3����ʯ�һ���ʯ�ң���ȥHCl������ֹ������ˮ�Ľ���
��4��ȼ��H2 �� ��ֹ��Ⱦ����
��5��MnO4��+5Fe2++8H+�TMn2++5Fe3++4H2O��2MnO4��+16H++10Cl��=2Mn2++5Cl2��+8H2O��70.1%
���������⣺��1��װ�������Եļ��飬���ó���©������ʹ��עˮ��������ˮ�γ�һ��ˮ���ұ��ֲ��䣬�رջ�������©����עˮ���γ�һ��ˮ����Һ��߶Ȳ��䣬˵��װ�����������ã��ʴ�Ϊ���رջ�������©����עˮ���γ�һ��ˮ����Һ��߶Ȳ��䣬˵��װ�����������ã���2��װ�õ�����˳��������װ��A��������ͨ��Ũ��������ͨ��װ��D�еIJ������м��ȷ�Ӧ���ڼ���������������ԭ�Ȼ�������FeCl2��HCl��ʣ������ͨ��װ��C��ȼ�����������������ң�װ�ýӿ�����˳����a b c e f d��
�ʴ�Ϊ��a b c e f d����3��װ��C�м�ʯ�һ���ʯ���������ɵ��Ȼ��⣬��C�и����Ӧʢ�ż�ʯ�����ó�ȥHCl������ֹ������ˮ�Ľ��룬
�ʴ�Ϊ����ʯ�һ���ʯ�ң���ȥHCl������ֹ������ˮ�Ľ��룻��4��װ��A���Ʊ���������������ˮ��ѡ������Լ����������֪������ԭ�Ȼ�������FeCl2��HCl���Ʊ�FeCl2 �� ���Ȼ�����ˮ����ˮ�⣬Ӧע��ǰ��Ҫ��ˮ���룬������β��������β��������β������δ��Ӧ��ȫ��������HCl��װ��C�оƾ��Ƶ�����Ϊȼ��H2 �� ��ֹ��Ⱦ������
�ʴ�Ϊ��ȼ��H2 �� ��ֹ��Ⱦ��������5��ͼ�����ݷ�����֪�����εζ���ֵ���̫���������ʵ�����ȥ�����ݵ�һ�κ͵ڶ��εζ����������������Һ��ƽ�������V= ![]() ml=24ml�����������ԭ��Ӧ������ϵ���㣬MnO4��+5Fe2++8H+�TMn2++5Fe3++4H2O��2MnO4��+16H++10Cl��=2Mn2++5Cl2��+8H2O��
ml=24ml�����������ԭ��Ӧ������ϵ���㣬MnO4��+5Fe2++8H+�TMn2++5Fe3++4H2O��2MnO4��+16H++10Cl��=2Mn2++5Cl2��+8H2O��
��FeCl3��FeCl2���ʵ����ֱ�Ϊx��y��Fe2+Ϊymol��Cl��Ϊ��3x+2y��mol![]() +
+ ![]() =1.00molL��1��0.024L
=1.00molL��1��0.024L
162.5x+127y=5.435
���x=0.01mol��y=0.03mol��
����õ��Ȼ���������������= ![]() ��100%=70.1%��
��100%=70.1%��
�ʴ�Ϊ��70.1%��
��1��װ�������Եļ��飬���ó���©������ʹ��עˮ��������ˮ�γ�һ��ˮ���ұ��ֲ��䣻��2��װ�õ�����˳��������װ��A��������ͨ��Ũ��������ͨ��װ��D�еIJ������м��ȷ�Ӧ���ڼ���������������ԭ�Ȼ�������FeCl2��HCl��ʣ������ͨ��װ��C��ȼ��������3��װ��C�м�ʯ�һ���ʯ���������ɵ��Ȼ��⣬��C�и����Ӧʢ�ż�ʯ�����ó�ȥHCl������ֹ������ˮ�Ľ��룻��4�����Ʊ���������������ˮ��ѡ������Լ����������֪������ԭ�Ȼ�������FeCl2��HCl���Ʊ�FeCl2 �� ���Ȼ�����ˮ����ˮ�⣬Ӧע��ǰ��Ҫ��ˮ���룬������β��������β��������β������δ��Ӧ��ȫ��������HCl��װ��C�оƾ��Ƶ�����Ϊȼ��H2 �� ��ֹ��Ⱦ��������5��ͼ�����ݷ�����֪�����εζ���ֵ���̫���������ʵ�����ȥ�����ݵ�һ�κ͵ڶ��εζ����������������Һ��ƽ�������V= ![]() ml=24ml�����������ԭ��Ӧ������ϵ���㣬MnO4��+5Fe2++8H+�TMn2++5Fe3++4H2O��2MnO4��+16H++10Cl��=2Mn2++5Cl2��+8H2O��
ml=24ml�����������ԭ��Ӧ������ϵ���㣬MnO4��+5Fe2++8H+�TMn2++5Fe3++4H2O��2MnO4��+16H++10Cl��=2Mn2++5Cl2��+8H2O��
��FeCl3��FeCl2���ʵ����ֱ�Ϊx��y��Fe2+Ϊymol��Cl��Ϊ��3x+2y��mol![]() +
+ ![]() =1.00molL��1��0.024L
=1.00molL��1��0.024L
162.5x+127y=5.435
���x=0.1 y=0.3��
����õ��Ȼ�����������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʲ���������������Һ��Ӧ����
A.Fe2O3B.Al(OH)3 C.NaHCO3D.H2SiO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ϳ�·������й����⣺ 
��1��д��A��B��C�ṹ��ʽ��A�� �� B�� �� C�� ��
��2��������Ӧ���ͣ��� �� �� �� �� �� �� �� �� �� �ڵķ�Ӧ����
��3��д����Ӧ�ܵĻ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ�������
A. ˮ������Ư�ۡ�������Ϊ�����
B. ����������һ���ǽ�����������������ﲻһ���Ǽ���������
C. �ܵ����H+������������
D. ����������һ������������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ�ֺ�������������ϵͳԭ��ʾ��ͼ������˵����ȷ���ǣ� �� 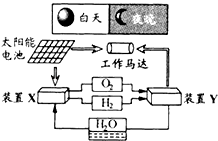
A.��ϵͳ��ֻ����3����ʽ������ת��
B.װ��Y�и����ĵ缫��ӦʽΪ��O2+2H2O+4e��=4OH��
C.װ��X��ʵ��ȼ�ϵ�ص�ȼ�Ϻ�����������
D.װ��X��Y�γɵ���ϵͳ��ʵ�����ʵ����ŷţ�����ʵ�ֻ�ѧ������ܼ����ȫת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʻ�Ϊͬ���칹���һ����
A. ˮ��������B. 12C��14CC. ��������춡��D. O2��O3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤��������ֵ������˵����ȷ���ǣ�������
A.0.5 mol O3��11.2 L O2�����ķ�����һ�����
B.��״���£�11.2 L��N2��CO��ɵĻ�����庬�е�ԭ����ĿΪNA
C.��״���£�22.4 L��CCl4�к��е�CCl4������ΪNA
D.���³�ѹ�£�22.4 L��NO2��CO2������庬��2NA����ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����n��HNO3��ϡ��Һǡ����m��Fe��ȫ��Ӧ����HNO3ֻ����ԭΪNO����n��m������ ��5��1����9��2����3��1����2��1����4��1��������
A.�ڢۢ�
B.�٢ۢ�
C.�ڢۢ�
D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ����������������������ʱֻ�ܱ�Ϊ+2 �������ǣ�������
A.FeCl3B.HNO3C.Cl2D.O2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com