
【题目】下列原子中第一电离能最大的是 ( )
A. Na B. K
C. Mg D. Al
科目:高中化学 来源: 题型:
【题目】冬季是雾霾天气高发的季节,其中汽车尾气和燃煤尾气是造成雾霾的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)
2CO2(g)+N2(g)
①在一定条件下,在一个容积固定为2L的密闭容器中充入0.8molNO和1.20molCO,开始反应至3min时测得CO的转化率为20%,则用N2表示的平均反应速率为V(N2)=__________。
②对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(CB)也可以表示平衡常数(记作Kp),则该反应平衡常数的表达式Kp=______________。
③该反应在低温下能自发进行,该反应的△H_______0,(选填“>”、“=”或“<”)
④在某一绝热,恒容的密闭容器中充入一定量的NO、CO发生上述反应,测得正反应的速率随时间变化的曲线如图所示(已知t2—t1=t3—t2)。则下列说法不正确的是__________。(填编号)
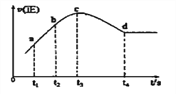
A.反应在c点未达到平衡状态 B.反应速率a点小于b点
C.反应物浓度a点大于b点 D.NO的转化率t1—t2=t2—t3
(2)使用甲醇汽油可能减少汽车尾气对环境的污染,某化工厂用水煤气为原料合成甲醇,恒温条件下,在体积可变的密闭容器中发生反应:CO(g)+2H2(g)CH3OH(g),到达平衡时,测得CO、H2、CH3OH分别为1mol、1mol、1mol,容器的体积为3L,现往容器中继续通人3molCO,此时v(正)____v(逆)(选填‘‘>”、“<’’或“=”),判断的理由____________。
(3)二甲醚也是清洁能源,用合成气在催化剂存在下制备二甲醚的反应原理为:
2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
已知一定条件下,该反应中CO的平衡转化率随温度、投料比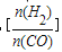 的变化曲线如图:
的变化曲线如图:
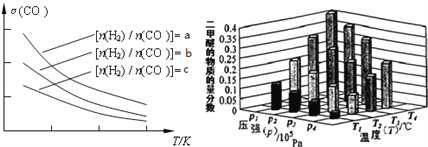
①a、b、c按从大到小的顺序排序为___________。
②某温度下,将2.0mol CO(g)和4.0mol H2(g)充入容积为2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如上图所示,关于温度和压强的关系判断正确的是___________;
A.P3>P2,T3>T2 B.P1>P3,T1>T3
C.P2>P4,T4>T2 D.P1>P4,T2>T3
③在恒容密闭容器里按体积比为1:2充入一氧化碳和氢气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是___________:
A.正反应速率先增大后减小
B.逆反应速率先增大后减小
C.化学平衡常数K值增大
D.反应物的体积百分含量增大
E.混合气体的密度减小
F.氢气的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下面列出了几组物质,请将正确的序号填写在空格上。
①金刚石与“足球烯”C60; ②HCHO和CH3CHO; ③CH3CH2OH和CH3OCH3;④CH4和CH3CH2CH3;⑤D与T ; ⑥CH2=CH—CH2—CH3和CH3—CH=CH—CH3;⑦氧气(O2)与臭氧(O3)
同位素_________________;同系物_____________ ;
同素异形体_____________;同分异构体______________。
(2)现有下列六种有机物a.乙烷 b.乙烯 c.苯 d.乙醇 e.乙酸 f.CH2===CH—COOH g.CH2OH(CHOH)4CHO h.乙酸乙酯
①能与Na和NaOH溶液都反应的是_____________。
②分子内所有原子一定在同一平面上的有___________。
③常温下可能与溴水发生加成反应的有_____________。
④在一定条件下能发生酯化反应的有_______________。
⑤能与新制Cu(OH)2悬浊液反应的有________________。
⑥能发生水解反应的有______________。
(3)现有 A:CH3CH2OH; B:CH2OH—CH2OH;
C:CH2OH—CH(OH)—CH2OH三种有机物:
①等物质的量的这三种有机物完全燃烧耗氧量之比为______________;
②写出A与金属钠反应的化学方程式:_____________________________。
③等物质的量的这三种有机物与足量金属钠反应,同温同压下产生氢气的体积比为:__________________________。
④写出B在铜作催化剂的条件下与氧气反应的方程式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】每到冬天就会出现大雾天气,能见度不到10米,致使汽车行驶受阻,下列关于雾的说法正确的是( )
A.无法确定雾中水滴的直径大小 B.不会产生丁达尔现象
C.雾中水滴的直径在1nm~100nm间 D.雾中水滴的直径小于1nm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作。下列说法中正确的是( )
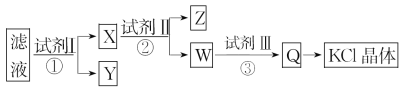
A.起始滤液的pH=7
B.试剂Ⅰ为Ba(NO3)2溶液
C.步骤②中加入试剂Ⅱ的目的是除去B![]()
D.图示的步骤中必须要经过2次过滤操作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向溶液中分别通入足量的相应气体后,下列各组离子还能大量存在的是( )
A.氯气:K+、Na+、SiO32﹣、NO3﹣
B.二氧化硫:Na+、NH4+、SO32﹣、C1﹣
C.硫化氢:H+、K+、MnO4﹣、SO42﹣
D.氨气:K+、Na+、AlO2﹣、CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有五价砷(As),西红柿中含有比较多的维生素C,两者同食时会生成有毒的三价砷。下列说法正确的是( )
A. 因为河虾中含有砷元素,所以不能食用
B. “两者同食”发生的反应中维生素C作氧化剂
C. 五价砷在维生素C作用下发生了还原反应
D. 已知砒霜的主要成分是氧化砷,可以推测所含的砷元素化合价为+5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示.
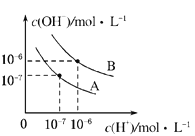
(1)95℃时水的电离平衡曲线应为______(填“A”或“B”),理由是______.
(2)曲线A所对应的温度下,pH=2的HCl溶液和pH=12的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1______α2(填“大于”、“小于”、“等于”或“无法确定”,下同),若将二者等体积混合,则混合溶液的pH______7.
(3)在曲线B所对应的温度下,将0.02molL﹣1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com