
ЎѕМвДїЎїДі»ЇС§РЛИ¤РЎЧй±ыОЄМЅѕїFe3+КЗ·сДЬСх»ЇSO2 Ј¬ ЙијЖБЛИзНјКµСйЧ°ЦГЈ® 
ЈЁ1Ј©ИзЙПНјБ¬ЅУєГЧ°ЦГЈ®КµСйЗ°У¦ЅшРРІЩЧч
ЈЁ2Ј©№ЫІмµЅЧ°ЦГCЦРІъЙъБЛ°ЧЙ«іБµнЈ¬Н¬С§ГЗМбіцБЛТФПВІВПлЈЁГїёцІВПлЦ»їјВЗТ»ЦЦОпЦКµДСх»ЇРФЈ©Ј®
ІВПл1ЈєЈ»
ІВПл2ЈєSO2±»Fe3+Сх»ЇБЛЈ»
ІВПл3ЈєSO2±»NO3©ЃСх»ЇБЛ
ЈЁ3Ј©јЧН¬С§ИПОЄІВПл1ХэИ·Ј¬ІўАыУГЙПКцЧ°ЦГAЅшРРБЛЕЕіэёЙИЕµДМЅѕїКµСйЈ®
ТТН¬С§ИПОЄІВПл2ХэИ·Ј¬ФтЧ°ЦГCЦР·ґУ¦µДАлЧУ·ЅіМКЅКЗ
ЈЁ4Ј©±ыН¬С§ИПОЄІВПл3ХэИ·Ј¬ЛыАыУГјЧН¬С§µДКµСйЧ°ЦГЈ¬ЙијЖКµСйСйЦ¤ІВПлЈ®ЗлФЪ±нёсЦРРґіцКµСйІЅЦиТФј°Ф¤ЖЪПЦПуєНЅбВЫЈ®ПЮСЎКµСйКФјБЈєNaNO3ИЬТєЎўKSCNИЬТєЎўFeCl3ИЬТєЎўBaCl2ИЬТєЎўFeЈЁNO3Ј©3ИЬТє
КµСйІЅЦи | Ф¤ЖЪПЦПуєНЅбВЫ |
Ўѕґр°ёЎї
ЈЁ1Ј©јмІйЧ°ЦГµДЖшГЬРФ
ЈЁ2Ј©їХЖшУлSO2ЅшИлH2OЦРЈ¬СхЖш°С¶юСх»ЇБтСх»ЇЙъіЙБЛH2SO4
ЈЁ3Ј©SO2+2Fe3++Ba2++2H2O=BaSO4Ўэ+2Fe2++4H+
ЈЁ4Ј©Ѕ«Ч°ЦГCЦРµДИЬТє»»ОЄNaNO3 єНBaCl2µД»мєПИЬТєЈ¬И»єуґтїЄ·ЦТєВ©¶·»оИыЅшРР·ґУ¦Ј»·ґУ¦Т»¶ОК±јдєуЈ¬ИфCЦРіцПЦ°ЧЙ«іБµнЈ¬ФтЦ¤ГчІВПл3ХэИ·
ЎѕЅвОцЎїЅвЈєЈЁ1.Ј©ЧйЧ°НкТЗЖчРијмСйЧ°ЦГµДЖшГЬРФЈ¬ЛщТФґр°ёКЗЈєјмІйЧ°ЦГµДЖшГЬРФЈ»
ЈЁ2.Ј©ІВПл2ЈєSO2±»Fe3+Сх»ЇБЛЈ»ІВПл3ЈєSO2±»NO3©ЃСх»ЇБЛЈ¬Ч°ЦГЦРє¬УРµДСх»ЇјБ»№УРСхЖшЈ¬№КїЙДЬ±»СхЖшСх»ЇЈ¬ЛщТФґр°ёКЗЈєїХЖшУлSO2ЅшИлH2OЦРЈ¬СхЖш°С¶юСх»ЇБтСх»ЇЙъіЙБЛH2SO4Ј»
ЈЁ3.Ј©°ґ№Ыµг2Ј¬Ч°ЦГBЦР·ґУ¦µДАлЧУ·ЅіМКЅКЗSO2+2Fe3++Ba2++2H2O=BaSO4Ўэ+2Fe2++4H+ Ј¬ ЛщТФґр°ёКЗЈєSO2+2Fe3++Ba2++2H2O=BaSO4Ўэ+2Fe2++4H+Ј»
ЈЁ4.Ј©±ыН¬С§№ЫµгКЗФЪSO2УлNO3©Ѓ·ґУ¦Ј¬ФтїЙУГNaNO3ИЬТєЎўBaCl2ИЬТєґъМжBaCl2ИЬТєЎўFeЈЁNO3Ј©3ИЬТєјґїЙЈ¬ѕЯМеІЩЧчОЄЈєЅ«Ч°ЦГCЦРµДИЬТє»»ОЄNaNO3 єНBaCl2µД»мєПИЬТєЈ¬·ґУ¦Т»¶ОК±јдєуЈ¬ИфCЦРіцПЦ°ЧЙ«іБµнЈ¬ФтЦ¤ГчІВПл3ХэИ·Ј¬ЛщТФґр°ёКЗЈє
КµСйІЅЦи | Ф¤ЖЪПЦПуєНЅбВЫ |
Ѕ«Ч°ЦГCЦРµДИЬТє»»ОЄNaNO3 єНBaCl2µД»мєПИЬТєЈ¬ | ·ґУ¦Т»¶ОК±јдєуЈ¬ИфCЦРіцПЦ°ЧЙ«іБµнЈ¬ФтЦ¤ГчІВПл3ХэИ· |


 ФД¶БїміµПµБРґр°ё
ФД¶БїміµПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїВ±ЧеФЄЛШµДµҐЦКєН»ЇєПОпєЬ¶аЈ¬ОТГЗїЙТФАыУГЛщС§ОпЦКЅб№№УлРФЦКµДПа№ШЦЄК¶ИҐИПК¶єНАнЅвЛьГЗЈ®
ЈЁ1Ј©В±ЧеФЄЛШО»УЪФЄЛШЦЬЖЪ±нµДЗшЈ» деµДјЫµзЧУЕЕІјКЅОЄ Ј®
ЈЁ2Ј©ФЪТ»¶ЁЕЁ¶ИµДИЬТєЦРЈ¬Зв·ъЛбКЗТФ¶ю·ЦЧУµЮєПЈЁHFЈ© 2 РОКЅґжФЪµДЈ®К№Зв·ъЛб·ЦЧУµЮєПµДЧчУГБ¦КЗ Ј®
ЈЁ3Ј©ЗлёщѕЭПВ±нМṩµДµЪТ»µзАлДЬКэѕЭЕР¶ПЈ¬ЧоУРїЙДЬЙъіЙЅПОИ¶ЁµДµҐєЛСфАлЧУµДВ±ЛШФЧУКЗЈЁМоГыіЖЈ©Ј®
·ъ | ВИ | де | µв | |
µЪТ»µзАлДЬЈЁkJ/molЈ© | 1681 | 1251 | 1140 | 1008 |
ЈЁ4Ј©ТСЦЄµвЛбЈЁHIO3Ј©єНёЯµвЛбЈЁH5IO6Ј©µДЅб№№·Ц±рИзНјIЎўII ЛщКѕЈє 
Зл±ИЅП¶юХЯЛбРФЗїИхЈєHIO3H5IO6ЈЁМоЎ°ЈѕЎ±ЎўЎ°ЈјЎ±»тЎ°=Ў±Ј©Ј®
ЈЁ5Ј©КФ·ЦОц ClO2©ЃЦРРДВИФЧУµДФУ»ЇАаРН Ј¬ КФРґіцТ»ёц ClO3©ЃµДµИµзЧУМе Ј®
ЈЁ6Ј©Нј1ОЄµвѕ§Меѕ§°ыЅб№№Ј®УР№ШЛµ·ЁЦРХэИ·µДКЗ Ј®
A.µв·ЦЧУµДЕЕБРУР2ЦЦІ»Н¬µДИЎПтЈ¬2ЦЦИЎПтІ»Н¬µДµв·ЦЧУТФ4ЕдО»КэЅ»МжЕдО»РОіЙІгЅб№№
B.УГѕщМЇ·ЁїЙЦЄЖЅѕщГїёцѕ§°ыЦРУР4ёцµвФЧУ
C.µвѕ§МеОЄОЮПЮСУЙмµДїХјдЅб№№Ј¬КЗФЧУѕ§Ме
D.µвѕ§МеЦРґжФЪµДП໥ЧчУГУР·Зј«РФјьєН·¶µВ»ЄБ¦
ЈЁ7Ј©ТСЦЄCaF2ѕ§МеЈЁјыНј2Ј©µДГЬ¶ИОЄ¦Сg/cm3 Ј¬ NAОЄ°ў·ьјУµВВЮіЈКэЈ¬АвЙППаБЪµДБЅёцCa2+µДєЛјдѕаОЄa cmЈ¬ФтCaF2µДПа¶Ф·ЦЧУЦКБїїЙТФ±нКѕОЄ Ј® 
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїИз±нЦРЖАјЫєПАнµДКЗ
СЎПо | »ЇС§·ґУ¦ј°ЖдАлЧУ·ЅіМКЅ | ЖАјЫ |
A | NaHSO4ИЬТєУлBa(OH)2ИЬТє·ґУ¦ЦБ | ХэИ· |
B | ПтМјЛбГѕИЬТєЦРјУИлЧгБїПЎСОЛбЈє | ґнОуЈ¬МјЛбГѕІ»У¦РґіЙАлЧУРОКЅ |
C | Пт·РЛ®ЦРµОјУ±ҐєНµДВИ»ЇМъИЬТєЦБТєМе±дОЄємєЦЙ«ЈєFe3++3H2O | ХэИ· |
D | NaOHИЬТєЦРНЁИлЙЩБїCO2·ґУ¦ЈєOH+CO2 | ХэИ· |
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїЅ«0.050molSO2ЈЁgЈ©єН0.030molO2ЈЁgЈ©·ЕИлИЭ»эОЄ1LµДГЬ±ХИЭЖчЦРЈ¬·ґУ¦2SO2ЈЁgЈ©+O2ЈЁgЈ©2SO3ЈЁgЈ©ЎчHЈј0Ј¬ФЪТ»¶ЁМхјюПВґпµЅЖЅєвЈ¬ІвµГcЈЁSO3Ј©=0.040mol/LЈ®
ЈЁ1Ј©ёГМхјюПВ·ґУ¦µДЖЅєвіЈКэKµДКэЦµОЄ Ј¬ ИзЙэёЯОВ¶ИЈ¬ФтKЦµЈЁМоЎ°ФцґуЎ±ЎўЎ°јхРЎЎ±»тЎ°І»±дЎ±Ј©Ј®
ЈЁ2Ј©ФЪЖдЛыМхјюІ»±дК±
ўЩИфФцґуO2µДЕЁ¶ИЈ¬ФтSO2µДЧЄ»ЇВКЈЁМоЎ°ФцґуЎ±»тЎ°јхРЎЎ±Ј©Ј»
ўЪИфЙэёЯОВ¶ИЈ¬ФтЖЅєвЈЁМоЧЦДёґъєЕЈ©Ј»
AЈ®І»ТЖ¶Ї BЈ®ПтХэ·ґУ¦·ЅПтТЖ¶Ї CЈ®ПтДж·ґУ¦·ЅПтТЖ¶Ї
ўЫУыК№ЖЅєвПтХэ·ґУ¦·ЅПтТЖ¶ЇЗТ·ґУ¦ЛЩВКјУїмЈ¬ПВБРґлК©їЙРРµДКЗ Ј® ЈЁМоЧЦДёґъєЕЈ©
AЈ®ПтЖЅєв»мєПОпЦРідИлAr BЈ®ПтЖЅєв»мєПОпЦРідИлO2
CЈ®К№УГґЯ»ЇјБV2O5 DЈ®ЅµµН·ґУ¦µДОВ¶ИЈ®
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїМъЎўПЎСОЛбЎўіОЗеКЇ»ТЛ®ЎўВИ»ЇНИЬТєКЗіЈјыµДОпЦКЈ¬ЛДЦЦОпЦКјдµД·ґУ¦№ШПµИзНјЛщКѕЎЈНјЦРБЅФІПаЅ»Ії·Ц(AЎўBЎўCЎўD)±нКѕОпЦКјдµД·ґУ¦Ј¬ЖдЦР¶ФУ¦·ґУ¦µДАлЧУ·ЅіМКЅКйРґХэИ·µДКЗ( )
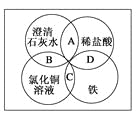
A. OHЈЈ«HCl===H2OЈ«ClЈ
B. Ca(OH)2Ј«Cu2Ј«===Ca2Ј«Ј«Cu(OH)2
C. FeЈ«Cu2Ј«===CuЈ«Fe2Ј«
D. FeЈ«2HЈ«===Fe3Ј«Ј«H2Ўь
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїіш·їЦРіЈУГµДПВБРОпЦКЦРЈ¬КфУЪУР»ъОпµДКЗЈЁ Ј©
A.КіСОB.ЧФАґЛ®C.ХбМЗD.ЅрКфµ¶ѕЯ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї№ШУЪПВБРёчКµСй»тЧ°ЦГµДРрКцЦРЈ¬ХэИ·µДКЗЈЁ Ј© 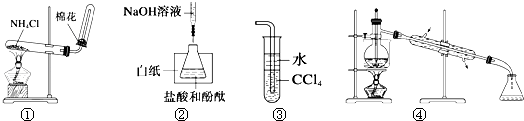
A.КµСйўЩїЙУГУЪЦЖИЎ°±Жш
B.КµСйўЪЦРЧоєуТ»µОNaOH±кЧјТєК№ИЬТєУЙОЮЙ«±дОЄємЙ«Ј¬јґґпµЅµО¶ЁЦХµг
C.Ч°ЦГўЫїЙУГУЪОьКХОІЖшЦРЙЩБїNH3»тHClЈ¬Іў·АЦ№µ№Оь
D.Ч°ЦГўЬїЙУГУЪґУѕЖѕ«Л®ИЬТєЦРЦЖИЎОЮЛ®ТТґј
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїДЙГЧZnSѕЯУР¶АМШµД№вµзР§У¦Ј¬ФЪµзС§ЎўґЕС§Ўў№вС§µИБмУтУ¦УГ№г·єЈ®ТФ№¤Тµ·ПФьРї»ТЈЁЦчТЄіЙ·ЦОЄZnЎўZnOЈ¬»№є¬УРFe2O3ЎўFeOЎўCuOµИФУЦКЈ©ОЄФБПЦЖ±ёДЙГЧZnSµД№¤ТµБчіМИзПВЈє
ЈЁТСЦЄKsp[FeЈЁOHЈ©3]=3.8ЎБ10©Ѓ38Ј» Ksp[CuЈЁOHЈ©2]=2ЎБ10©Ѓ20Ј»KspЈЁZnSЈ©=1.6ЎБ10©Ѓ24Ј©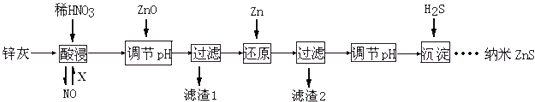
ПВБРЛµ·ЁІ»ХэИ·µДКЗЈЁ Ј©
A.ЛбЅюК±FeOУлПЎHNO3·ґУ¦µДАлЧУ·ЅіМКЅОЄ3FeO+10H++NO3©Ѓ=3Fe3++NOЎь+5H2O
B.Ѕ«ЛбЅюµДОІЖшС»·АыУГЈ¬јУИлµДXЖшМеїЙТФКЗO2
C.ВЛФь2ЦРµДіЙ·ЦєНZnєНFe
D.µ±ИЬТєЦРZn2+ЕЁ¶ИОЄРЎУЪ1.0ЎБ10©Ѓ5molL©Ѓ1К±Ј¬ФтїЙИПОЄЖдіБµнНкИ«Ј®ИфТЄК№Zn2+іБµнНкИ«Ј¬ИЬТєЦРS2©ЃЕЁ¶ИУ¦ґуУЪ1.6ЎБ10©Ѓ19molL©Ѓ1
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїµчІй·ўПЦЈ¬ѕ№эЧ°РЮµДѕУКТЦРЧ°РЮІДБП»б»єВэКН·ЕіцДіР©»ЇС§ОпЦКЈ¬ХвР©ОпЦКЕЁ¶И№эёЯЈ¬»бОЈє¦ИЛµДЙнМеЎЈХвР©ОЫИѕОпЦРЧоіЈјыµДКЗЈЁЎЎЎЎЈ©
A.јЧИ©B.Т»Сх»ЇМјC.¶юСх»ЇБтD.іфСх
Ійїґґр°ёєНЅвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com