
����Ŀ������ZnS���ж��صĹ��ЧӦ���ڵ�ѧ����ѧ����ѧ������Ӧ�ù㷺���Թ�ҵ����п�ң���Ҫ�ɷ�ΪZn��ZnO��������Fe2O3��FeO��CuO�����ʣ�Ϊԭ���Ʊ�����ZnS�Ĺ�ҵ�������£�
����֪Ksp[Fe��OH��3]=3.8��10��38�� Ksp[Cu��OH��2]=2��10��20��Ksp��ZnS��=1.6��10��24��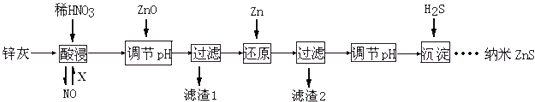
����˵������ȷ���ǣ� ��
A.���ʱFeO��ϡHNO3��Ӧ�����ӷ���ʽΪ3FeO+10H++NO3��=3Fe3++NO��+5H2O
B.�������β��ѭ�����ã������X���������O2
C.����2�еijɷֺ�Zn��Fe
D.����Һ��Zn2+Ũ��ΪС��1.0��10��5molL��1ʱ�������Ϊ�������ȫ����ҪʹZn2+������ȫ����Һ��S2��Ũ��Ӧ����1.6��10��19molL��1
���𰸡�C
���������⣺A������ϡ�����ǿ�����ԣ�����FeO��ϡHNO3��Ӧ���ӷ���ʽΪ��3FeO+10H++NO3��=3Fe3++NO��+5H2O����A��ȷ��
B��ϡ���������β��Ϊһ������������Ҫѭ��������NO��һ����ת�������ἴ4NO+3O2+2H2O=4HNO3 �� ����ͨ���������������������β��ѭ�����ã������X���������O2 �� ��B��ȷ��
C�����������ǿ�����������ܽ�������Һ�к���������������п������ͭ���ӣ��ټ�������п����PHֵ��ʹ�������������������������˳�ȥ���ټ�п�û�����Һ��ͭ�����˳�ȥ���������չ��������Ĵ����û�����ͭ���й�����п����C����
D����Qc��Ksp �� ������ZnS��������S2��Ũ�ȴ��� ![]() =
= ![]() =1.6��10��22 molL��1 �� ��D��ȷ��
=1.6��10��22 molL��1 �� ��D��ȷ��
��ѡC��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E����Ԫ���У�Aԭ�Ӻ����M����ֻ�����ԳɶԵ��ӣ�Bԭ�Ӻ����L���������K���������C�ǵؿ��ں�����������������ߵ�Ԫ�أ�D�ĺ˵������A��C�ĺ˵����֮�ͣ�E��Ԫ�����ڱ��ĸ�Ԫ���е縺�������ش��������⣺
��1��A��B��Ԫ�ط�������Ϊ����
��2��AC2��BC2���ӵ�����ṹ�ֱ����� �� ��ͬ������������ˮ�е��ܽ�Ƚϴ������д����ʽ������������
��3��D�ĺ�������Ų�ʽΪ �� ���γɻ�����ʱ��������ϼ�Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС���Ϊ̽��Fe3+�Ƿ�������SO2 �� �������ͼʵ��װ�ã� 
��1������ͼ���Ӻ�װ�ã�ʵ��ǰӦ��������
��2���۲쵽װ��C�в����˰�ɫ������ͬѧ����������²��루ÿ������ֻ����һ�����ʵ������ԣ���
����1����
����2��SO2��Fe3+�����ˣ�
����3��SO2��NO3��������
��3����ͬѧ��Ϊ����1��ȷ������������װ��A�������ų����ŵ�̽��ʵ�飮
��ͬѧ��Ϊ����2��ȷ����װ��C�з�Ӧ�����ӷ���ʽ��
��4����ͬѧ��Ϊ����3��ȷ�������ü�ͬѧ��ʵ��װ�ã����ʵ����֤���룮���ڱ�����д��ʵ�鲽���Լ�Ԥ������ͽ��ۣ���ѡʵ���Լ���NaNO3��Һ��KSCN��Һ��FeCl3��Һ��BaCl2��Һ��Fe��NO3��3��Һ
ʵ�鲽�� | Ԥ������ͽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������ò�����ѧ���ܵ��ǣ� ��
A.�е���ת�ƣ���ʧ��ƫ�ƣ��Ļ�ѧ��Ӧ����������ԭ��Ӧ
B.p����ԭ�ӹ����ƽ���뾶����Ӳ�����������
C.��������ԭ�Ӻ��⣬�����ɵ͵��ߵIJ�ͬ���Ӳ��Ϸֲ��Ų���
D.��ԭ�ӵ�����ͼ��С�ڵ��ʾ���ӵ��˶��켣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���շ���͡��һ�ֵ���Ѫ֬��ҩ���ṹ��ͼ��ʾ��δ��ʾ����ռ乹�ͣ������й����շ���͡������������ȷ���ǣ� �� 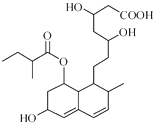
A.����ͨ����Ӧ�γɸ߷��ӻ�����
B.����ʹ����KMnO4��Һ��ɫ
C.�ܷ����ӳɡ�ȡ������ȥ��Ӧ
D.1mol������������1mol NaOH��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʳ�õ��Ƹ����ܹ�Ԥ����Ѫѹ, ��������Ѫ�ܼ��������ʡ�������Ƽ�ָ���ǣ�������
A.ԭ��B.����C.Ԫ��D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ԭ������������˳��(ϡ���������)���Ե�������Ԫ�����ʵ�������ȷ����(����)
A. ԭ�Ӱ뾶�����Ӱ뾶����С
B. �������Ӧ��ˮ������Լ�����������ǿ
C. ���ʵľ������ͽ������塢ԭ�Ӿ���ͷ��Ӿ���
D. ���ʵ��۵㽵��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷�����X��ϩ��Y���Ժϳ����������ռ�BAD��
��֪��G���ܷ���������Ӧ��B��FeCl3��Һ����ɫ��C��D�Ĺ���Ϊ�����Ȼ�����COOH���ķ�Ӧ������BAD�ṹ��ʽΪ�� 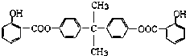
BAD�ĺϳ�·�����£�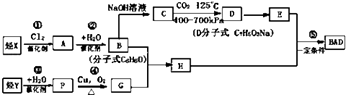
�Իش��������⣺
��1��д���ṹ��ʽYD ��
��2�����ڼӳɷ�Ӧ���У���������ţ� ��
��3��1molBAD�����뺬molNaOH����Һ��ȫ��Ӧ��
��4��д������ʽ��Ӧ�� �� F+E ��
��5��E�ж���ͬ���칹�壬�жϷ�������Ҫ���ͬ���칹����ĿΪ�֣�
���ܷ���������Ӧ����FeCl3��Һ����ɫ�ۺ˴Ź�������ͼ�����ĸ����շ壮
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��֤������������к��е�CO2�������Կ��������������л���ò����ġ�ijѧУѧ������С���������ͼ��ʾװ�ã�����Ϊ��װ��Ӧѡ�õ��Լ��ǣ� ��

A. I��NaOH��Һ II����Ca(OH)2��Һ
B. I��Ca(OH)2��Һ II����NaOH��Һ
C. I��ϡ���� II����Ca(OH)2��Һ
D. I��NaOH��Һ II����CaCl2��Һ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com