
下列实验操作或装置符合实验要求的是( )

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
有两种短周期元素X和Y,可组成化合物XY3,当Y的原子序数为m时,X的原子序数为:①m-4;②m+4;③m+8;④m-2;⑤m+6。其中正确的组合是( )
A.①②④ B.①②⑤ C.①②③⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
为了证明一水合氨(NH3·H2O)是弱电解质,甲、乙、丙三人分别选用下列试剂进行实验:0.01 mol·L-1氨水、0.1 mol·L-1NH4Cl溶液、NH4Cl晶体、酚酞试剂、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.01 mol·L-1氨水的pH为10,则认定一水合氨是弱电解质,你认为这一方法是否正确?(填“是”或“否”)________,并说明理由:_________________________
________________________________________________________________________。
(2)乙取出10 mL 0.01 mol·L-1氨水,用pH试纸测出其pH=a,然后用蒸馏水将其稀释至1 000 mL,再用pH试纸测出其pH为b,若要确认一水合氨是弱电解质,则a、b值应满足什么条件?________________________________________________________________________
(用等式或不等式表示)。
(3)丙取出10 mL 0.0 1 mol·L-1氨水,滴入2滴酚酞溶液,显粉红色,再加入NH4Cl晶体少量,颜色变____________(填“深”或“浅”)。
1 mol·L-1氨水,滴入2滴酚酞溶液,显粉红色,再加入NH4Cl晶体少量,颜色变____________(填“深”或“浅”)。
(4)请你根据所提供的试剂,再提出一个既合理又简便的方案证明一水合氨是弱电解质:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下是实验室常用的部分仪器,请回答下列问题:
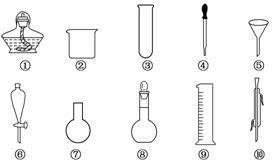
(1)序号为⑧和⑩的仪器的名称分别为__________、__________。
(2)在分液操作中,必须用到上述仪器中的________(填序号)。
(3)能作反应容器且可直接加热的仪器是上述中的________(填名称)。
(4)在配制溶液时,需要用到的仪器是________(填序号)。
(5)仪器上标有温度的是________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室保存下列试剂,其中保存方法和理由描述都正确的是( )
| 编号 | 试剂 | 保存方法 | 理由 |
| A | 钠 | 保存在煤油中 | 防止与空气中水、氧气接触发生反应 |
| B | 液溴 | 密封保存在细口瓶中 | 防止挥发 |
| C | 浓硝酸 | 密封保存在铁器中 | 避免见光分解 |
| D | 烧碱 | 存放在带磨口玻璃塞的广口瓶中 | 防止与空气中氧气接触被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
氯化铜 (CuCl2·2H2O)中含FeCl2杂质。为制得纯净氯化铜晶体,首先将其制成水溶液, 然后按下面所示操作步骤进行提纯。
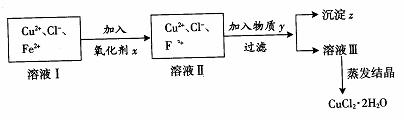
(1)加入氧化剂x的目的是
(2)下列氧化剂中最适合本实验的是
A.Cl2 B.KMnO4 C.NaClO D.H2SO4
(3)物质y和沉淀z的化学式分别是 和
查看答案和解析>>
科目:高中化学 来源: 题型:
氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制流程:

根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为________________________________。
(2)混合①中使用冰水的目的是________________________________。
(3)操作Ⅱ和操作Ⅲ的名称分别是________、________。
操作Ⅲ一般适用于分离________混合物。(选填编号)
a.固体和液体 b.固体和固体
c.互不相溶的液体 d.互溶的液体
(4)混合②中加入Na2SO3的目的是________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色,于是甲乙丙同学设计了简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为________,若假设成立,可观察到的现象为________。乙同学假设工业氢溴酸呈淡黄色是因为________,其用于证明该假设所用的试剂为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com