
【题目】25℃时,用0.1 mol·L-1的HCl溶液逐滴滴入10.00 mL0.1 mol·L-1的NH3·H2O溶液中,其AG值变化的曲线如图所示。已知AG=![]() ,下列分析错误的是
,下列分析错误的是
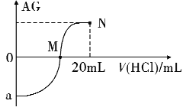
A. 滴定前HC1溶液的AG =12;图中a<0
B. M点为完全反应点,V( HCl) =10 mL,且c(Cl-) >c(NH4+)
C. 从M点到N点水的电离程度先增大后减小
D. N点溶液中:c(Cl-) =2c(NH3·H2O) +2c(NH4+)
【答案】B
【解析】
AG=![]() ,AG>0,说明c(H+)>c(OH-),溶液显酸性,反之AG<0,溶液显碱性。
,AG>0,说明c(H+)>c(OH-),溶液显酸性,反之AG<0,溶液显碱性。
A.滴定前HC1溶液的浓度为0.1 mol·L-1,AG =![]() =lg
=lg![]() =12;图中a为0.1 mol·L-1的NH3·H2O溶液AG,溶液显碱性,故a <0,故A正确;B. M点的AG=0,说明c(H+)=c(OH-),溶液显中性,若氨水与盐酸完全反应,则生成氯化铵,水解后,溶液显酸性,因此M点为盐酸不足,V( HCl) <10 mL,故B错误;C. M点溶液显中性,为氨水和氯化铵的混合溶液,N点为等浓度的盐酸和氯化铵的混合溶液,中间经过恰好完全反应生成氯化铵溶液的点(设为P),从M点到P点,溶液中氨水的物质的量逐渐减小,水的电离程度逐渐增大,从P点到N点,盐酸逐渐增大,水的电离受到的抑制程度逐渐增大,即水的电离逐渐减小,因此从M点到N点水的电离程度先增大后减小,故C正确;D. N点溶液中含有等浓度的盐酸和氯化铵,根据物料守恒,c(Cl-) =2c(NH3·H2O) +2c(NH4+),故D正确;故选B。
=12;图中a为0.1 mol·L-1的NH3·H2O溶液AG,溶液显碱性,故a <0,故A正确;B. M点的AG=0,说明c(H+)=c(OH-),溶液显中性,若氨水与盐酸完全反应,则生成氯化铵,水解后,溶液显酸性,因此M点为盐酸不足,V( HCl) <10 mL,故B错误;C. M点溶液显中性,为氨水和氯化铵的混合溶液,N点为等浓度的盐酸和氯化铵的混合溶液,中间经过恰好完全反应生成氯化铵溶液的点(设为P),从M点到P点,溶液中氨水的物质的量逐渐减小,水的电离程度逐渐增大,从P点到N点,盐酸逐渐增大,水的电离受到的抑制程度逐渐增大,即水的电离逐渐减小,因此从M点到N点水的电离程度先增大后减小,故C正确;D. N点溶液中含有等浓度的盐酸和氯化铵,根据物料守恒,c(Cl-) =2c(NH3·H2O) +2c(NH4+),故D正确;故选B。


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
【题目】向50 mL 14.0 molL﹣1浓硝酸中加入足量铜,充分反应后共收集到标准状况下4.48 L NO和NO2混合气体(不考虑NO2与N2O4的相互转化),则参加反应铜的质量为
A. 6.4gB. 12.8gC. 16.0gD. 19.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化硼是一种超硬耐磨涂层材料。下图为其晶体结构中最小的重复结构单元,其中的每个原子均满足8 电子稳定结构。下列有关说法正确的是
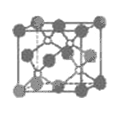
A. 磷化硼晶体的化学式为BP,属于离子晶体
B. 磷化硼晶体中每个原子均形成4个共价键
C. 磷化硼晶体的熔点高,且熔融状态下能导电
D. 磷化硼晶体结构微粒的空间堆积方式与氯化钠相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是过渡金属元素,可以形成多种化合物。
(1)CuCl的盐酸溶液能够与CO发生反应:CuCl+CO+H2O=Cu(CO)Cl·H2O
①电负性:C ______O(填“>”或“=”或“<”)。
②CO常温下为气体,固态时属于 晶体。
(2)Cu+与NH3形成的配合物可表示成[Cu(NH3)n]+,该配合物中,Cu+的4s轨道及4p通过sp杂化接受NH3提供的电子对。
[Cu(NH3)n]+ 中Cu+ 与n个氮原子的空间结构呈 型,n= 。
(3)CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):

请回答下列问题:
①配离子[Cu(En)2]2+的中心原子基态第L层电子排布式为 。
②乙二胺分子中氮原子轨道的杂化类型为 ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是: 。
③配合物[Cu(En)2]Cl2中不存在的作用力类型有 (填字母);
A 配位键 B 极性键 C 离子键 D 非极性键 E.氢键 F.金属键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a | |||||||||||||||||
b | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o | p | |||||||||||||||
试回答下列问题:
(1)元素p为26号元素,请写出其基态原子外围电子排布式:____。
(2)c与a形成6个原子组成分子结构简式:__________,该分子是:_______(填“极性”或“非极性”)分子。
(3)表中O、P两元素的部分电离能数据列于下表:
元 素 | O | P | |
电离能kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态O2+再失去一个电子比气态P2+再失去一个电子难。对此,你的解释是__________________________;
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
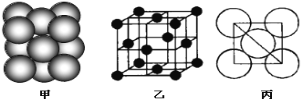
晶胞中i原子的配位数为___________,一个晶胞中i原子的数目为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在碱金属元素中,锂的金属性最弱,其原因是_______________________________________。锂在氧气中燃烧所得产物的化学键类型是________________。
(2)在周期表中,锂的性质与镁相似,预测锂在氮气中燃烧的化学方程式:__________________________。碳酸锂、硫酸锂的溶解性依次为__________、__________(填“易溶”“微溶”或“难溶”)。
(3)锂在自然界中存在的主要形式为锂辉石(LiAlSi2O6)、锂云母[Li2F2Al2(SiO3)3]等。锂辉石(LiAlSi2O6)中化合价最高的元素和锂云母[Li2F2Al2(SiO3)3]中非金属性最强的元素组成的化合物的电子式_________,它是____________(填“离子化合物”或“共价化合物”)。常温常压下,它呈_____态,原因是_____________________。
(4)四氢硼锂(LiBH4)、四氢铝锂(LiAlH4)都是重要还原剂,在有机合成中用途广泛。比较半径:r(Li+)_____r(H—),(填“>”“<”或“=”)理由是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 为四种常见元素,其中 X、Y、Z 为短周期元素。ZX4分子是由粗Z提纯Z的中间产物,X的最高价氧化物对应的水化物为无机酸中的最强酸,Y的离子在同周期中离子半径最小,其氧化物有两性且可用于制造一种极有前途的高温材料,Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料,W原子的最外层电子数小于4且W的常见化合价有+3、+2,WX3 的稀溶液呈黄色,回答下列问题:
(1)X在元素周期表的位置________________,其简单阴离子的结构示意图为____________________,用电子式表示X的氢化物的形成过程______________________________。
(2)Z的氧化物在通讯领域用来作_______________。锗与Z是同一主族元素,它可用来制造半导体晶体管。研究表明:有机锗具有明显的抗肿瘤活性,锗不与 NaOH溶液反应但在有 H2O2 存在时可与NaOH溶液反应生成锗酸盐,反应的化学方程式为:_______________________________
(3)W(OH)2 在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为:____________________________________,若灼烧W(OH)2 固体得到___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氯酸钠(NaClO3)等为原料制备亚氯酸钠(NaClO2)的工艺流程如下,下列说法中,不正确的是
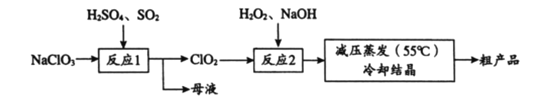
A. 反应1中,每生成1 mol ClO2有0.5 mol SO2被氧化
B. 从母液中可以提取Na2SO4
C. 反应2中,H2O2做氧化剂
D. 采用减压蒸发可能是为了防止NaClO2受热分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术的关键原料之一。
(l)三氟化氮可由氨气和氟气反应得到: 4NH3+3F2=NF3+3NH4F。NH3的电子式为__________,反应中氨气显示的化学性质有______________,当有17.0 g氨气发生反应时,转移电子的物质的量为_____。
(2)在潮湿的空气中,NF3能与水蒸气发生反应,产物有HF、NO和一种酸,则被氧化与被还原元素原子的物质的量之比为_________,NF3、F2、NO三种气体氧化性由弱到强的顺序为_________。
(3)三氟化氮在空气中泄露时,很易被发现,依据的现象是______________________。
(4)NCl3结构类似NF3,但NCl3中N元素显-3价,NCl3遇水发生反应,目反应为非氧化还原反应,该反应的化学方程式为____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com