
【题目】图中a、b、c、d、e为周期表短周期的一部分元素,下列叙述正确的是( )

A. b元素除0价外,只有一种化合价
B. a的晶体中只有一种作用力
C. b、e简单气态氢化物的稳定性:b<e
D. d元素的第一电离能是同周期元素中最大的
【答案】B
【解析】
a、b、c、d、e为元素周期表短周期中的部分元素,根据它们在元素周期表中的相对位置知,a、b、c、d、e分别是He、O、Si、Cl、N元素。据此分析解答。
A.b是O元素,O元素除了0价外还有-1价、-2价,故A错误;
B.a为He,属于稀有气体元素,单质为单原子分子,形成的晶体中只有一种作用力——分子间作用力,故B正确;
C.元素的非金属性越强,简单气态氢化物越稳定,非金属性O>N,简单气态氢化物的稳定性:b>e,故C错误;
D.同一周期,从左到右,元素的第一电离能呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素,第三周期中,第一电离能最大的为Ar,故D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】化锡(SnI4)是一种橙黄色结晶,熔点为 144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿、四氯化碳等,遇水易水解,常用作分析试剂和有机合成试剂。实验室制备四氯化锡的主要步骤如下:
步骤1:将一定量锡、碘和四氯化碳加入干燥的烧瓶中,烧瓶上安装如图装置Ⅰ和Ⅱ。

步骤2:缓慢加热烧瓶,待反应停止后,取下冷凝管,趁热迅速进行过滤除去未反应的锡。用热的四氯化碳洗涤漏斗上的残留物,合并滤液和洗液,用冰水浴冷却,减压过滤分离。
步骤3:滤下的母液蒸发浓缩后冷却,再回收晶体。
请回答下列问题
(1)图中装置II的仪器名称为___________,该装置的主要作用是____________。
(2)减压过滤的操作有①将含晶体的溶液倒入漏斗,②将滤纸放入漏斗并用水润湿,③微开水龙头,④开大水龙头,⑤关闭水龙头,⑥拆下橡皮管。正确的顺序是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,乳酸成为研究热点之一。乳酸可以用化学方法合成,也可以由淀粉通过发酵法制备。利用乳酸![]() 为原料制成的高分子材料具有生物兼容性,而且在哺乳动物体内或自然环境中都可以最终降解成为二氧化碳和水。乳酸还有许多其他用途。
为原料制成的高分子材料具有生物兼容性,而且在哺乳动物体内或自然环境中都可以最终降解成为二氧化碳和水。乳酸还有许多其他用途。
(1)请写出乳酸分子中官能团的名称___、___。
(2)乳酸能与纯铁粉反应制备一种补铁药物--乳酸亚铁,反应如下,计算乳酸亚铁中铁的质量分数为___。

(3)乳酸聚合成的纤维非常适合做手术缝合线,其原因是___。
(4)乳酸发生下列变化:
![]()
所用的试剂是a___,b___(写化学式)
(5)请写出乳酸与少量的Na2CO3溶液反应的化学方程式___。
(6)乳酸乙酯(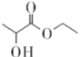 )是一种食用香料,常用于调制果香型、乳酸型食用和酒用精。乳酸乙酯的同分异构体M有如下性质:0.1molM分别与足量的金属钠和碳酸氢钠反应,产生的气体在相同状况下的体积相同,则M的结构最多有___(不考虑空间异构)种。
)是一种食用香料,常用于调制果香型、乳酸型食用和酒用精。乳酸乙酯的同分异构体M有如下性质:0.1molM分别与足量的金属钠和碳酸氢钠反应,产生的气体在相同状况下的体积相同,则M的结构最多有___(不考虑空间异构)种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物D的一种合成路线如下:
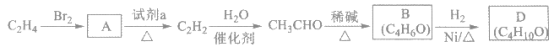
已知:![]()
 +H2O(R、R'表示烃基或氢)
+H2O(R、R'表示烃基或氢)
(1)由C2H4生成A的化学方程式是___________。
(2)试剂a是________。
(3)写出B中所含官能团的名称________。
(4)有机物D的结构简式是________。
(5)请以乙烯为起始原料,以CH3CH=CHCOOH为目标产物,结合已知信息选择必要的无机试剂,写出合成路线。_______(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行铜与浓硫酸的反应,并探究产物的性质(夹持装置已略去)。

(1)试管①中发生反应的化学方程式是_________,此反应中浓硫酸显_______性;
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是_____________;
(3)若试管②中的试剂为酸性 KMnO4溶液,实验时,观察到溶液褪色,则说明生成的气体具有_____性;
(4)若试管中②的试剂是硫化氢水溶液,写出反应方程式__________________;
(5)试管③中的试剂为_____,其作用是______,反应的离子方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟离子电池是一种前景广阔的新型电池,其能量密度是目前锂电池的十倍以上且不会因为过热而造成安全风险。如图是氟离子电池工作示意图,其中充电时F-从乙电极流向甲电极,下列关于该电池的说法正确的是( )

A.放电时,甲电极的电极反应式为Bi-3e-+3F-=BiF3
B.放电时,乙电极电势比甲电极高
C.充电时,导线上每通过1mole-,甲电极质量增加19g
D.充电时,外加电源的正极与乙电极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,体积均为25. 00 mL,浓度均为0.0100 mol/L的HA、H3B溶液分别用0.0100mol/L NaOH溶液滴定,溶液的pH随V(NaOH)变化曲线如图所示,下列说法中正确的是

A.NaOH溶液滴定HA溶液可选甲基橙作指示剂
B.均为0. 0100 mol/L HA、H3B溶液中,酸性较强的是HA
C.25℃时,0. 0100 mol/L Na2HB溶液的pH >7
D.25℃时,向Na2HB溶液中滴加HA溶液反应的离子方程式为:HB2- + HA == H2B- + A-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某化学兴趣小组的同学学习元素周期律时设计的两套实验方案。
【实验一】实验步骤如下:
实验序号 | 实验步骤 |
① | 向新制的Na2S溶液中滴加新制的氯水 |
② | 将镁条投入1mol/L的稀盐酸中 |
③ | 将铝条投入1mol/L的稀盐酸中 |
(1)设计该实验方案的目的是:探究同周期元素的__________________________。
(2)实验①的现象是 ,反应的化学方程式是 。
【实验二】 为验证Cl2、Br2的非金属性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如下图。
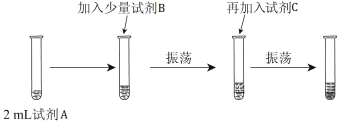
(3)试剂A是 ;试剂B是 ;试剂C是 。
(4)试剂C在实验中所起的作用是 ,加入C振荡、静置后看到的现象是: 。以上反应可以证明Cl2的非金属性_______(填“强于”或“弱于”)Br2的非金属性,反应的离子方程式为:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铝在生产生活中有着广泛的用途。回答下列问题:
(1)铝元素在周期表中的位置是_______________。
(2)比较原子结构示意图:它们的共同之处是___________![]() 选填编号,下同
选填编号,下同![]() ;不同之处是___________。
;不同之处是___________。
a.电子层数b.次外层电子数c.最外层电子数d.质子数
(3)常温下铝制容器可以用来盛放浓硫酸而不被溶解,这种现象称为___________。
氢氧化铝和盐酸反应的化学方程式为_________________________________。
能把溶液中的铁离子和铝离子分离开的试剂是___________。![]() 选填编号
选填编号![]()
a.盐酸b.硫酸铜溶液 c.氨水 d.氢氧化钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com