
����Ŀ�����顢��ϩ����Ȳ���Ǽ���������һ�����顢����ϩ���Ҵ�����ȩ�����ᡢ�����������к���Ҫ����;��
(1)��Ȳͨ����ˮ������________����������ȡһ������ķ�Ӧ����_________������ϩ��ȡ�Ҵ��ķ�Ӧ����__________��
(2)һ����������еĹ�����Ϊ_________��������ϩ�Ľṹ��ʽΪ__________��
(3)д�����Ҵ�������ϩ�Ļ�ѧ��Ӧ����ʽ__________��
(4)д�������һ��ͬ���칹��Ľṹ��ʽ_________�������ͬ���칹���Ƿ���ȩ������__________��
(5)�Ҷ���(HOCH2CH2OH)Ҳ��һ�ֺ���Ҫ�Ļ���ԭ�ϣ��������һ������ϳ��Ҷ�����·��ͼ�����ϳ�·�߳��õı�ʾ��ʽΪ��A![]() Ŀ������___________��
Ŀ������___________��
���𰸡���ˮ��ɫ ���� �ӳɷ�Ӧ ��ԭ�ӻ�-Cl ![]() CH3CH2OH
CH3CH2OH![]() CH2=CH2��+H2O HCOOCH3 ȡ������������������ͭ����Һ�����ȣ�������(ש)��ɫ������֤������ȩ������û�к�ɫ������֤��û��ȩ�� CH3CH2Cl
CH2=CH2��+H2O HCOOCH3 ȡ������������������ͭ����Һ�����ȣ�������(ש)��ɫ������֤������ȩ������û�к�ɫ������֤��û��ȩ�� CH3CH2Cl CH2=CH2
CH2=CH2![]() ClCH2CH2Cl
ClCH2CH2Cl![]() HOCH2CH2OH
HOCH2CH2OH
��������
(1)��Ȳ�������ͼ�����������ˮ�����ӳɷ�Ӧ�����鷢��ȡ����Ӧ����һ�����飬��ϩ�����ӳɷ�Ӧ�����Ҵ���
(2)һ�����麬�еĹ�����Ϊ��ԭ�ӣ�����ϩΪ��ϩ�ļӾ۲��
(3)�Ҵ���Ũ�����ϼ���170�棬������ȥ��Ӧ������ϩ��ˮ��
(4)������������Ϊͬ���칹�壻�������Ʊ���������ͭ��Һ����ȩ����
(5)��һ������ϳ��Ҷ��������ȷ�����ȥ��Ӧ�������������������ӳɷ�Ӧ����1��2-�������飬1��2-��������������������Һ��ˮ��������Ҷ�����
(1)��Ȳ�����к�������̼̼��������������ˮ�����ӳɷ�Ӧ��ʹ��ˮ��ɫ�������������ڹ��������·���ȡ����Ӧ����һ�����飬��Ӧ����Ϊ���գ���ϩ�����к������͵�̼̼˫����������H2O�����ӳɷ�Ӧ�����Ҵ���
(2)һ�����黯ѧʽ��CH3CH2Cl�����еĹ�����Ϊ��ԭ�ӣ�����ϩΪ��ϩ�ļӾ۲���ṹ��ʽΪ![]() ��
��
(3)�Ҵ���Ũ�����ϼ���170�棬������ȥ��Ӧ������ϩ��ˮ��������ϩ�Ļ�ѧ��Ӧ����ʽΪ��CH3CH2OH![]() CH2=CH2��+H2O��
CH2=CH2��+H2O��
(4)ͬ���칹���Ƿ���ʽ��ͬ���ṹ��ͬ�Ļ�����������ʽ��C2H4O2��������������Ϊͬ���칹�壬��������ṹ��ʽΪHCOOCH3�������к���ȩ�����������Ʊ���������ͭ��Һ����ȩ��������Ϊ��ȡ������������������ͭ����Һ�����ȣ�������(ש)��ɫ������֤������ȩ������û�к�ɫ������֤��û��ȩ����
(5)��һ������ϳ��Ҷ�����һ����������NaOH���Ҵ���Һ�У��ڼ��������·�����ȥ��Ӧ���� CH2=CH2��CH2=CH2�������������ӳɷ�Ӧ����1��2-��������CH2Cl-CH2Cl��Ȼ��CH2Cl-CH2Cl������������Һ���ڼ��������·���ˮ�ⷴӦ�������Ҷ������Ʊ�����ΪCH3CH2Cl CH2=CH2
CH2=CH2![]() ClCH2CH2Cl
ClCH2CH2Cl![]() HOCH2CH2OH��
HOCH2CH2OH��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F�ĺ˵�������������Ҿ�Ϊ�˵����С��18�ķ�ϡ������Ԫ�ء�A�ĵ�������Ȼ�����ܶ���С�����壬A��C���γ�A2C��A2C2���ֳ�����Һ̬�����B��Cԭ�ӵ�����������֮�͵���11��D����C�ļ����ӵĺ�������Ų���ͬ��C��Eԭ�ӵ�������������ͬ����ش��������⣺
��1��д��Ԫ�ط��ţ�B______��D______��
��2��AԪ�ؾ����������ӵĺ��صı�ʾ����Ϊ_____��E�ļ����ӵĽṹʾ��ͼ��______��
��3��A2C2�ķ���ʽΪ________��
��4��������F�ĵ���ͨ����������������Һ�У�������Ӧ�����ӷ���ʽ��_________________________________________________��
��5����״���£��Թ����ռ���F�ļ��⻯�������ˮ��(�������ʲ����Թ�����ɢ)��һ��ʱ����Թ�����Һ�����ʵ����ʵ���Ũ��Ϊ____________mol��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ի�����Ϊԭ���Ʊ������ϩ�ĺϳ�·�ߣ�
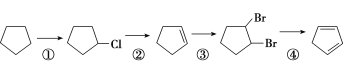
(1)��Ӧ�ٵIJ���������________����Ӧ�Ļ�ѧ����ʽΪ___________________��
(2)��Ӧ�ڵķ�Ӧ�Լ��ͷ�Ӧ������________����Ӧ�۵ķ�Ӧ������________��
(3)![]() ��NaOHˮ��Һ��Ӧ�Ļ�ѧ����ʽ________________________��
��NaOHˮ��Һ��Ӧ�Ļ�ѧ����ʽ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A~D����ѧʵ���г����ļ����¶ȼ�װ��ʾ��ͼ��
��1�������~����ѡȡ������ʹ���¶ȼƵ�ʵ�飬ѡ��A��Bװ���ʺϵ�ʵ����д�ո�
���ƾ���Ũ�����ϼ�������ϩ������ʯ��ˮ��Ӧ����Ȳ��������������������Ļ������������ȡ����Ӧ����ʯ�ͷ���ʵ�飬��Ũ����Ͷ������̻�ϼ���������
A | B | C |
|
|
|
_____________ | ___________ |
����Ũ����;ƾ��Ļ��˳��Ϊ_________________________��д��ʵ��������ϩ�Ļ�ѧ����ʽ____________________________��
����Ϊ�˻���ȶ�����������___________����ˮ��д��ʵ��������Ȳ�Ļ�ѧ����ʽ___________________________________��
��2��ѡ��װ��C����������ʵ�飬D�г������ܵ�������_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ��е����λ����ͼ��ʾ����Zԭ�ӵ������������ǵ�һ���������3��������˵������ȷ����( )
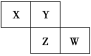
A. X�������̬�⻯���ˮ��Һ������
B. ����������Ӧˮ���������W��Zǿ
C. Z�ĵ�����������Ӧ��Y������������Ӧ����
D. X��ԭ�Ӱ뾶С��Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25���101kPaʱ�����顢��Ȳ�ͱ�ϩ��ɵĻ����20mL�������������ϲ���ȫȼ�գ���ȥˮ�������ָ���ԭ�����¶Ⱥ�ѹǿ�������������С��40mL��ԭ���������Ȳ���������Ϊ ( ��)
A. 12.5%B. 25%C. 50%D. 75%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ж��ַ�����ͬλ�ء�![]() I�׳�����131�����㷺������ҽѧ��ϣ���Ϊ�ټ��ͼ�״���ڷ���ʧ��֢�����ơ������й�
I�׳�����131�����㷺������ҽѧ��ϣ���Ϊ�ټ��ͼ�״���ڷ���ʧ��֢�����ơ������й�![]() I������ȷ���ǣ� ��
I������ȷ���ǣ� ��
A.��Ԫ�ص����ԭ������Ϊ131
B.![]() I��һ���·��ֵĵ�ĺ���
I��һ���·��ֵĵ�ĺ���
C.![]() Iλ��Ԫ�����ڱ��е������ڢ�A��
Iλ��Ԫ�����ڱ��е������ڢ�A��
D.![]() I���ڵ�����������������֮��Ϊ29
I���ڵ�����������������֮��Ϊ29
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2Sˮ��Һ�д��ڵ���ƽ��H2S![]() H++HS-��HS-
H++HS-��HS-![]() H++S2-������H2S��Һ��
H++S2-������H2S��Һ��
A.��ˮ��ƽ�������ƶ�����Һ��������Ũ������
B.ͨ�����SO2���壬ƽ�������ƶ�����ҺpHֵ����
C.�μ�������ˮ��ƽ�������ƶ�����ҺpHֵ��С
D.������������ͭ���壨��������仯������Һ����������Ũ�ȶ���С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B�������ʵķ���ʽ����C7H8O�����Ƕ��ܸ������Ʒ�Ӧ�ų�������A������NaOH��Һ����B������NaOH��Һ��B��ʹ������ˮ��ɫ����������ɫ��������A���ܡ�B�����ϵ�һ����������ֽṹ��
(1)д��A��B�Ľṹ��ʽ��A________��B________��
(2)д��B��NaOH��Һ������Ӧ�Ļ�ѧ����ʽ�� _____________________��
(3)A������Ʒ�Ӧ�Ļ�ѧ����ʽΪ____________�������������Ʒ�Ӧ���ɵ���H2���ֱ���A��B��H2O�������ʵ����ʵ���֮��Ϊ________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com