
【题目】观察下面几种烷烃的球棍模型


(1)与C互为同系物的是__,与C互为同分异构体的是__。
(2)在烷烃的同系物中,随碳原子数增加,其熔、沸点依次___(其中碳原子数满足__条件的烷烃常温下呈气态),液态时密度依次__。
【答案】AB D 升高 小于等于4 增大
【解析】
从烷烃的球棍模型可以看出,A为丙烷,B为丁烷,C为戊烷,D为2-甲基丁烷;
(1)C分子内含有5个碳原子,而A分子内含有3个碳原子,B分子内含有4个碳原子,D分子内含有5个碳原子;
(2)在烷烃的同系物中,随碳原子数增加,相对分子质量增大,分子间作用力增大 (其中碳原子数满足不大于4条件的烷烃常温下呈气态),液态时密度也随相对分子质量的增大而增大;
(1)同系物所含碳原子数一定不同,属于同分异构体的烷烃,碳原子数一定相同,所以与C互为同系物的是A、B,与C互为同分异构体的是D。答案为:A、B;D;
(2)在烷烃的同系物中,随碳原子数增加,相对分子质量增大,分子间作用力增大,其熔、沸点依次升高(其中碳原子数满足小于等于4条件的烷烃常温下呈气态),液态时密度依次增大。答案为:升高;小于等于4;增大。


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】原电池是化学对人类的一项重大贡献。
Ⅰ(1).某兴趣小组为研究原电池原理,设计如图装置。a和b不连接时,烧杯中发生反应的现象是___________________________。
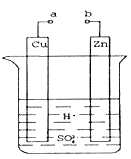
(2)a和b用导线连接,Cu极为原电池___________ (填“正”或“负”)极,电极反应式是___________ ,发生__________(填“氧化”或“还原”)反应。
(3)将a与直流电源的正极相连并把Cu换成石墨电极,b与直流电源的负极相连,则石墨电极反应式 ______________________,该过程的总反应方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D都是元素周期表中的短周期元素,它们的核电荷数依次增大.A是元素周期表中原子半径最小的元素,非金属元素B原子的核外电子数是未成对电子数的3倍,C原子的最外层p轨道的电子为半充满结构,D是地壳中含量最多的元素,E位于第4周期,其基态原子的内层轨道全部排满电子,且最外层电子数与A相同。回答下列问题:
⑴E的基态原子价电子排布图 ______ 。
⑵B、C、D的第一电离能由小到大的顺序为 ______ 。![]() 用元素符号表示
用元素符号表示![]()
⑶CA3物质能与很多化合物通过配位键发生相互作用,CA3与第2周期中的另一种元素的氢化物相互作用得到的化合物X是科学家潜心研究的一种储氢原料,X是乙烷的等电子体;加热X会缓慢释放H2,转变为化合物Y,Y是乙烯的等电子体。
![]() 化合物CA3的分子空间构型为 ______ ,X的结构式为 ______
化合物CA3的分子空间构型为 ______ ,X的结构式为 ______ ![]() 必须标明配位键
必须标明配位键![]() 。
。
![]() 形成CA3物质的中心原子在X、Y分子中的杂化方式分别是 ___,Y分子中δ键和π键数目之比为 ____。
形成CA3物质的中心原子在X、Y分子中的杂化方式分别是 ___,Y分子中δ键和π键数目之比为 ____。
⑷E能与类卤素(SCN)2反应生成E(SCN)2,类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H—S—C![]() N)的沸点低于异硫氰酸(H—N
N)的沸点低于异硫氰酸(H—N![]() C
C![]() S)的沸点,其原因是 ______ 。
S)的沸点,其原因是 ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一瓶签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合制剂,某同学为了确认其成分,取部分制剂作为试液,设计并完成了如下实验:

已知:控制溶液pH=4时,Fe(OH)3沉淀完全,Ca2+、Mg2+不沉淀。
该同学得出的结论正确的是
A. 根据现象1可推出该试液中含有Na+
B. 根据现象2可推出该试液中并不含有葡萄糖酸根
C. 根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+
D. 根据现象5可推出该试液中一定含有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是可以综合利用的。从海水中提取食盐和溴的过程如下:

(1)请写出一种海水淡化的方法:__。
(2)步骤Ⅰ获取Br2的离子方程式为___。
(3)步骤Ⅱ用SO2水溶液吸收Br2,使溴蒸气转化为氢溴酸以达到富集的目的。其反应的化学方程式为Br2+SO2+2H2O=H2SO4+2HBr,在该反应中,氧化剂是__(填化学式)。若反应中生成2molHBr,则消耗___molSO2。
(4)根据上述反应判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下向不同电解质溶液中加入新物质时,溶液导电性会发生变化。下列图示中,电流强度(I)随新物质加入量(m)的变化趋势与实验过程相符合的是

A. 向CH3COOH溶液中逐渐通入NH3至过量
B. 向NH4Cl溶液中逐渐加入NaOH固体至过量
C. 向Ba(OH)2溶液中滴入等浓度的硫酸至过量
D. 向NaAlO2溶液中滴入等浓度的盐酸至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往含Cl-和I-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示。下列说法正确的是
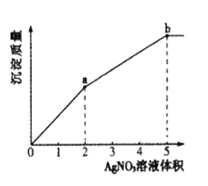
A.KSP (AgCl) < KSP (AgI)
B.c( Cl- ) :c( I-) =3:2
C.m( AgCl ) :m( AgI ) =" 2" :3
D.a~b段产生黄色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液X含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的几种,已知该溶液中各离子物质的量浓度均为
中的几种,已知该溶液中各离子物质的量浓度均为![]() 不考虑水的电离及离子的水解
不考虑水的电离及离子的水解![]() 。为确定该溶液中含有的离子,现进行了如下的操作:
。为确定该溶液中含有的离子,现进行了如下的操作:
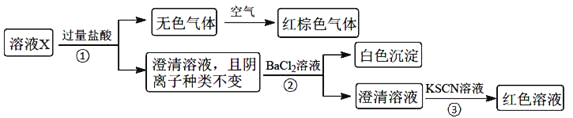
下列说法正确的是![]()
A.无色气体可能是NO和![]() 的混合物
的混合物
B.由步骤![]() 可知,原溶液肯定存在
可知,原溶液肯定存在![]()
C.溶液X中所含离子种类共有4种
D.另取100mL原溶液X,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的固体质量为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将足量的BaSO4固体溶于50 mL水中,充分搅拌,慢慢加入Na2CO3固体,随着c(![]() )增大,溶液中c(Ba2+)的变化曲线如图所示。则下列说法正确的是
)增大,溶液中c(Ba2+)的变化曲线如图所示。则下列说法正确的是

A. 该温度下Ksp(BaSO4)>Ksp(BaCO3)
B. 加入Na2CO3固体,立即有BaCO3固体生成
C. BaCO3的Ksp=2.5×10-10
D. 曲线BC段内,c(![]() )∶c(
)∶c(![]() )=25
)=25
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com