
【题目】某化学小组拟设计实验探究SO2与钙盐溶液的反应情况。
(文献资料)
①CaSO3是难溶于水、易溶于盐酸的白色固体;
②实验室用Na2SO3粉末和80%硫酸反应制备SO2;
③浓硫酸与水混合时放出大量的热,产生大量“酸雾”。
(设计实验)
实验Ⅰ:探究二氧化硫与氯化钙溶液反应。
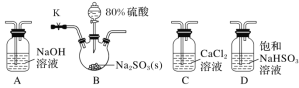
(1)若气体从左至右流动,选择装置并排序为________(填代号)。
(2)D装置作用是___________________________________________
(用离子方程式表示)。
(3)连接装置进行实验,发现C装置中产生白色沉淀。
①甲同学对白色沉淀成分提出如下假设:
假设1:白色固体是CaSO3;
假设2:白色固体是CaSO4;
假设3:白色固体是CaSO4和CaSO3。
②乙同学设计实验证明白色沉淀是CaSO4,他的实验方案是_____________________________________。
③丙同学认为C中生成硫酸钙的原因是装置内O2氧化了SO2。
排除装置内O2干扰采取的措施是:在启动B中反应之前,____________(填实验步骤)
重新实验,C中无明显现象,所以SO2和CaCl2溶液不反应。
实验Ⅱ:探究SO2和Ca(ClO)2溶液反应。
丁同学仅将上述实验C装置中氯化钙溶液换成漂白精溶液,进行实验时产生了大量白色沉淀。
(4)化学反应有两种情况。
①若SO2过量,则发生反应为Ca(ClO)2+2SO2+2H2O===CaSO4↓+2HCl+H2SO4
②若SO2少量,则发生反应为_____________________________________________________。
(5)为了探究C中SO2是否过量,戊同学取少量C中上层清液于试管中,加入下列物质可以达到实验目的的是________(填字母)。
a.NaHCO3溶液 b.品红溶液
c.AgNO3溶液 d.紫色石蕊溶液
【答案】BDCA ![]() +H+===SO2↑+H2O 取少量白色固体于试管,加入盐酸,白色固体不溶解 打开K,通入一定时间N2(或Ar) Ca(ClO)2+SO2+H2O===CaSO4↓+HClO+HCl bd
+H+===SO2↑+H2O 取少量白色固体于试管,加入盐酸,白色固体不溶解 打开K,通入一定时间N2(或Ar) Ca(ClO)2+SO2+H2O===CaSO4↓+HClO+HCl bd
【解析】
(1)浓硫酸与亚硫酸钠反应时会形成酸雾,酸雾中含有硫酸,所以SO2中混有硫酸;
(2)用饱和亚硫酸氢钠溶液除去SO2中的“酸雾”;
(3)②利用硫酸钙不溶于盐酸,亚硫酸钙溶于盐酸;
③打开K,向装置内通入N2(或Ar)等惰性气体,将装置内空气排出来,避免干扰。
(4)观察、分析SO2过量、少量的产物不完全相同;
(5)将问题转化成“检验次氯酸、硫酸”,利用次氯酸具有漂白性。
(1)阅读文献知,浓硫酸与亚硫酸钠反应时会形成酸雾,酸雾中含有硫酸,所以SO2中混有硫酸,如果不净化SO2,硫酸与氯化钙反应产生硫酸钙。实验装置顺序:制备SO2、除去SO2中酸雾、SO2与氯化钙溶液反应、吸收尾气等。
(2)类似除去CO2气体中氯化氢,用饱和亚硫酸氢钠溶液除去SO2中的“酸雾”,化学方程式为2NaHSO3+H2SO4===Na2SO4+2SO2↑+2H2O。
(3)②利用硫酸钙不溶于盐酸,亚硫酸钙溶于盐酸。不能选择硝酸与白色沉淀反应,因为3CaSO3+2HNO3===3CaSO4↓+2NO↑+H2O。
③空气中氧气干扰,其过程为SO2+H2O===H2SO3,2H2SO3+O2===2H2SO4,CaCl2+H2SO4===CaSO4↓+2HCl。装置B中还有导管未用,可以打开K,向装置内通入N2(或Ar)等惰性气体,将装置内空气排出来,避免干扰。
(4)观察、分析SO2过量、少量的产物不完全相同。如果SO2少量,部分次氯酸没有被还原,即产物有次氯酸。
(5)将问题转化成“检验次氯酸、硫酸”,利用次氯酸具有漂白性,用品红溶液、紫色石蕊溶液检验,故选bd。


科目:高中化学 来源: 题型:
【题目】二氧化锰是制造锌锰干电池的基本材料,工业上以软锰矿、菱锰矿为原料来制备。某软锰矿主要成分为MnO2,还含有Si(16.27%),Fe(5.86%),Al(3.42%),Zn(2.68%)和Cu(0.86%)等元素的氧化物,其处理流程图如下:
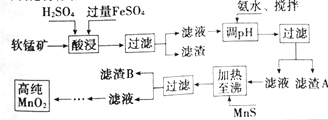
化合物 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
KSP近似值 | 10-34 | 10-16 | 10-38 |
(1)灼烧软锰矿样品时,铜的焰色为___(填字母)。
A.黄色 B.绿色 C.紫色 D.红色
(2)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要离子反应方程式为___。
(3)“氨水、搅拌”,其中“搅拌”不仅能加快反应速率,还能___。滤渣S的成分是Fe(OH)3、Al(OH)3,加入氨水需调节pH至少达到___,恰好能使Fe3+、Al3+沉淀完全(当c≤10-5mol·L-1时,认为该离子沉淀完全)。
(4)滤渣B的成分是___。
(5)工业上采用间接氧化还原滴定法测定MnO2纯度,其操作过程如下:准确称量0.9200g该样品,与足量酸性KI溶液充分反应后,配制成100mL溶液。取其中10.00mL,恰好与25.00mL0.0800 mol·L-1 Na2S2O3溶液反应(I2+2S2O32-=2I-+S4O62-)。计算该样品纯度为___%(精确到0.1%)。
(6)从废旧碱性锌锰电池中可以回收利用的物质有___(写两种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用 NA 表示阿伏加德罗常数的值。下列有关说法正确的是
A.3 g 乙烷中所含共价键数目为 0.6 NA
B.1 mol CH3+中含电子数为 10 NA
C.4.6 g 甲酸和二甲醚(CH3OCH3)的混合物中所含分子数为 0.1 NA
D.标准状况下,11.2 L 苯完全燃烧后生成的 CO2 分子数为 3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。

下列说法正确的是( )
A. 沸点A2D<A2X
B. CA3分子是非极性分子
C. C形成的单质中σ键与π键个数之比为1∶2
D. B、C、D形成的气态氢化物互为等电子体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
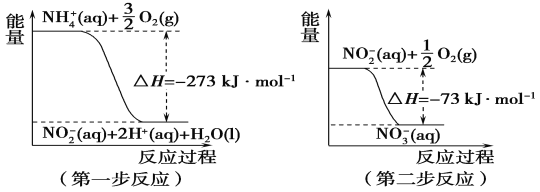
①第一步反应是________(填“放热”或“吸热”)反应。
②1 mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式:__________________。
(2)在298 K、101 kPa时,已知:2H2O(g)=O2(g)+2H2(g) ΔH1;
Cl2(g)+H2(g)=2HCl(g) ΔH2;
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3。
则ΔH3与ΔH1和ΔH2之间的关系正确的是___________。
A.ΔH3=ΔH1+2ΔH2 B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2 D.ΔH3=ΔH1-ΔH2
(3)已知红磷比白磷稳定,则反应P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1;P(红磷,s)+5O2(g)=2P2O5(s) ΔH2;ΔH1和ΔH2的关系是ΔH1_________ΔH2(填“>”、“<”或“=”)。
(4)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72 kJ/mol,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
物质 | H2(g) | Br2(g) | HBr(g) |
1 mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
则表中a=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含CH3COOH和CH3COO-的溶液中, CH3COOH、CH3COO-二者中各自所占的物质的量分数(a)随溶液pH变化的关系如图所示。

下列说法不正确的是
A. 在pH<4.76的溶液中,c(CH3COO-)<c(CH3COOH)
B. 在pH=7的溶液中,a(CH3COOH)=0,a(CH3COO-)=1.0
C. 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+)
D. 在pH=4.76的溶液中加盐酸,a(CH3COOH)与a(CH3COO-)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuBr(溴化亚铜)是一种白色固体,不溶于水,在空气中会慢慢被氧化成绿色粉末,常用作催化剂,可用下图所示实验制得。
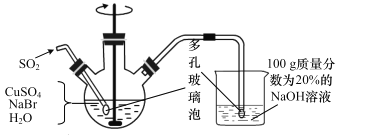
三颈烧瓶中的反应为 2Cu2++SO2+2Br-+2H2O=2CuBr↓+SO42-+4H+。
(1)实验所用蒸馏水需煮沸,目的是_______________。装置中使用多孔玻璃泡的目的是___________。
(2)将反应后得到的 CuBr 过滤并洗涤,检验 CuBr 是否洗净的方法是______。
(3)烧杯中若 NaOH 的量不足,则烧杯中最终所得溶液中的溶质是__________。
(4)CuBr 在空气中氧化所得绿色粉末为 xCuBr2·yCu(OH)2,为探究该粉末的化学式, 现进行如下实验:准确称取一定质量的绿色粉末,溶于足量乙酸中,用蒸馏水配制成 100 mL 溶液。
①取 25 mL 溶液,向其中加入足量的 AgNO3 溶液,充分反应后过滤、洗涤、干燥, 所得淡黄色固体质量为 0.94 g。
②另取 25 mL 溶液,向其中加入过量的 KI 溶液,再用 0.400mol·L-1Na2S2O3 标准溶液滴定至终点,消耗 25.00 mL。已知反应过程中的方程式如下:2Cu2++4I﹣=2CuI↓+I2、2S2O32-+I2=2I﹣+S4O62﹣。请确定该绿色粉末的化学式_________(需要计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出用键线式表示的有机物的分子式![]() 分子式:______。
分子式:______。
(2)![]() 分子中最多有 ___________个原子共直线;最多有___________个原子共平面。
分子中最多有 ___________个原子共直线;最多有___________个原子共平面。
(3)烯烃A是2-丁烯的一种同分异构体,它在催化剂作用下与氢气反应的产物不是正丁烷,则A的结构简式为___________; A与溴的四氯化碳溶液反应的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组通过下列装置探究![]() 与
与![]() 能否反应产生
能否反应产生![]() 。
。
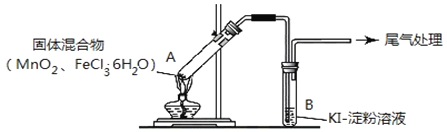
实验操作和现象如下表:
实验编号 | 操作 | 现象 |
实验1 | 按如图所示加热 |
|
实验2 | 把A中的混合物换为 B中溶液换为KSCN溶液,加热。 | A中部分固体溶解,产生白雾和黄色气体,B中KSCN溶液变红 |
回答下列问题:
![]() 实验1和实验2产生白雾的原因是__________________________________________。
实验1和实验2产生白雾的原因是__________________________________________。
![]() 实验2说明黄色气体中含有___________
实验2说明黄色气体中含有___________![]() 填化学式
填化学式![]() 则实验1中
则实验1中![]() 的现象也可能是发生了另一个离子反应,则其离子方程式为_________________________________________。
的现象也可能是发生了另一个离子反应,则其离子方程式为_________________________________________。
![]() 为进一步确认黄色气体中含有
为进一步确认黄色气体中含有![]() ,该学习小组对实验1提出两种改进方案:
,该学习小组对实验1提出两种改进方案:
方案1:在A、B间增加盛有某种试剂的洗气瓶C,结果B中溶液仍变为蓝色。
方案2:将B中淀粉KI溶液替换为NaBr溶液,结果B中溶液呈橙红色,且未检出![]() 。
。
则方案1中C中盛放的试剂是______;方案2中检验![]() 的试剂名称是______,选择NaBr溶液的依据是______________________________________________________。
的试剂名称是______,选择NaBr溶液的依据是______________________________________________________。
![]() 实验1充分加热后,若反应中被氧化与未被氧化的氯元素质量之比为1:2,则A中发生反应的化学方程式为_________________________________________,用离子方程式表示尾气处理的方式___________________________________。
实验1充分加热后,若反应中被氧化与未被氧化的氯元素质量之比为1:2,则A中发生反应的化学方程式为_________________________________________,用离子方程式表示尾气处理的方式___________________________________。
![]() 该学习小组认为实验1中溶液变蓝,可能还有另外一种原因是____________________。请你设计实验方案验证此猜想___________________________________________________________________________________________________________________________________________________。
该学习小组认为实验1中溶液变蓝,可能还有另外一种原因是____________________。请你设计实验方案验证此猜想___________________________________________________________________________________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com