
| A、醋酸铵和盐酸反应 CH3COONH4+H+═CH3COOH+NH4+ |
| B、氢氧化钡溶液和硫酸铜溶液反应 Ba2++SO42-═BaSO4↓ |
| C、钠与水反应 Na+2H2O═Na++OH-+H2↑ |
| D、碳酸氢钠溶液与NaOH溶液反应:HCO3-+OH-=CO32-+H2O |


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
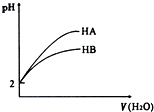 pH=2的两酸HA、HB加水稀释后,溶液pH随加水量的变化曲线如图所示.则下列叙述正确的是( )
pH=2的两酸HA、HB加水稀释后,溶液pH随加水量的变化曲线如图所示.则下列叙述正确的是( )| A、电离平衡常数HA>HB |
| B、等体积的HA和HB与等浓度的NaOH反应,HA消耗的NaOH多 |
| C、等体积的HA和HB与等质量的Zn反应,HA反应速率大 |
| D、另取0.1mol/L上面两酸HA、HB加水稀释100倍后,则酸性HB>HA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Br2+2Fe2+=2Fe3++2Br- |
| B、2Fe3++2I-=2Fe2++I2 |
| C、I2+2Fe2+=2Fe3++2I- |
| D、2Fe3++2Cl-=2Fe2++Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100 mL该溶液中含0.8 g NaOH |
| B、200 mL该溶液与100 mL 0.2 mol?L-1的硫酸溶液反应形成中性溶液 |
| C、100 mL该溶液中约含0.02×6.02×1023个Na+ |
| D、配制含1 L水的该溶液,需NaOH的质量为8 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铍的金属性比钠弱 |
| B、氯化铍的氧化性比氯化锂强 |
| C、氢氧化铍的碱性比氢氧化钙的强 |
| D、单质铍易跟冷水反应产生H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X是金属元素 |
| B、X的钠盐的化学式为:Na2X |
| C、X的最高价氧化物的化学式为:XO3 |
| D、X的最高价氧化物的水化物为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、SO32-、S2-、K+ |
| B、Na+、K+、S2-、SO42- |
| C、HSO3-、Cl-、OH-、Ba2+ |
| D、Cu2+、Cl-、OH-、K+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com