
| A、100 mL该溶液中含0.8 g NaOH |
| B、200 mL该溶液与100 mL 0.2 mol?L-1的硫酸溶液反应形成中性溶液 |
| C、100 mL该溶液中约含0.02×6.02×1023个Na+ |
| D、配制含1 L水的该溶液,需NaOH的质量为8 g |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
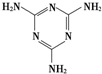 (双项)三聚氰胺(结构式如图所示)是一种重要的化工原料,可用于阻燃剂、水泥减水剂和高分子合成等领域.一些不法分子却往牛奶中加入三聚氰胺,以提高奶制品的含氮量.下列说法正确的是( )
(双项)三聚氰胺(结构式如图所示)是一种重要的化工原料,可用于阻燃剂、水泥减水剂和高分子合成等领域.一些不法分子却往牛奶中加入三聚氰胺,以提高奶制品的含氮量.下列说法正确的是( )| A、三聚氰胺不属于蛋白质 |
| B、三聚氰胺是高分子化合物 |
| C、三聚氰胺分子中含有碳碳双键 |
| D、三聚氰胺的分子式为C3H6N6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同主族金属元素的原子半径越大熔点越高 |
| B、稀有气体原子序数越大沸点越低 |
| C、分子间作用力越弱的分子其沸点越低 |
| D、同周期元素的原子半径越小越易失去电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸铵和盐酸反应 CH3COONH4+H+═CH3COOH+NH4+ |
| B、氢氧化钡溶液和硫酸铜溶液反应 Ba2++SO42-═BaSO4↓ |
| C、钠与水反应 Na+2H2O═Na++OH-+H2↑ |
| D、碳酸氢钠溶液与NaOH溶液反应:HCO3-+OH-=CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含H+的溶液显酸性,含OH-的溶液显碱性 |
| B、用丁达尔现象实验可区分葡萄糖溶液和氢氧化铁胶体 |
| C、某饱和溶液变成不饱和溶液,溶质的质量分数一定减小 |
| D、向含有BaCl2和NaOH的混合液中通入足量的二氧化硫,最终会有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下将铝和铜用导线连接组成原电池放入到氢氧化钠溶液中 |
| B、常温下将铝和铜用导线连接组成原电池放入到稀盐酸溶液中 |
| C、与氯气反应时,铝失去3个电子,而铜失去2个电子 |
| D、Al(OH)3有两性而Cu(OH)2只有弱碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、前者多 | B、后者多 |
| C、一样多 | D、无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com