
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。
(1)现有一种无色的鲜花营养液,可能由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几种物质组成,为探究其成分,某同学设计并完成了如下图所示的实验。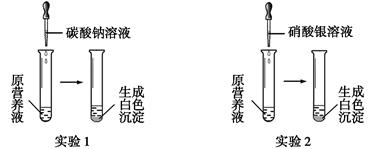
根据以上实验,请你填空。
①由实验1可确定原营养液中一定没有的物质是 (填化学式),写出生成白色沉淀的离子方程式是 。
②若测得原营养液中K+、Cl-的数目之比为2∶1,则原营养液是由 种溶质配制成的。
③某同学用氯化钙、硝酸钾、氯化钾配成的营养液中K+、Cl-、NO3-的数目之比为2∶5∶1,
则所用硝酸钾和氯化钙的物质的量之比是 。
(2)下表是500mL某“鲜花保鲜剂”中含有的成分,阅读后回答下列问题。
| 成分 | 质量(g) | 摩尔质量(g ·mol-1) |
| 蔗糖 | 68.4 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
(1)①碳酸钾; Ca2++CO32-=CaCO3↓ ②3 ③1:2
(2)①0.4 mol?L-1 ②500ml容量瓶、胶头滴管 ③AC
解析试题分析:(1)①向营养液中加入碳酸钠溶液产生白色沉淀,说明营养液中含有硝酸钙,不能含有碳酸钾。它们会发生离子反应。生成白色沉淀的离子方程式是Ca2++CO32-=CaCO3↓。②由于原营养液中K+、Cl-的数目之比为2∶1,不含碳酸钾,KCl中二者的比是1:1,原物质含有钾不含氯的物质只可能是硝酸钾。故原营养液是由有硝酸钙、硝酸钾、氯化钾三种物质配制而成。③由氯化钙、硝酸钾、氯化钾配成的营养液中,K+、Cl-、NO3-的数目之比为2∶5∶1,假设n(NO3-)=1mol,则n(KNO3)="1" mol,,n(KCl)=1mol,n(CaCl2)=2mol。所以n(KNO3): n(CaCl2)=1:2。(2)①C(蔗糖)=(68.4g∕342g·mol-1)∕0.5L="0.4" mol?L-1.准确配制500ml一定浓度的溶液需500ml要容量瓶及胶头滴管。③在溶液配制过程中A.定容时仰视容量瓶刻度线,加水过多,浓度偏低,正确。B.容量瓶在使用前未干燥,里面有少量蒸馏水,后来加入的水就少些,但最终量没变,所以浓度没变化。错误。。所以C.在移液时,液体不小心从外壁流出,会导致溶质减少。浓度偏低。正确。D.溶液的特性是均一性、稳定性。若定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理。不会产生任何影响。错误。故导致浓度偏小的是AC。
考点:考查离子反应一定体积、一定物质的量浓度的溶液的配制时应该注意的问题和误差分析等的知识。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:高中化学 来源: 题型:填空题
实验室配制500 mL 0.2 mol·L-1的Na2SO4溶液,实验操作步骤有:
A.在天平上称出14.2 g硫酸钠固体,把它放在烧杯中,用适量的蒸馏水使它完全溶解并冷却 至室温。
B.把制得的溶液小心地转移到容量瓶中。
C.继续向容量瓶中加蒸馏水至液面距刻度线1~2 cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低处与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。
E.将容量瓶瓶塞塞紧,充分摇匀后装瓶。
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)____ _。
(2)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒,还缺少的仪器是________、________。
(3)下列情况会使所配溶液浓度偏高的是(填序号)______ __。
A.容量瓶使用前内壁沾有水珠 B.没进行上述的操作步骤D
C.加蒸馏水时,不慎超过了刻度线 D.砝码上沾有杂质
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
黄铁矿主要成分是FeS2。某硫酸厂在进行黄铁矿成分测定时,取0.1000 g样品在空气中充分灼烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL 。
已知:SO2 + 2Fe3+ + 2H2O→SO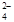 + 2Fe2+ + 4H+
+ 2Fe2+ + 4H+
Cr2O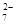 + 6 Fe2+ + 14 H+ →2 Cr3+ + 6 Fe3+ + 7 H2O
+ 6 Fe2+ + 14 H+ →2 Cr3+ + 6 Fe3+ + 7 H2O
(1)样品中FeS2的质量分数是(假设杂质不参加反应) 。
(2)若灼烧6 g FeS2产生的SO2全部转化为SO3气体时放出9.83 kJ热量,产生的SO3与水全部化合生成H2SO4,放出13.03kJ热量,写出SO3气体转化为H2SO4的热化学方程式: 。
(3)煅烧10 t上述黄铁矿,理论上产生SO2的体积(标准状况)为 ,制得98%的硫酸质量为 t ,SO2全部转化为H2SO4时放出的热量是 kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
0.5mol H2SO4的质量是________g,含______________个分子,含________mol氧原子,能和________mol NaOH完全反应,该硫酸所含氢元素的质量与________g中所含氢元素的质量相同。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某课题组进行实验研究时,欲配制浓度均为1.0mol?L-1 的Ba(OH)2和H2SO4溶液。
Ⅰ.该组同学在配制Ba(OH)2溶液时,只找到在空气中暴露已久的Ba(OH)2·8H2O试剂(相对分子质量:315),发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。
(1)用化学方程式解释未溶物产生的原因
(2)某同学查得Ba(OH)2·8H2O在283K、293K和303K时的溶解度(g/100g H2O)分别为2.5、3.9和5.6。据此认为即便使用纯净的Ba(OH)2·8H2O,在室温下也不能配得1.0 mol?L-1Ba(OH)2溶液,其理由是:
Ⅱ.用18 mol?L-1的浓硫酸配制450 mL 1.0 mol?L-1稀硫酸。
(3)实验时,需量取浓硫酸的体积为 mL,需用的主要仪器有量筒、烧杯、玻璃棒、 、
(4)配制溶液时,定容的操作方法是:
(5)实验中下列情况会使所配溶液浓度偏高的是
| A.洗涤量取浓硫酸的量筒2~3次,并将洗涤液转入容量瓶中 |
| B.定容时仰视刻度线 |
| C.振荡摇匀后再重新加水至刻度线 |
| D.用水洗涤容量瓶未干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分)按要求填空:
(1)以下物质:①NH3 ②CaCO3 ③酒精 ④饱和食盐水 ⑤Cu ⑥KOH ⑦HCl属于电解质的有 (填编号);
(2)14.7gH2SO4分子所含氢原子数与 L (标准状况下)NH3所含氢原子数相等;
(3)固体NaCl(I2)(括号内的物质为杂质),除去杂质的方法为 。
(4)要除去某食盐晶体中的CaCl2、MgCl2、Na2SO4等杂质,有以下操作:
| A.蒸发结晶 | B.过滤 | C.加入过量的Na2CO3溶液 | D.加水溶解 E、加入过量的烧碱溶液 F、加入过量稀盐酸 G、加入过量的Ba(NO3)2溶液 H、加入过量的稀硝酸 I、加入过量的BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
标准状况下,1体积水中能溶解500体积的HCl气体。若向1 L水中通入标准状况下的448LHCl气体,假设气体完全溶解。
(1)若所得溶液密度为1.2 g/cm3,则溶液中含HCl物质的量浓度为 ;
(2)从该溶液中取出10mL浓盐酸溶解于水配制成500mL溶液,配制后的稀溶液中含HCl物质的量浓度为 。
(3)在用浓盐酸配制上述稀盐酸时,所用仪器中,使用前必须检查是否漏液的仪器有 ;配制过程中,造成浓度偏低的操作可能有_______________(选填下列操作的序号)。
| A.容量瓶蒸馏水洗后未加干燥 |
| B.量筒用蒸馏水洗后未干燥 |
| C.将烧杯中浓盐酸移入容量瓶后,未用水洗涤烧杯,即向容量中加水到刻度 |
| D.用胶头滴管向容量瓶中加水时,不慎超过刻度线,用另外胶头滴管从瓶中吸出部分溶液使剩余溶液刚巧达刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
常温下,将20.0g质量分数为14.0%的KNO3溶液跟30.0g质量分数为24.0%的KNO3溶液混合,得到密度为1.15g·cm-3的混合溶液。计算:
(1)混合后溶液的质量分数。
(2)混合后溶液的物质的量浓度。
(3)在1 000g水中需溶解多少摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
实验室中用锌和稀硫酸反应制取氢气。
(1)要制取3.36L(标准状况)气体,需要1 mol/L H2SO4多少毫升?
(2)某同学用向下排空气法收集氢气,测得所收集气体密度是纯氢气密度的1.2倍。求该气体中氢气所占的体积分数(设空气的平均相对分子质量为29)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com