
(1)下列实验操作或对实验事实的描述不正确的是 (填序号)。
A.不宜用瓷坩埚灼烧氢氧化钠或碳酸钠
B.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏大
C.分液操作时,由于分液漏斗下端已沾满下层液体,故上层液体要从上口倒出
D.用托盘天平称量11.74g氯化钠晶体
E.用结晶法分离硝酸钾和氯化钠的混合物
(2)实验室需要0.1 mol·L-1NaOH溶液450 moL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
①如图所示的仪器中配制溶液肯定不需要的是 (填序号);配制上述溶液还需用到的玻璃仪器是 (填仪器名称)。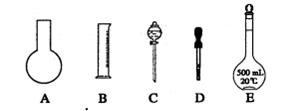
②下列操作中,容量瓶所不具备的功能有 (填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
③请计算需用托盘天平称取固体NaOH的质量为 g。某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,烧杯的实际质量为 g。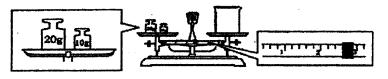
④根据计算得知,所需质量分数为98%、密度为I.84 g·cm-3的浓硫酸的体积为 mL(计算结果保留一位小数)。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是 。
(1)D (2)①A C; 烧杯、玻璃棒 ②B C E ③ 2.0;27.4
④13.6; 将浓硫酸沿烧杯内壁缓缓注入水中,并用玻璃棒不断搅拌。
解析试题分析:(1)瓷坩埚含有二氧化硅,能与碱性物质反应,故A项正确;定容时俯视溶液的体积偏小,使浓度偏大,B项正确;为了彻底分离互不混溶的液体,当下层液体流尽时,立即关闭旋塞,然后再从漏斗上口把上层液体倾倒出来,C项正确;托盘天平的读数为小数点后一位,D项错误;硝酸钾的溶解度随温度变化大,氯化钠溶解度随温度变化小,可用结晶法分离。
(2)①配制溶液不用烧瓶和分液漏斗,要用烧杯和玻璃杯;
②容量瓶不能贮存溶液,也不能用来加热,另外容量瓶只有一条刻度线,不能测量规格以下的液体的体积;
③根据容量瓶的规格,需配制500ml溶液,m(NaOH)=0.5L×0.1mol/L×40g/mol=2g;图中所示,物质和砝码位置放反了,烧杯的质量为30g-2.6g=27.4g;
④0.5L×0.5mol?L?1=V×1.84g?cm?3×98%,可得V=13.6ml。
考点:本题考察化学实验基本操作和化学计算。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:单选题
某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( )
| A.甲装置:可用来证明碳的非金属性比硅强 |
| B.乙装置:橡皮管的作用是能使水顺利流下 |
| C.丙装置:用图示的方法不能检查此装置的气密性 |
| D.丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
碳酸钙常用作牙膏的摩擦剂.某同学设计了一种制备碳酸钙的方案,其流程图如下:(所用石灰石含有杂质SiO2)
回答下列问题:
(1)充分煅烧110吨石灰石得到固体66吨.标准状况下生成二氧化碳的体积为 L,石灰石中碳酸钙的质量分数为 %.
(2)假设第①步反应完全进行,则第②步反应过滤后得到的不溶性滤渣的成分为 .
(3)第③步反应一般不采用通入CO2的主要原因是 ,相应的离子方程式为 .
(4)CaCO3是一种难溶液物质,25℃时其KSP=2.8×10-9.现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2.0×10-4mol/L,则生成沉淀所需CaCl2溶液的物质的量浓度最小是 .
(5)某学生用石灰石为原料,设计了另一种制备碳酸钙的实验方案,其流程图如下:
与前一方案相比较,该方案的优点是 .
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关实验装置进行的相应实验,能达到实验目的的是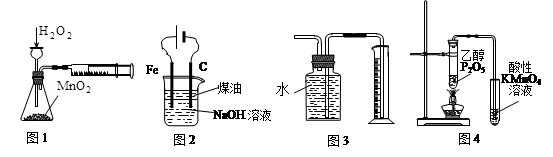
| A.图1定量测定H2O2的分解速率 |
| B.图2装置制备Fe(OH)2并能较长时间观察其颜色 |
| C.图3装置测量Cu与浓硝酸反应产生气体的体积 |
| D.图4证明CH3CH2OH发生消去反应生成了乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
“封管试验”具有简易、方便、节约、绿色等优点。观察下列四个“封管试验”(夹持装置未画出),判断下列说法正确的是
| A.加热时,a上部聚集了固体NH4Cl,说明NH4C1的热稳性比较好 |
| B.加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色的固体 |
| C.加热时,c中溶液红色变深,冷却后又变浅 |
| D.水浴时,d内气体颜色变浅,e内气体颜色加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
铬铁矿主要成分为FeO·Cr2O3,还含有杂质Al2O3。一般铬铁矿中Cr2O3质量分数约为40%。由铬铁矿制备重铬酸钾的方法如下:
已知:
①4FeO·Cr2O3+8Na2CO3+7O2 8Na2CrO4+2 Fe2O3+8CO2↑;
8Na2CrO4+2 Fe2O3+8CO2↑;
②Na2CO3+Al2O3 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
③ Cr2O72-+H2O  2CrO42-+2H+
2CrO42-+2H+
根据题意回答下列问题:
(1)操作I为 ,固体X中主要含有 (填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用 (填写仪器或试剂名称)。
(2)酸化步骤用醋酸调节溶液pH<5,其目的是 。
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、 、过滤、 、干燥。
(4)固体Y中主要含有氢氧化铝,请写出调节溶液的pH=7~8时生成氢氧化铝的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com