
【题目】下列热化学方程式,正确的是( )
A.4g固体硫完全燃烧生成SO2,放出37 kJ热量:S(s)+O2(g)=SO2(g) ΔH= -296kJ/mol
B.1molN2与3molH2在某密闭容器中反应放出73kJ热量,则反应的热化学方程式为:
N2(g)+3H2(g)![]() 2NH3(g) △H= -73kJ/mol
2NH3(g) △H= -73kJ/mol
C.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g) ==CO2(g)+ 2H2O(g) ΔH=-890.3kJ·mol-1
D.强酸强碱的中和热为- 57.3 kJ/mol:
Ba(OH) 2(aq)+H2SO4(aq)=BaSO4(S)+2H2O(l) ΔH=-114.6kJ/mol
【答案】A
【解析】4g固体硫完全燃烧生成SO2,放出37 kJ热量,1mol固体硫完全燃烧生成SO2,放出37 ×8kJ热量:S(s)+O2(g)=SO2(g) ΔH= -296kJ/mol,故A项正确;1molN2与3molH2在某密闭容器中反应放出73kJ热量,因为反应是可逆的,不能进行到底,故反应的热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H<-73kJ/mol,B项错误;甲烷的标准燃烧热为
2NH3(g) △H<-73kJ/mol,B项错误;甲烷的标准燃烧热为
-890.3kJ·mol-1,H2O为液态,故甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g) ==CO2(g)+ 2H2O(l) ΔH=-890.3kJ·mol-1,C项错误;强酸强碱的中和热为- 57.3 kJ/mol,而
Ba(OH) 2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l)有BaSO4(s)生成,故ΔH<-114.6 kJ/mol,D项错误;


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】己烯雌酚是一种激素类药物,结构如图所示,下列有关叙述中正确的是( ) 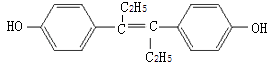
A.该有机物属于芳香烃
B.该物质不能使酸性高锰酸钾溶液褪色
C.该分子对称性好,所以没有顺反异构
D.该有机物分子中,最多可能有18个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组在指定溶液中能大量共存的是( )
A.强酸溶液中:K+、Fe2+、MnO4﹣、SO42﹣
B.![]() =0.1mol/L的溶液:Na+、K+、SiO32﹣、NO3﹣
=0.1mol/L的溶液:Na+、K+、SiO32﹣、NO3﹣
C.既能溶解Al(OH)3又能溶解 H2SiO3的溶液中:Na +、CO32﹣、SO32﹣、NO3﹣
D.在含有大量HCO3﹣的溶液中:K+、Na+、AlO2﹣、Br﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:
物质 | 活性炭 | NO | E | F |
初始 | 3.000 | 0.10 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
(1)写出NO与活性炭反应的化学方程式;
(2)计算上述反应T1℃时的平衡常数K1=;
(3)上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为;
(4)如图为在T1℃达到平衡后在t2、t3、t4、t5时改变某一个反应条件,平衡体系中反应速率随时间变化的情况,且所改变的条件均不同.已知t3﹣t4阶段为使用催化剂.请判断该反应△H0(填“>”或“<”). 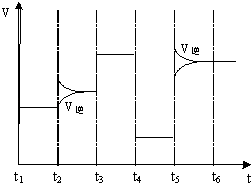
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验,能成功的是
A.苯和溴水、铁屑混合制溴苯
B.用溴水除乙烷中混有的乙烯
C.苯与浓硝酸和浓硫酸的混合物共热至70℃~80℃制硝基苯
D.用酒精和浓盐酸通过加热来制取乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下2L密闭容器中,3种气体加入起始状态和平衡状态时的物质的量(n)如下表所示:
X | Y | W | |
起始状态(mol) | 2 | 1 | 0 |
平衡状态(mol) | 1 | 0.5 | 1.5 |
下列有关说法正确的是( )
A.该温度下,该反应的平衡常数K=9
B.升高温度,若W的体积分数减小,此反应△H>0
C.该温度下,该反应的方程式为 2X(g)+Y(g)3W(g)
D.增大压强,正、逆反应速率都增大,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,
(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:; 
(2)若已知下列数据:
化学键 | H﹣H | N≡N |
键能/kJmol﹣1 | 435 | 943 |
试根据表中及图中数据计算N﹣H的键能kJmol﹣1
(3)合成氨反应通常用铁触媒作催化剂.使用铁触媒后E1和E2的变化是:E1 , E2(填“增大”、“减小、”“不变”).
(4)用NH3催化还原NOX还可以消除氮氧化物的污染.例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=akJ/mol
N2(g)+O2(g)=2NO(g);△H2=bkJ/mol
若1mol NH3还原NO至N2 , 则该反应过程中的反应热△H3=kJ/mol(用含a、b的式子表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com