
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见如图,电池总反应可表示为2H2+O2===2H2O,下列有关说法正确的是( )

A.电子通过外电路从b极流向a极
B.b极上的电极反应式为O2+2H2O+4e-===4OH-
C.每转移0.1 mol电子,便消耗1.12 L的H2
D.H+由a极通过固体酸电解质传递到b极
【答案】D
【解析】根据电池总反应:2H2+O2=2H2O可知:通入氢气的一极为电池的负极,发生氧化还原反应,反应为H2﹣2e﹣═2H+,通入氧气的一极为电池的正极,发生氧化反应,反应为O2+4e﹣+4H+=2H2O;电池工作时,电子通过外电路从负极流向正极,即从a极流向b极,电解质中阳离子向正极移动,即H+由a极通过固体酸电解质传递到b极;每转移0.1mol电子,消耗0.05mol的H2,生成0.05mol水,A.a为负极,b是正极,则电子应该是通过外电路由a极流向b,故A错误;B.该电池为酸性电池,所以正极电极反应为O2+4e﹣+4H+=2H2O,故B错误.C.每转移0.1mol电子,消耗0.05mol的H2,但气体存在的条件未知,体积不一定为1.12 L,故C错误;D.原电池中,阳离子向正极移动,所以H+由a极通过固体酸电解质传递到b极,故D正确;


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用下面所示装置制取氯酸钾、次氯酸钠和氯水并进行探究实验。

实验I.制取氮酸钾、次氯酸钠和氯水
(1)写出装置A实验室制取Cl2的化学反应方程式________________________________。
(2)制取实验结束后,取出装置B中的试管,冷却结晶、过滤、洗涤,该实验操作过程需要的玻璃仪器有胶头滴管、烧杯、_________、_________。为提高氯酸钾和次氯酸钠的产率,在实验装置中还需要改进的是_________。
(3)装置 C 中反应需要在冰水浴中进行,其原因是________________________________。
(4)装置D中的实验现象是溶液先变红后褪色,最后又变为_________色。
实验Ⅱ 尾气处理
实验小组利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(5)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中的CO2的影响)
①提出合理假设
假设1:只存在SO32- ;假设2:既不存在SO32-也不存在ClO-;假设 3:_________。
②设计实验方案,进行实验。请在答题卡上写出实验步骤以及预期现象和结论。限选实验试剂:3mol/L H2SO4、1mol/LNaOH 溶液、0.01mol/L 酸性 KMnO4 溶液、淀粉 KI 溶液。
实验步骤 | 预期现象和结论 |
步骤1:取少量吸收液分置于A、B试管中 | |
步骤2:向A试管中滴加0.01mol/L酸性 | (1)若溶液褪色,则假设1成立 |
KMnO4溶液 | (2)若溶液不褪色,则假设2或3成立 |
步骤3:_____ | _____ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,已知A元素最低化合价为-3价,它的最高价氧化物含氧56.36%,原子核内中子数比质子数多1个,试回答:

⑴写出它们的元素符号:
A________B________C________D________E_________。
⑵A、B、C、D的气态氢化物稳定性最差的是_______。
⑶A、B、C的原子半径由小到大的顺序是_________。
⑷A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ti、Fe、Cr、Mn等均为过渡元素,在生产生活中起着不可替代的重要作用,对其单质和化合物的应用研究是目前科学研究的前沿之一。请回答下列问题:
(1)Cr元素的基态原子电子排布式为_____________________,比较Fe和Mn的各级电离能后发现,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子______(填“难”或“易”)。
(2)Cu元素处于周期表____________区,向盛有硫酸铜的试管里加入氨水,首先形成蓝色沉淀,继续加入氨水,沉淀溶解,此时的离子方程式为______________,若加入乙醇将析出____________色的晶体,其配离子的离子构型为_____________
(3)某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应(巨磁电阻效应)。用A、B、O表示这类特殊晶体的化学式:_____________。
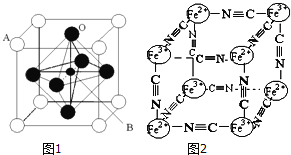
(4)有一种蓝色晶体可表示为:[KxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上,K+位于上述晶胞体心,且K+空缺率为50%(体心中没有K+的占总体心的百分比),其晶体中的阴离子晶胞结构如上图的图2所示,该晶体的化学式可表示为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①氯化钠溶液和鸡蛋清 ②氯化钠溶液中少量的硝酸钾 ③碳酸钡和氯化钡的溶液分离以上三组混合物依次采取的方法正确的是( )
A .渗析、结晶、过滤 B.渗析、蒸馏、过滤
C .蒸馏、萃取、分液 D.分液、过滤、加热升华
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2015天津]下列有关“化学与生活”的叙述不正确的是
A.点燃爆竹后,硫燃烧生成SO3
B.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
C.服用阿司匹林出现水杨酸反应时,用NaHCO3溶液解毒
D.使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃分子的球棍模型,据此回答下列问题:

(1)书写结构简式:C____________F_____________
(2)能够发生加成反应的烃有________(填数字)种。
(3)一卤代物种类最多的是________(填对应字母)。
(4)等质量的上述六种烃,完全燃烧时消耗O2最多的是________(填对应字母)。等物质的量的上述六种烃,完全燃烧时消耗O2最多的是________(填对应字母)。
(5)在120 ℃,1.01×105 Pa下与足量O2混合点燃,完全燃烧后气体体积没有变化的烃是________(填对应字母)。
(6)常温下含碳量最高的烃是________(填对应字母)。
(7)写出F发生溴代反应的化学方程式_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物阿司匹林可由水杨酸制得,它们的结构如图所示。有关说法正确的是( )

A. 1 mol阿司匹林最多可消耗3 molH2
B. 水杨酸分子中所有原子不可能共面
C. 水杨酸可以发生取代、加成、氧化、加聚反应
D. 1 mol阿司匹林最多可消耗2 molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性溶液中能大量共存的无色透明离子组是( )
A.K+、Na+、NO3-、MnO4- B.K+、Na+、Cl-、SO42-
C.K+、Na+、Br-、Cu2+ D.Na+、Ba2+、OH-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com