
【题目】“纳米材料”是当今材料科学研究的前沿,1纳米(nm)=10﹣9m,其研究成果广泛应用于催化及军事科学中,“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料,如将“纳米材料”分散到液体分散剂中,所得混合物可能具有的性质是( )
A.有丁达尔效应
B.能全部透过半透膜
C.不能透过滤纸
D.所得分散系不稳定
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】用质量分数98%、密度为1.84g·cm-3的浓硫酸配制480mL0.92mol·L-1的稀硫酸
(1)配制时,除量筒、烧杯、玻璃棒外还需玻璃仪器有________、________。
(2)减小误差量取时需选用合适的量筒量取____________mL浓硫酸
(3)在容量瓶的使用方法中,下列操作不正确的是________。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2cm处,改用胶头滴管加蒸馏水到标线
D.往容量瓶中转移溶液时应用玻璃棒引流
(4)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是__________。
①转移溶液时不慎有少量洒到容量瓶外面 ②没有洗涤烧杯和玻璃棒③定容时俯视刻度线④容量瓶不干燥,含有少量蒸馏水⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。⑥未冷却到室温就将溶液转移到容量瓶并定容
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组查阅资料得知工业上常采用蒽醌法生产 H2O2,其原理与流程如图所示:
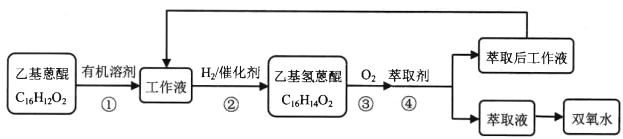
下列说法不正确的是
A. 蒽醌法制备 H2O2理论上消耗的原料是H2、O2,乙基蒽醌可循环使用
B. 步骤②为还原反应,步骤③为氧化反应
C. 步骤④中可选用 CCl4作为萃取剂
D. 应除净萃取后工作液残留的H2O2,否则释放的氧气与氢气混合易爆炸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.离子反应和氧化还原反应都是高中化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有______。(填序号)
①单质 ②化合物 ③氧化物 ④酸 ⑤碱 ⑥盐 ⑦电解质
人们常用图示法表示不同反应类型之间的关系,如化合反应和氧化还原反应的关系可用图1表示。图2为离子反应、氧化还原反应和置换反应三者之间的关系,则表示置换反应的是____(填字母),请写出符合图2阴影部分的一个离子方程式______。


图1 图2
Ⅱ.现有失去标签的四瓶无色溶液A,B,C,D,只知它们是K2CO3,K2SO4,Na HSO4和Ba(NO3)2,为鉴别它们,进行如下实验:
①A+D→溶液+气体 ②B+C→溶液+沉淀
③B+D→溶液+沉淀 ④A+B→溶液+沉淀
⑤将④得到的沉淀物加入③所得的溶液中,沉淀很快溶解并产生无色无味的气体。
根据以上实验事实,请完成如下问题:
(3)写出各物质化学式:A__________;B__________;C__________;D__________。
(4)写出实验③中反应中相关的离子方程式。____________________________。
(5)书写离子方程式
①NaHCO3溶液与H2SO4溶液混合:_________________________。
②向石灰水中通入过量二氧化碳________________________________。
③氢氧化亚铁和浓盐酸反应____________________________________。
④醋酸溶液和碳酸镁悬浊液混合生成气体并得到澄清溶液______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【加试题】某研究小组按下列路线合成某药物X(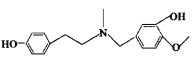 ):
):
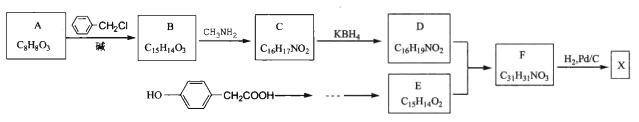
已知: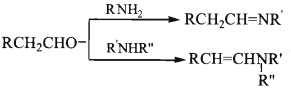
![]()
![]()
请回答:
(1)下列说法不正确的是_______。
A.化合物A能发生银镜反应
B.化合物B能与 FeCl3发生显色反应
C.化合物X的分子式为 C17H21NO3
D.化合物F含有两种含氧官能团
(2)化合物D的 结构简式是_________。
(3)写出 B→C的化学方程式______________。
(4)利用题中有关信息及物质,设计 以![]() 为原料制备E的合成路线(用流程图表示,无 机试剂任选) _____________________。
为原料制备E的合成路线(用流程图表示,无 机试剂任选) _____________________。
(5)写出同时符合下列条件的C的所有同分异构体的结构简式_____________。
① 分子中含有两个苯环,且苯环上都只有对位取代基;
② IR谱显示存在-CONH-和![]() 结构,lH-NMR谱显示分子中有7种氢原子。
结构,lH-NMR谱显示分子中有7种氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组变化中,化学反应的反应热前者大于后者的一组是( )
①CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H1; CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H2;
②2H2(g)+O2(g)=2H2O(l)△H1; H2(g)+O2(g)=H2O(l)△H2
③t℃时,在一定条件下,将1molSO2和1molO2混合后,分别置于恒容和恒压的两个密闭容器中,达到平衡状态时放出的热量分别为Q1、Q2
④CaCO3(s)=CaO(s)+CO2(g)△H1;CaO(s)+H2O(l)=Ca(OH)2(s)△H2
A. ①③④ B. ②③ C. ①④ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄曲霉素AFTB1,其结构简式如下图所示,它是污染粮食的真菌霉素,人类的P53特殊基因在黄曲霉素的作用下会发生突变,有引发肝癌的可能性。下列说法正确的是

A. 黄曲霉素分子中所有的原子肯定均共面
B. 黄曲霉素分子中含有4个手性碳原子
C. 1mol黄曲霉素最多能与5 mol H2发生加成反应
D. 黄曲霉素可以发生取代、加成、还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用类似制乙酸乙酯的装置,用环己醇制备环己烯:
已知: 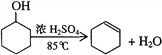
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
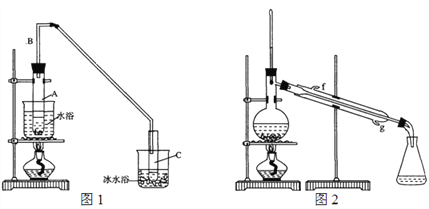
(1)制备粗品:采用如图1所示装置,用环己醇制备环己烯。
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是_____________,导管B的作用是_______________。
②试管C置于冰水浴中的目的是________________________。
(2)制备精品:
①环己烯粗品中含有环己醇和少量有机酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在______层(填“上”或“下”),分液后用________洗涤(填字母)。
A. KMnO4溶液 B. 稀H2SO4 C. Na2CO3溶液
②再将环己烯按图2装置蒸馏,冷却水从____口(填字母)进入。蒸馏时加入生石灰,目的是______________________________________。
③收集产品时,控制的温度应在______左右,实验制得的环己烯精品质量低于理论产量,可能的原因是______(填字母)。
a. 蒸馏时从70℃开始收集产品
b. 环己醇实际用量多了
c. 制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是________(填字母)。
a. 用酸性高锰酸钾溶液
b. 用金属钠
c. 测定沸点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com