
【题目】某学生用托盘天平称量食盐,将食盐放在右盘,砝码放在左盘,称得食盐的质量为15.5 g(1 g以下用游码)。该学生所称量的食盐的实际质量是( )
A. 15.5 g B. 15.0 g C. 14.5 g D. 16.0 g
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】已知B为黑色粉末,用D,E,G做焰色反应实验,隔蓝色钴玻璃观察,焰色均呈紫色,F为深红棕色液体,H能使淀粉变蓝,它们之间的相互转化关系如图1所示. 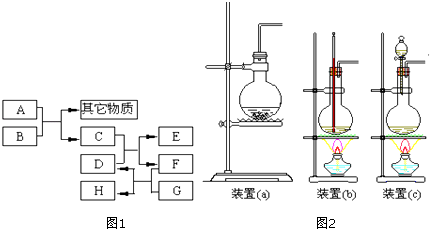
(1)请根据以上关系进行判断,指出下列物质的化学式:
A , C , D , G .
(2)写出下列反应的化学方程式:C+D:;A+B: .
在A和B的反应中,A显示出来的性质是(填写序号,多选倒扣).
①只有还原性;②还原性和酸性;③只有氧化性;④氧化性和酸性
当A和B进行反应时,应选择图2所示装置中的较为合适.
(3)C还能由以下反应制得:KClO3+6HCl=KCl+3Cl2↑+3H2O,在该反应中,被氧化的氯元素与被还原的氯元素的物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车发动机中生成NO的反应为:N2(g)+O2(g)2NO(g),t℃时,K=0.09.在t℃下甲、乙、丙三个恒容密闭容器中,投入N2(g)和 O2(g)模拟反应,起始浓度如表所示.下列判断不正确的是( )
起始浓度 | 甲 | 乙 | 丙 |
c(N2)/molL﹣1 | 0.46 | 0.46 | 0.92 |
c(O2)/molL﹣1 | 0.46 | 0.23 | 0.92 |
A.起始时,反应速率:丙>甲>乙
B.平衡时,c(NO):甲=丙>乙
C.平衡时,N2的转化率:甲>乙
D.平衡时,甲中c(N2)=0.4 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施中,不能提高化学反应速率的是
A. Zn与稀硫酸的反应中,用Zn片代替Zn粉
B. KC103的分解反应中,适当提高反应温度
C. H202的分解反应中,添加适量MnO2
D. 合成氨的反应中,增大体系的总压力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列化学方程式或离子方程式
(1)金属铝与氢氧化钠溶液反应
(2)工业用焦炭与二氧化硅制粗硅
(3)金属铝与氧化铁的铝热反应
(4)Na2O2与水反应的离子方程式
(5)氯化亚铁溶液与氯气反应的离子方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下有可逆反应:A(g)+2B(g)2C(g)+D(g).现将5mol A和10mol B加入一体积为2L的密闭容器中,反应至10min时改变某一条件,C的物质的量浓度随时间变化关系如图所示.下列有关说法正确的是( ) 
A.在0~5min内,正反应速率逐渐增大
B.反应从起始至5min时,B的转化率为50%
C.5min时的平衡常数与10min时的平衡常数不等
D.第15min时,B的体积分数为25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)0.2molO3和0.3molO2的质量(选填“相等”、“不相等”或“无法判断”),分子数之比为 , 所含原子数之比为 , 在相同条件下的体积之比为。
(2)73gHCl气体中含有个分子,标准状况下占有的体积为L。
(3)相同物质的量浓度的KCl、MgCl2、AlCl3三种溶液,分别与AgNO3溶液反应,当生成的AgCl的沉淀的质量之比为3:2:1时,三种溶液的体积比为。
(4)标准状况下VL氯化氢气体溶解在1L水中,所得溶液的密度为ρgmL,溶液中溶质的质量分数为ω,物质的量浓度为cmolL-1 , 则ω=(任写一种表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃ 时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是( ) 
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线,可得Ka(HY)≈10﹣5
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X﹣)>c(Y﹣)>c(OH﹣)>c(H+)
D.HY与HZ混合,达到平衡时:c(H+)═ ![]() +c(Z﹣)+c(OH﹣)
+c(Z﹣)+c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O![]() +O2+xOH-=Fe3O4↓+S4O
+O2+xOH-=Fe3O4↓+S4O![]() +2H2O。请回答下列问题。
+2H2O。请回答下列问题。
(1)水热法制备Fe3O4纳米颗粒的反应中,还原剂是____________。
(2)反应的化学方程式中x=________。
(3)每生成1 mol Fe3O4,反应转移的电子为________mol,被Fe2+还原的O2的物质的量为________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com