
【题目】下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是( )
A | B | C | D | |
反应 装置或 图像 |
|
|
|
|
实验现 象或图 像信息 | 反应开始 后,针筒活 塞向右移动 | 反应物总能 量大于生成 物总能量 | 反应开始后, 甲处液面低 于乙处液面 | 温度计的 水银柱不 断上升 |
A. A B. B C. C D. D
科目:高中化学 来源: 题型:
【题目】一定条件下,向含HNO3的废水中加入CH3OH进行污水处理,发生反应5CH3OH+6HNO3===3N2↑+5CO2↑+13H2O下列说法正确的是
A. CH3OH被氧化,表现氧化性
B. 此条件下还原性强弱为N2>CH3OH
C. 若氧化产物比还原产物多0.2 mol,则该反应中转移3 mol e-
D. 该反应过程中断裂的化学键既有极性键又有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融)=4Na+O2↑+2H2O;后来盖· 吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+2H2↑+4Na↑。下列有关说法正确的是( )
A.电解熔融氢氧化钠制钠,阳极发生电极反应为:Na++e-=Na
B.盖·吕萨克法制钠原理是利用铁的还原性比钠强
C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数比为2:l
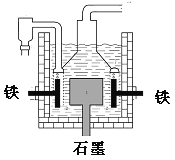
D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理利用燃料减小污染符合“绿色奥运”理念,下列关于燃料的说法正确的是( )
A. “可燃冰”是将水变为油的新型燃料
B. 氢气是具有热值高、无污染等优点的燃料
C. 乙醇是比汽油更环保、不可再生的燃料
D. 石油和煤是工厂经常使用的可再生的化石燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸(g=1.84g·cm-3)配制成浓度为0.5mol·L-1的稀硫酸500ml。
(1)选用的主要仪器有:
①________,②_________,③__________,④__________,⑤____________。
(2)请将下列各操作,按正确的序号填在横线上。
A.用量筒量取浓H2SO4 B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线 D.洗净所用仪器
E.稀释浓H2SO4 F.将溶液转入容量瓶
其操作正确的顺序依次为____________________________。
(3)简要回答下列问题:
①所需浓硫酸的体积为____________mL。
②如果实验室有15mL、20mL、50mL的量筒应选用____________mL的量筒最好,量取时发现量筒不干净用水洗净后直接量取将使浓度__________(“偏高”、“偏低”、“无影响”)
③将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并用玻璃棒不断搅拌的目的是____________,若搅拌过程中有液体溅出结果会使浓度偏____________。
④在转入容量瓶前烧杯中液体应____________,否则会使浓度偏____________;并洗涤烧杯和玻璃棒2~3次,洗涤液也要转入容量瓶,否则会使浓度____________。
⑤定容时必须使溶液凹液面与刻度线相切,若俯视会使浓度____________;仰视则使浓度____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
(1)当反应达到平衡时,N2和H2的浓度比是________;N2和H2的转化率比是________。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量__________,密度__________。(填“变大”、“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将________(填“正向”、“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将________(填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度________(填“大于”、“小于”或“等于”)原来的2倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将34.2g Al2(SO4)3 固体溶于水配成100mL溶液。
(1)写出Al2(SO4)3在水溶液中的电离方程式:__________________________________。
(2)该溶液中Al2(SO4)3的物质的量浓度为________________________。
(3)从该溶液中取出10mL,其中SO42— 的物质的量浓度为____________________。
(4)从该溶液中取出10mL,稀释到100mL,稀释后溶液中溶质Al2(SO4)3的物质的量浓度为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种物质作用,反应条件或反应物的用量改变时,对生成物没有影响的是
A. NaOH与 CO2 B. Na2O2 与CO2 C. NaOH与AlCl3 D. Na与O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式中,正确的是( )
A. 稀硫酸滴在铜片上:Cu+2H+===Cu2++H2↑
B. 稀硫酸与Ba(OH)2溶液混合:SO![]() +Ba2+===BaSO4↓
+Ba2+===BaSO4↓
C. 稀硝酸滴在大理石上:CaCO3+2H+===Ca2++H2CO3
D. 氧化铁与稀盐酸混合:Fe2O3+6H+===2Fe3++3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com