
【题目】一定条件下,向含HNO3的废水中加入CH3OH进行污水处理,发生反应5CH3OH+6HNO3===3N2↑+5CO2↑+13H2O下列说法正确的是
A. CH3OH被氧化,表现氧化性
B. 此条件下还原性强弱为N2>CH3OH
C. 若氧化产物比还原产物多0.2 mol,则该反应中转移3 mol e-
D. 该反应过程中断裂的化学键既有极性键又有非极性键
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析正确的是( )
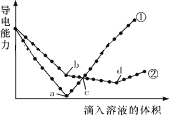
A.②代表滴加H2SO4溶液的变化曲线
B.b点溶液中大量存在的离子是SO42-、Na+、OH-
C.a、d两点对应的溶液均显中性
D.c点两溶液中含有相同量的OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为V L的某密闭容器中,a mol CO与2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)![]() CH3OH(g)。CO的转化率与温度、压强的关系如图所示:
CH3OH(g)。CO的转化率与温度、压强的关系如图所示:
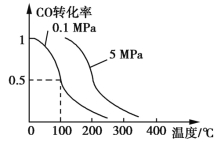
(1)该反应是 反应(填“放热”或“吸热”)。
(2)在压强为0.1 MPa条件下,200 ℃时,该反应的平衡常数K (填“=”“<”或“>”)V2/a2。
(3)在温度、容积不变的情况下,向该密闭容器再增加a mol CO(g)、2a mol H2(g)和b mol CH3OH(g),则达到新平衡时,CO的转化率 (填“增大”“减小”“不变”或“无法确定”),平衡常数 (填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】未来氢气将作为新能源的优点的是( )
①燃烧时发生氧化反应 ②充分燃烧的产物不污染环境
③氢气是一种再生能源 ④燃烧时放出大量热量
A. ①②③ B. ①②④ C. ①③④ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的叙述正确的( )
A.Fe在少量氯气中点燃可生成FeCl2B.Na在空气中加热生成淡黄色固体
C.次氯酸见光分解生成Cl2D.Cu与稀H2SO4加热可生成SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5 mol·L-1 盐酸、0.55 mol·L-1NaOH溶液,尚缺少的实验玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),原因是________________________________。
(3)他们记录的实验数据如下:已知:Q=cm(t2 -t1),反应后溶液的比热容c为4.18 kJ·℃-1·kg-1,各物质的密度均为1 g·cm-3。
①计算完成下表。(保留小数点后一位)

②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:
(4)若用KOH代替NaOH,对测定结果 (填“有”或“无”)影响;若用醋酸代替HCl做实验,测定所得的中和热的数值将 (填“变大”或“变小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解硫酸钠溶液生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1∶2,以下说法正确的是( )

A. a极与电源的负极相连
B. a电极反应式:2H2O+2e-= H2↑+2OH-
C. 离子交换膜d为阴离子交换膜
D. 产物丙为硫酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是( )
A | B | C | D | |
反应 装置或 图像 |
|
|
|
|
实验现 象或图 像信息 | 反应开始 后,针筒活 塞向右移动 | 反应物总能 量大于生成 物总能量 | 反应开始后, 甲处液面低 于乙处液面 | 温度计的 水银柱不 断上升 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com