
| c[Co(H2O)6]2+c4(Cl-) |
| c(CoCl2-) |
| c[Co(H2O)6]2+c4(Cl-) |
| c(CoCl2-) |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����ʱ����1.0mol/L NaOH��Һ�к�ijŨ��������Һʱ����pH������NaOH��Һ�������ϵ��ͼ��ʾ��ԭ������Һ�����ʵ���Ũ�Ⱥ���ȫ��Ӧ����Һ��������ǣ�������
����ʱ����1.0mol/L NaOH��Һ�к�ijŨ��������Һʱ����pH������NaOH��Һ�������ϵ��ͼ��ʾ��ԭ������Һ�����ʵ���Ũ�Ⱥ���ȫ��Ӧ����Һ��������ǣ�������| A��1 mol/L 60mL |
| B��0.5 mol/L 80mL |
| C��0.5 mol/L40mL |
| D��1 mol/L 80mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Һ�е������ӵ���Ŀ���ӣ���������ǿ |
| B������ĵ���̶�����[H+]��С |
| C���ټ���10mL pH=11 NaOH��Һ�����ҺpH=7 |
| D����Һ����ˮ�������[H+]=1��10-11mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ͭƬ���������缫�����ϡ���� |
| B����ͭƬ���������缫���������ͭ��Һ |
| C����ͭƬ����������Ƭ�������������������Һ |
| D����ͭƬ��ʯī���Ȼ�����Һ�����ߵ����ԭ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
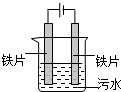 �縡ѡ���۷�������ˮ��ԭ����ͼ��ʾ�����������ɵĽ�����ʹ��ˮ�е����������۳��Ŷ���ȥ�����ʱ����Ҳ������������壮����˵����ȷ���ǣ�������
�縡ѡ���۷�������ˮ��ԭ����ͼ��ʾ�����������ɵĽ�����ʹ��ˮ�е����������۳��Ŷ���ȥ�����ʱ����Ҳ������������壮����˵����ȷ���ǣ�������| A����������Ƭ��ͭƬ������Ƭ |
| B���������������������O2 |
| C����������H+�������ƶ� |
| D������ˮ���������������ɼ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com