
| 编号 | 碘酸钾浓度/mol/L | PH | 碘酸钾损失率/% | |||
| 30℃ | 50℃ | 80℃ | 100℃ | |||
| 1 | 0.003 | 0 | 21 | 70.3 | 71 | 77.3 |
| 2 | 0.003 | 7 | 0 | 0.3 | 0.67 | 1 |
| 3 | 0.003 | 14 | 1.3 | 2.7 | 1.3 | 1 |
| 9mg |
| 127g/mol |
| 16mg |
| 127g/mol |


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| c(X) |
| c(W) |
查看答案和解析>>
科目:高中化学 来源: 题型:
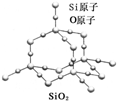
| A、晶体中Si、O原子个数比为1:2 |
| B、晶体中Si、O原子最外层都满足8电子结构 |
| C、晶体中一个硅原子含有Si-O键数目为4 |
| D、晶体中最小环上的原子数为6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸雨 | B、臭氧空洞 |
| C、光化学烟雾 | D、温室效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若管道漏气遇氨就会产生白烟 |
| B、该反应利用了Cl2的强氧化性 |
| C、NH3发生还原反应 |
| D、生成1 mol N2有6 mol电子转移 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com