
【题目】氯化氢(HCl),是无色而有刺激性气味的气体。对上呼吸道有强刺激,对眼、皮肤、黏膜有腐蚀。其水溶液俗称盐酸,学名氢氯酸。氯化氢极易溶于水,在0℃时,1体积的水大约能溶解500体积的氯化氢。实验室制取一般是用固体氯化钠和浓硫酸起反应,不加热或稍微加热,分别生成硫酸氢钠和氯化氢。 实验室可用如下装置制取氯化氢 ,化学方程式为:NaCl(s)+H2SO4=NaHSO4+HCl↑
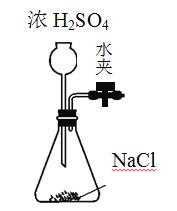
(1)如何检验该装置的气密性(请说明具体操作) _________。
(2)多余的氯化氢如何处理?画出装置图。_________。
【答案】用水夹夹住导气管的橡胶管部分,从长颈漏斗向锥形瓶中注水,将长颈漏斗下口浸没,停止加水后,长颈漏斗中的液面高于锥形瓶中的液面,且液面差保持不变; 
【解析】
(1)利用液差法检查装置气密性;(2)根据氯化氢气体有毒又极易溶于水分析。
(1)利用液差法检查此装置的气密性,具体操作如下:用水夹夹住导气管的橡胶管部分,从长颈漏斗向锥形瓶中注水,将长颈漏斗下口浸没,停止加水后,长颈漏斗中的液面高于锥形瓶中的液面,一段时间后若液面差保持不变,则气密性良好;
(2)氯化氢气体有毒,如果不处理直接排放到空气中,会污染环境,用氢氧化钠溶液吸收多余的氯化氢,由于氯化氢易溶于水,容易倒吸,因此用如图所示的一个防倒吸尾气吸收装置 。
。


科目:高中化学 来源: 题型:
【题目】传统中药“金银花”中抗菌杀毒的有效成分是“绿原酸”。某高中化学创新兴趣小组运用所学知识并参考相关文献,设计了一种“绿原酸”的合成路线如图:
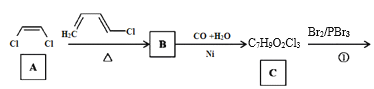
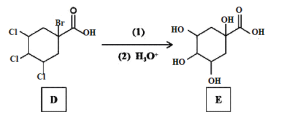
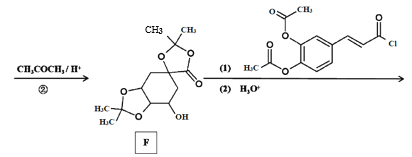
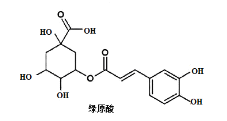
已知:① ;
;
②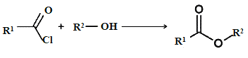 。
。
回答下列问题:
(1)有机物A的名称是___,A→B的反应类型___。
(2)C的结构简式___,有机物F中官能团的名称是___。
(3)若碳原子上连有4个不同的原子或基团时,该碳原子称为手性碳。用星号(*)标出E中的手性碳: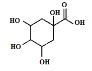 ___。
___。
(4)反应②的目的是__,写出D→E中第(1)步的反应方程式___。
(5)绿原酸在碱性条件下完全水解后,再酸化,得到的芳香族化合物的同分异构体有多种,满足以下条件的有___种(不考虑立体异构,任写一种)。
a.含有苯环
b.1mol该物质能与2molNaHCO3反应
写出核磁共振氢谱显示峰面积之比为3:2:2:1的结构简式为__。
(6)参照上述合成方法,设计由丙酸为原料制备高吸水性树脂聚丙烯酸钠的合成路线___(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯是一种食用香料,其结构简式如图,有关柠檬烯的分析正确的是
![]()
A.一定条件下,它分别可以发生加成、取代、氧化、还原等反应
B.它的分子式为C10H18
C.它的分子中所有的碳原子一定在同一平面上
D.它和丁基苯(![]() C4H9)互为同分异构体
C4H9)互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol/L的K2SO4溶液、0.2mol/L的Al2(SO4)3溶液和纯水混合,要使混合液中K+ 、Al3+、 SO42-的浓度分别为0.1mol/L、0.1mol/L、0.2mol/L,则所取三者的体积比是(假定混合后的体积不变)( )
A.1:1:1 B.2:1:2 C.1:1:2 D.2:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如图:
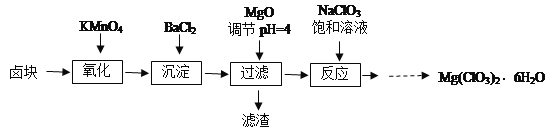
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
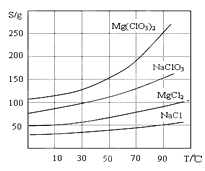
②四种化合物的溶解度(S)随温度(T )变化曲线如图所示:
(1)过滤所需要的玻璃仪器有______。
(2)如图是某学生的过滤操作示意图,其操作不规范的是______(填标号)。
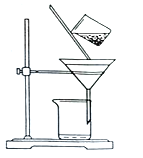
a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(3)加入BaCl2的目的是除去SO42-,如何检验SO42-已沉淀全?______
(4)加入NaClO3饱和溶液会发生如下反应:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,请利用该反应,结合图像,制取Mg(ClO3)2·6H2O的实验步骤依次为:①取样,加入NaClO3饱和溶液充分反应,②______;③______;④______;⑤过滤、洗涤,获得Mg(ClO3)2·6H2O晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则下列对该反应的推断合理的是( )

A.该反应的化学方程式为6A+2D![]() 3B+4C
3B+4C
B.0~1s内, v(A)=v(B)
C.0~5s内,B的平均反应速率为006mol·L-1·s-1
D.5s时,v(A)=v(B)=v(C)=v(D)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为铜与稀硝酸反应的有关性质实验(洗耳球:一种橡胶为材质的工具仪器,可挤压)。
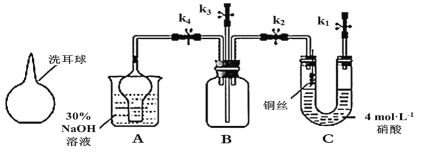
实验步骤如下:
①按照如图装置连接好仪器,关闭所有止水夹。检查装置的气密性。
②在装置A中的烧杯中加入30%的氢氧化钠溶液。在装置C的U型管中加入4.0mol·L-1的硝酸,排除U型管左端管内空气。
③塞紧连接铜丝的胶塞,打开止水夹K1,反应进行一段时间。
④进行适当的操作,使装置C中产生的气体进入装置B的广口瓶中,气体变为红棕色。气体进入烧杯中与氢氧化钠溶液反应。
回答下列问题:
(1)装置C中发生反应的离子方程式为__。反应后的溶液呈蓝色,其原因是铜离子和水分子形成了水合铜离子,1mol水合铜离子中含有σ键数目为12NA,该水合铜离子的化学式为__。
(2)装置A上面的导管口末端也可以连接__来代替干燥管,实现同样作用。
(3)加入稀硝酸,排除U型管左端管内空气的操作是__。
(4)步骤④中“使装置C中产生的气体进入装置B的广口瓶中”的操作是打开止水夹__(填写序号),并用洗耳球在U型管右端导管口挤压空气进入。
(5)步骤④中使“气体进入烧杯中与氢氧化钠溶液反应”的操作是__,尾气中主要含有NO2和空气,与NaOH溶液反应只生成一种盐,则离子方程式为有__。
(6)某同学发现,本实验结束后硝酸还有很多剩余,请你改进实验,使能达到预期实验目的,反应结束后硝酸的剩余量尽可能较少,你的改进是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4与CO2重整生成H2和CO的过程中主要发生下列反应
![]()
![]()
在恒压、反应物起始物质的量比![]() 条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是

A.升高温度、增大压强均有利于提高CH4的平衡转化率
B.曲线B表示CH4的平衡转化率随温度的变化
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800K、n(CH4):n(CO2)=1:1条件下,反应至CH4转化率达到X点的值,改变除温度外的特定条件继续反应,CH4转化率能达到Y点的值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)有以下几种物质:①碳酸氢钠晶体 ②液态氯化氢 ③铁 ④蔗糖 ⑤酒精 ⑥熔融的K2SO4 ⑦干冰 ⑧石墨。试回答(填序号):
(1)以上物质能导电的是_________________________。
(2)以上物质中属于非电解质的是_________________________。
(3)以上物质中溶于水后水溶液能导电的是_________________________。
(4)①、②在水溶液中反应的离子方程式为_________________________________。
(二)某溶液的溶质可能由下列离子组成:Cl-、![]() 、
、![]() 、H+、Ba2+、Na+,某同学进行了如下实验:
、H+、Ba2+、Na+,某同学进行了如下实验:
Ⅰ 向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤;
Ⅱ 向Ⅰ中滤液中加入AgNO3溶液,有白色沉淀产生;
Ⅲ 将Ⅰ中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生。
(5)依据以上实验可以推断,原溶液中一定含有____________ (用离子符号表示,下同);一定没有______________;可能含有________________,检验是否存在该离子的方法为_____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com