
【题目】CH4与CO2重整生成H2和CO的过程中主要发生下列反应
![]()
![]()
在恒压、反应物起始物质的量比![]() 条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是

A.升高温度、增大压强均有利于提高CH4的平衡转化率
B.曲线B表示CH4的平衡转化率随温度的变化
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800K、n(CH4):n(CO2)=1:1条件下,反应至CH4转化率达到X点的值,改变除温度外的特定条件继续反应,CH4转化率能达到Y点的值
【答案】BD
【解析】
A.甲烷和二氧化碳反应是吸热反应,升高温度,平衡向吸热反应即正向移动,甲烷转化率增大,甲烷和二氧化碳反应是体积增大的反应,增大压强,平衡逆向移动,甲烷转化率减小,故A错误;
B.根据两个反应得到总反应为CH4(g)+2CO2(g) ![]() H2(g)+3CO(g) +H2O (g),加入的CH4与CO2物质的量相等,CO2消耗量大于CH4,因此CO2的转化率大于CH4,因此曲线B表示CH4的平衡转化率随温度变化,故B正确;
H2(g)+3CO(g) +H2O (g),加入的CH4与CO2物质的量相等,CO2消耗量大于CH4,因此CO2的转化率大于CH4,因此曲线B表示CH4的平衡转化率随温度变化,故B正确;
C.使用高效催化剂,只能提高反应速率,但不能改变平衡转化率,故C错误;
D.800K时甲烷的转化率为X点,可以通过改变二氧化碳的量来提高甲烷的转化率达到Y点的值,故D正确。
综上所述,答案为BD。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】Y是一种天然除草剂,其结构如图所示,下列说法正确的是( )
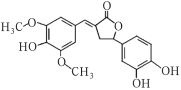
A.Y可以和Na2CO3溶液发生反应
B.Y分子中所有碳原子一定在同一平面内
C.1molY最多能与6molNaOH反应
D.Y与足量的H2发生加成反应的产物含9个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化氢(HCl),是无色而有刺激性气味的气体。对上呼吸道有强刺激,对眼、皮肤、黏膜有腐蚀。其水溶液俗称盐酸,学名氢氯酸。氯化氢极易溶于水,在0℃时,1体积的水大约能溶解500体积的氯化氢。实验室制取一般是用固体氯化钠和浓硫酸起反应,不加热或稍微加热,分别生成硫酸氢钠和氯化氢。 实验室可用如下装置制取氯化氢 ,化学方程式为:NaCl(s)+H2SO4=NaHSO4+HCl↑
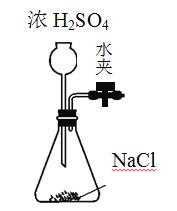
(1)如何检验该装置的气密性(请说明具体操作) _________。
(2)多余的氯化氢如何处理?画出装置图。_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现以C8H18为原料经裂解制得乙烯,进而制得1,2-二溴乙烷,根据如图所示装置,结合有关知识回答问题:
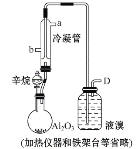
(1)制取乙烯的化学方程式为___。
(2)制取的二溴乙烷可能混有一些杂质,这些杂质可能是___。
(3)冷凝管的进出水方向为___,使用冷凝管的目的是___。
(4)设计三种简单的实验证明广口瓶内发生的是加成反应而不是取代反应。
第一种___;
第二种___;
第三种___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应方向的描述中正确的是
A.某吸热反应能自发进行,因此该反应是熵增反应
B.知道了某过程有自发性之后,可预测反应过程发生的快慢
C.CaCO3(s)![]() CaO(s)+CO2(g) △H>0,该反应能否自发进行与温度无关
CaO(s)+CO2(g) △H>0,该反应能否自发进行与温度无关
D.冰融化为水的过程中:△H<0,△S>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇酸树脂是一种成膜性好的树脂,如图是一种醇酸树脂的合成线路:

已知:![]()
![]()
![]() 反应①的化学方程式是______.
反应①的化学方程式是______.
![]() 写出B的结构简式是______.
写出B的结构简式是______.
![]() 反应①~③中属于取代反应的是______
反应①~③中属于取代反应的是______![]() 填序号
填序号![]() .
.
![]() 反应④的化学方程式为是______.
反应④的化学方程式为是______.
![]() 反应⑤的化学方程式是______.
反应⑤的化学方程式是______.
![]() 下列说法正确的是______
下列说法正确的是______![]() 填字母
填字母![]() .
.
a B存在顺反异构
b 1molE与足量的银氨溶液反应能生成2mol![]()
c F能与![]() 反应产生
反应产生![]()
d丁烷、![]() 丙醇和D中沸点最高的为丁烷
丙醇和D中沸点最高的为丁烷
![]() 写出符合下列条件的与
写出符合下列条件的与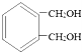 互为同分异构体的结构简式______.
互为同分异构体的结构简式______.
![]() 能与浓溴水反应生成白色沉淀
能与浓溴水反应生成白色沉淀![]() 苯环上一氯代物有两种
苯环上一氯代物有两种![]() 能发生消去反应.
能发生消去反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如下,A为一元羧酸,10.2g A与足量NaHCO3溶液反应生成2.24L CO2(标准状况),A的分子式为
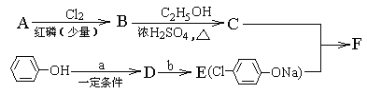
A. C2H4O2B. C3H6O2C. C4H8O2D. C5H10O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
(1)上述反应中,__元素的化合价升高,则该元素的原子__(填“得到”或“失去”)电子;而__元素的化合价降低,则该元素的原子被__(填“氧化”或“还原”)。
(2)上述反应中,若有10个铝原子参与反应,则转移的电子总数为__,用“双线桥法”表示反应中电子转移的方向和数目:___
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生以铁丝和Cl2为原料进行下列三个实验。从分类角度分析,下列说法正确的是 ( )
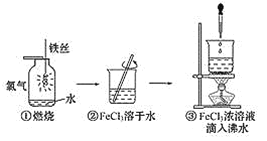
A.实验①、②所涉及的物质均为电解质
B.实验①、③发生的均为离子反应
C.实验②、③均未发生氧化还原反应
D.实验①、③反应制得的物质均为纯净物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com