
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.71gCl2溶于足量水中,Cl-的数量为NA
B.46g乙醇中含有共价键的数量为7NA
C.25℃时,1LpH=2的H2SO4溶液中含H+的总数为0.02NA
D.标准状况下,2.24LCO2与足量Na2O2反应转移的电子数为0.1NA
【答案】D
【解析】
A.Cl2与水反应是可逆反应,Cl-的数量少于NA,A错误;
B.每个乙醇分子中含8个共价键,46g乙醇的物质的量=![]() =1mol,则共价键的物质的量=1mol
=1mol,则共价键的物质的量=1mol![]() 8=8mol,所以46g乙醇所含共价键数量为8NA,B错误;
8=8mol,所以46g乙醇所含共价键数量为8NA,B错误;
C.25℃时,1LpH=2的H2SO4溶液中,C(H+)=10-2mol·L-1,n(H+)=10-2mol·L-1×1L=0.01mol,所以含H+的总数为0.01NA,C错误;
D.每1molCO2对应转移电子1mol,标准状况下,2.24L的物质的量=0.1mol,故0.1molCO2与足量Na2O2反应转移的电子数为0.1NA,D正确。
答案选D。


科目:高中化学 来源: 题型:
【题目】(1)证明溴乙烷中溴元素的存在,有下列几步,其正确的操作顺序是___。
①加入硝酸银溶液 ②加入氢氧化钠溶液 ③加热 ④加入稀硝酸至溶液呈酸性
(2)有机物M结构如图,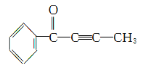 。根据M的结构回答:最多有__个原子共平面。
。根据M的结构回答:最多有__个原子共平面。
(3)某烃A和炔烃B的混合物共1L,完全燃烧生成相同状况下的二氧化碳1.4L,水蒸气1.6L,写出两种烃的结构简式A__,B___。
(4)实验室制取硝基苯的化学反应方程式是___。
(5)溴乙烷水解得到乙醇,乙醇可以发生催化氧化成醛,写出乙醇催化氧化的方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有对四种元素的叙述如下:
①元素X的基态原子的价电子排布式3s23p1
②元素Y的基态原子的原子结构示意图![]()
③元素Z的基态原子Z3-的轨道表示式![]()
④元素T的基态原子有两个电子层,电子式为![]()
则下列有关比较中正确的是( )
A.第一电离能:T>Z>X>Y
B.简单离子半径:Z>T>Y>X
C.电负性:Z>T>Y>X
D.最高正化合价:T>Z>X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)在不同条件下分解产物不同,200℃时在Cu表面分解的机理如图。已知200℃时:反应Ⅰ:3N2H4(g)=N2(g)+4NH3(g) ΔH1=-32.9 kJ·mol-1反应Ⅱ:N2H4(g)+H2(g)2NH3(g)ΔH2=-41.8 kJ·mol-1
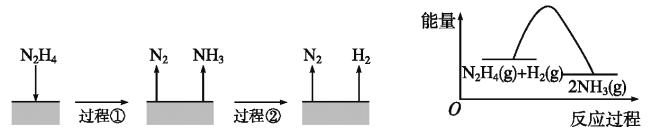
下列说法不正确的是()
A. 图所示过程①是放热反应
B. 反应Ⅱ的能量过程示意图如图所示
C. 断开3 mol N2H4(g)的化学键吸收的能量大于形成1 molN2(g)和4 mol NH3(g)的化学键释放的能量
D. 200℃时,肼分解生成氮气和氢气的热化学方程式为N2H4(g)=N2(g)+2H2(g)ΔH=+50.7 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯氧布洛芬具有良好的解热、镇痛、抗炎、抗风湿作用,苯氧布洛芬的合成路线如下:
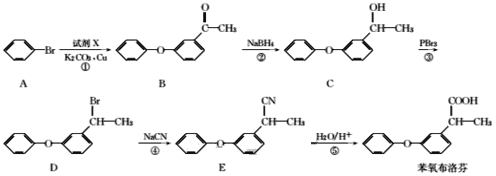
回答下列问题:
(1)苯氧布洛芬中官能团的名称为___。
(2)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。A-D四种物质中,含有手性碳的有机物为___(填字母)。
(3)反应②的反应类型是___。
(4)若过程①发生的是取代反应,且另一种产物为HBr,由A生成B发生反应的化学方程式为___。
(5)有机物M与C互为同分异构体,M满足下列条件:
I.能与FeCl3溶液发生显色反应,1molM可消耗2molNaOH;
Ⅱ.M分子中有6种不同化学环境的氢,核磁共振氢谱为3:2:2:2:2:3,且分子中含有![]() 结构。
结构。
M的结构有___种,写出其中一种结构简式:___。
(6)根据已有知识并结合相关信息,写出以丙酮(CH3COCH3)为原料制备2一甲基丙酸的合成路线流程图(无机试剂任用)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】快离子导体是一类具有优良离子导电能力的固体电解质。图1(Li3SBF4)和图2是潜在的快离子导体材料的结构示意图。回答下列问题:
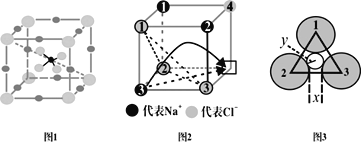
(1)S+2e-=S2-过程中,获得的电子填入基态S原子的___(填轨道符号);
(2)BF3+NH3=NH3BF3的反应过程中,形成化学键时提供电子的原子轨道符号是___;产物分子中采取sp3杂化轨道形成化学键的原子是___;
(3)基态Li+、B+分别失去一个电子时,需吸收更多能量的是___,理由是___;
(4)图1所示的晶体中,锂原子处于立方体的位置___;若其晶胞参数为apm,则晶胞密度为___g·cm-3(列出计算式即可)
(5)当图2中方格内填入Na+时,恰好构成氯化钠晶胞的![]() ,且氯化钠晶胞参数a=564pm。氯化钠晶体中,Cl-按照A1密堆方式形成空隙,Na+填充在上述空隙中。每一个空隙由___个Cl-构成,空隙的空间形状为___;
,且氯化钠晶胞参数a=564pm。氯化钠晶体中,Cl-按照A1密堆方式形成空隙,Na+填充在上述空隙中。每一个空隙由___个Cl-构成,空隙的空间形状为___;
(6)温度升高时,NaCl晶体出现缺陷(如图2所示,某一个顶点没有Na+,出现空位),晶体的导电性大大增强。该晶体导电时,在电场作用下迁移到空位上,形成电流。迁移的途径有两条(如图2中箭头所示):
途径1:在平面内挤过2、3号氯离子之间的狭缝(距离为x)迁移到空位。
途径2:挤过由1、2、3号氯离子形成的三角形通道(如图3,小圆的半径为y)迁移到空位。已知:r(Na+)=95pm,r(Cl-)=185pm,![]() =1.4,
=1.4,![]() 。
。
①x=___,y=___;(保留一位小数)
②迁移可能性更大的途径是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项叙述中,正确的是( )
A.Na、Mg、Al的未成对电子数依次增多
B.价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素
C.2p和3p轨道形状均为哑铃形,能量也相等
D.氮原子的最外层电子排布图:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积恒定的密闭容器中,进行如下可逆反应:A(s)+B(g)![]() 2C(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是( )
2C(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是( )
①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量 ④B物质的量浓度
A. ①②④ B. ②③ C. ②③④ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于![]() 的说法正确的是
的说法正确的是
A. 所有原子可能都在同一平面上 B. 最多只可能有9个碳原子在同一平面
C. 有7个碳原子可能在同一直线 D. 只可能有5个碳原子在同一直线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com