
【题目】下列各项叙述中,正确的是( )
A.Na、Mg、Al的未成对电子数依次增多
B.价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素
C.2p和3p轨道形状均为哑铃形,能量也相等
D.氮原子的最外层电子排布图:![]()
科目:高中化学 来源: 题型:
【题目】在容积为1.0L的恒容密闭容器中进行可逆反应:![]() 。判断该可逆反应达到平衡状态的依据有( )
。判断该可逆反应达到平衡状态的依据有( )
A.单位时间内消耗X和Y的物质的量之比为1:2
B.容器内气体的压强不再随时间改变
C.容器内气体的密度不再随时间改变
D.气体Z的物质的量不再随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液氨与水相似,存在着微弱的电离:2NH3![]()
![]() +
+![]() 。-50℃时,两种离子的平衡浓度均为1×10-15mol/L,下列有关液氨的离子积及其电离平衡的叙述中错误的是
。-50℃时,两种离子的平衡浓度均为1×10-15mol/L,下列有关液氨的离子积及其电离平衡的叙述中错误的是
A.此温度下,液氨的离子积等于1×10-30
B.在液氨中放入NaNH2,则液氨的离子积数值将增大
C.此温度下,在液氨中加入NaNH2,则液氨中c(![]() )<1×10-15mol/L
)<1×10-15mol/L
D.在液氨中加入NH4Cl,则液氨中c(![]() )将大于c(
)将大于c(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲胺是农药螟铃畏的重要中间体,在一定温度压强及催化剂条件下由氨与甲醇作用而制得,反应原理为:2CH3OH(g)+NH3(g)CH3NHCH3(g)+2H2O(g)
已知:①CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) ΔH=-1560.8 kJ/mol kJ·mol-1
O2(g)=CO2(g)+2H2O(g) ΔH=-1560.8 kJ/mol kJ·mol-1
②2NH3(g)+![]() O2(g)=N2(g)+3H2O(g) ΔH=-236.0 kJ·mol-1
O2(g)=N2(g)+3H2O(g) ΔH=-236.0 kJ·mol-1
③CH3NHCH3(g)+![]() O2(g)=2CO2(g)+
O2(g)=2CO2(g)+![]() H2O(g)+
H2O(g)+![]() N2(g) ΔH=-1872.6 kJ·mol-1
N2(g) ΔH=-1872.6 kJ·mol-1
(1)写出CH3OH(g)与NH3(g)转化为CH3NHCH3(g)和H2O(g)的热化学方程式是____________。
(2)不同的催化剂对二甲胺合成催化效率不同(如图所示),则最合适的催化剂及温度是_____________
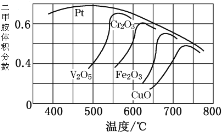
(3)一定条件下,原料气中n(CH3OH)/n(NH3)比值和温度对NH3平衡转化率影响的实验数据如图:
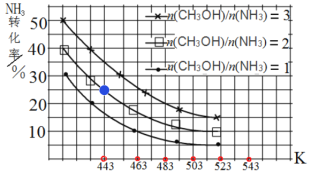
①温度为443 K时,在1 L反应容器中投入4 mol NH3和8 mol CH3OH进行反应,试计算达到平衡时CH3NHCH3(g)浓度为_________molL-1,该温度下化学平衡常数为_____________
②结合图中数据,归纳 NH3平衡转化率受外界条件影响的变化规律:a:_______b:________
(4)二甲胺水溶液类似于氨水,呈碱性;则二甲胺在水中的电离方程式为__________
(5)常温下,将二甲胺和盐酸等体积混合,两种溶液的物质的量浓度和混合溶液的pH如表所示:
实验编号 | 二甲胺浓度(mol.L-1) | 盐酸浓度(mol.L-1) | 混合后溶液的PH |
甲 | 0.1 | 0.1 | a |
乙 | 0.15 | 0.1 | 8 |
丙 | 0.2 | 0.1 | 10 |
①实验甲中,a______(填“大于”、“小于”或“等于”)7
②实验丙混合后的溶液中离子浓度大小关系为______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国芝加哥大学化学研究所近日揭示了WO3/CeO2-TiO2双催化剂在低温下催化氮的污染性气体转化为无毒气体,其过程如图所示
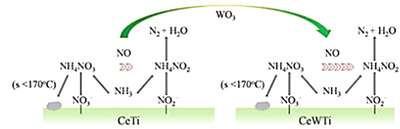
(1)Ti价电子排布式为______________,其能量最高的能层是___________。
(2)N、O、H三种原子的电负性由大到小的顺序为___________________。
(3)NO2-的空间构型为___________,与NO3-互为等电子体的分子为_______________
(4)WO3可作为苯乙烯氧化的催化剂![]() +H2O2
+H2O2![]()
![]() +H2O
+H2O
①![]() 中碳原子的杂化方式为_________。
中碳原子的杂化方式为_________。
②1molH2O2中δ键个数为____________。
③![]() 属于______________晶体。
属于______________晶体。
(5)W和Ti可形成金属互化物,某W和Ti的金属互化物如图所示,则该晶体的化学式为__________。
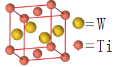
(6)金属钛的晶体堆积方式为 ____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K、Ka、KW分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是( )
A.在500 ℃、20 MPa条件下,在5 L密闭容器中进行合成氨的反应,使用催化剂后K增大
B.室温下K(HCN)<K(CH3COOH),说明CH3COOH的电离度一定比HCN的大
C.25 ℃时,pH均为4的盐酸和NH4I溶液中KW不相等
D.2SO2+O2![]() 2SO3达平衡后,改变某一条件时K不变,SO2的转化率可能增大、减小或不变
2SO3达平衡后,改变某一条件时K不变,SO2的转化率可能增大、减小或不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器内,800℃时反应2NO(g)+O2(g) ![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)800℃,反应达到平衡时,NO的物质的量浓度为__________ mol/L;升高温度,NO的浓度增大,则该反应是________(填“放热”或“吸热”)反应。
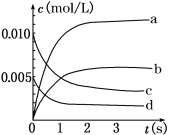
(2)如下图中表示NO2变化的曲线是________(填字母序号a、b、c、d)。用O2表示从0~2 s内该反应的平均速率v=________ mol/(L·s)。
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Cu(OH)2(s)![]() Cu2+(aq)+2OH-(aq),Ksp=c(Cu2+)·c2(OH-)=2×10-20。当溶液中各种离子的浓度幂的乘积大于溶度积时,则产生沉淀,反之固体溶解。
Cu2+(aq)+2OH-(aq),Ksp=c(Cu2+)·c2(OH-)=2×10-20。当溶液中各种离子的浓度幂的乘积大于溶度积时,则产生沉淀,反之固体溶解。
(1)某CuSO4溶液里c(Cu2+)=0.02mol·L-1,如果生成Cu(OH)2沉淀,应调整溶液的pH,使之大于________。
(2)要使0.2mol·L-1CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应aA(g)+bB(g)![]() cC(g),某温度下,在2L密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2L密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
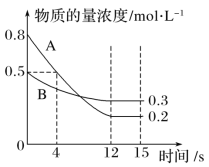
(1)从反应开始到12s时,用A表示的反应速率为___。
(2)经测定,前4s内v(C)=0.05mol·L-1·s-1,则该反应的化学方程式为___。
(3)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经相同时间后,测量三个容器中的反应速率分别为甲:v(A)=0.3mol·L-1·s-1,乙:v(B)=0.12mol·L-1·s-1,丙:v(C)=9.6mol·L-1·min-1。则甲、乙、丙三个容器中反应速率由快到慢的顺序为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com