
【题目】在2 L密闭容器内,800℃时反应2NO(g)+O2(g) ![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)800℃,反应达到平衡时,NO的物质的量浓度为__________ mol/L;升高温度,NO的浓度增大,则该反应是________(填“放热”或“吸热”)反应。
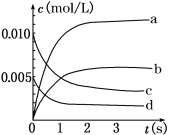
(2)如下图中表示NO2变化的曲线是________(填字母序号a、b、c、d)。用O2表示从0~2 s内该反应的平均速率v=________ mol/(L·s)。
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
【答案】0.0035 放热 b 1.5×10-3 bc c
【解析】
浓度不变说明反应达到平衡;升高温度平衡向吸热反应方向移动;依据反应物浓度减小、生成物浓度增大判断;氧气的消耗浓度是一氧化氮浓度的一半;达到平衡状态,反应体系中各种物质的浓度或含量不再发生变化、正逆反应速率相等;依据影响反应速率和化学平衡的因素判断。
(1)由表中数据可知从3s开始,NO的物质的量为0.007mol,不再变化,3s时反应达平衡,所以平衡时NO的浓度为0.007mol/2L= 0.0035 mol/L;升高温度,平衡向吸热反应方向移动,NO的浓度增大,则平衡向逆反应方向移动,所以正反应是放热反应。(2)平衡时消耗NO的是0.013mo,则生成NO2是0.013mol,其浓度是0.013mol÷2L=0.0065mol/L,所以b曲线表示NO2的变化;0~2 s内消耗NO是0.012ml,则消耗氧气是0.006mol其浓度变化是0.006mol÷2L=0.003mol/L,所以用氧气表示的反应速率是0.003mol/L÷2s=1.5×10-3mol/(L·s)。(3)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。A中反应速率的的关系是恒成立的,不能说明;根据反应的方程式可知,反应前后体积减小,所以压强也是减小的,因此选项b正确;c中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,正确;密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此d不正确,答案选bc。(4)a降低生成物的浓度,反应速率降低;升高温度平衡向逆反应方向进行,b不正确;催化剂不能改变平衡状态,d不正确;增大反应物的浓度可以加快化学反应速率,平衡向正反应方向移动,所以正确的答案选c。


科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是![]()
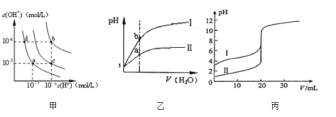
A.图甲中纯水仅升高温度,就可以从a点变到c点
B.图甲中在b点对应温度下,将pH=2的H2SO4溶液与pH=10的NaOH溶液等体积混合后,溶液显中性
C.图乙表相同温度下pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
D.图丙表示25℃时用0.100molL-1NaOH溶液分别滴定20.00ml0.100molL-1的盐酸和醋酸,V(NaOH)=20.00ml时,两份溶液中c(Cl-)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某课外活动小组设计的用化学电源使LED灯发光的装置。下列说法不正确的是( )

A.装置中存在“化学能→电能→光能”的转化
B.锌片上发生的电极反应为![]()
C.如果将稀硫酸换成柠檬汁,则导线中不会有电子流动
D.如果将锌片换成铁片,则电路中的电流方向不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项叙述中,正确的是( )
A.Na、Mg、Al的未成对电子数依次增多
B.价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素
C.2p和3p轨道形状均为哑铃形,能量也相等
D.氮原子的最外层电子排布图:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用某浓度NaOH溶液滴定一元酸HA的滴定曲线如图所示(横坐标为滴入NaOH的体积,纵坐标为所得混合液的pH;甲基橙变色范围为3.1~4.4)。下列判断正确的是
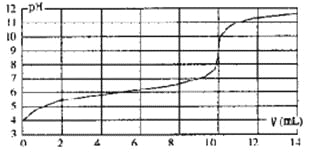
A.HA的浓度为l×10-4mol·L-1
B.实验时可选甲基橙作指示剂
C.V=10mL,酸碱恰好中和
D.pH=7时,溶液中c(Na+)>c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有些汽车安装了安全气囊,气囊中装有叠氮化钠(![]() )等固体粉末。一旦汽车发生强烈的撞击,叠氮化钠将迅速分解生成钠和氮气(
)等固体粉末。一旦汽车发生强烈的撞击,叠氮化钠将迅速分解生成钠和氮气(![]() ),使安全气囊打开,起到保护作用。此后气体通过气囊上的小孔迅速消散,气囊收缩。
),使安全气囊打开,起到保护作用。此后气体通过气囊上的小孔迅速消散,气囊收缩。
(1)写出叠氮化钠发生分解反应的化学方程式:____________________。
(2)写出安全气囊中选用叠氮化钠的理由:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.1molL-1NaOH溶液逐滴滴入10mL0.1molL-1NH4HSO4溶液中,溶液的pH与NaOH溶液体积关系如图所示:下列关系中,不正确的是
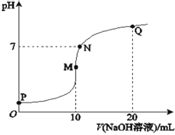
A.M点c(Na+)>c(NH4+)
B.N点c(NH4+)+c(Na+)=2c(SO42-)
C.Q点c(NH4+)+c(NH3H2O)=c(Na+)
D.M、N、Q三点中,水的电离程度M>N>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应![]() 达到平衡,正反应速率随时间变化的示意图如下所示。
达到平衡,正反应速率随时间变化的示意图如下所示。
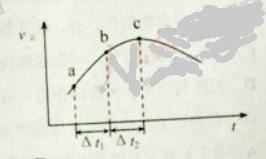
A. 反应在c 点达到平衡状态
B. 反应物浓度:![]() 点小于
点小于![]() 点
点
C. 反应物的总能量低于生成物的总能量
D. ![]() 时,SO2的转化率:
时,SO2的转化率:![]() 段小于
段小于![]() 段
段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为
A.0.01mol·L-1B.0.017mol·L-1
C.0.05mol·L-1D.0.50mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com