
【题目】短周期主族元素W、X、Y、Z,M是W的最高价氧化物对应的水化物,常温下,0.01 molL﹣1 M溶液的pH=12,X、Y、Z的单质e、f、g在通常状态下均为气态,并有如图所示的转化关系(反应条件略去)。在双原子单质分子中,f分子含共用电子对数最多,1个乙分子含10个电子。下列说法正确的是( )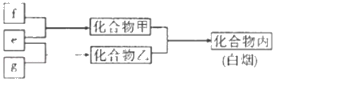
A.简单离子半径:Z>Y>W
B.X能分别与W、Y、Z组成共价化合物
C.化合物丙能抑制水电离
D.X与Y元素形成的最简单的气态氢化物是极性分子
【答案】D
【解析】
常温下,0.01 molL﹣1 M溶液的pH=12,则M为一元强碱,因为是W是短周期元素,所以M为NaOH,故W为Na;X、Y、Z的单质e、f、g在通常状态下均为气态,常见有H2、N2、O2、F2、Cl2,在双原子单质分子中,f分子含共用电子对数最多,则f为N2,故Y为N元素;甲与乙反应生成白烟,丙可能为NH4Cl也可能为NH4F,则甲为NH3、e为H2、X为H元素;由于1个乙分子含10个电子,可知乙为HF,g为F2,Z为F元素,丙为NH4F,综上所述,X为H,Y为N,Z为F,W为Na,据此分析回答。
A.W、Y、Z的简单离子分别为:Na+、N3﹣、F﹣,三者电子层结构相同,核电荷数越大离子半径越小,故离子半径:N3﹣>F﹣>Na+,A错误;
B.H元素与N元素、F元素均可组成共价化合物,但H元素与Na元素组成离子化合物,B错误;
C.丙为NH4F,铵根离子、氟离子都水解,促进水的电离,C错误;
D.X与Y元素形成的最简单的气态氢化物是NH3,NH3是极性分子,故D正确。
答案选D。


科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于I A族,W与X属于同一主族。下列说法正确的是 ( )
A.元素X、W的简单阴离子具有相同的电子层结构B.W的简单气态氢化物的热稳定性比Y的强
C.由Y、Z两种元素组成的化合物是离子化合物D.简单离子半径:r(X)<r(W)<r(Z)<r(Y)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来处理含Cr2O72-废水,如下图所示;电解过程中溶液发生反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
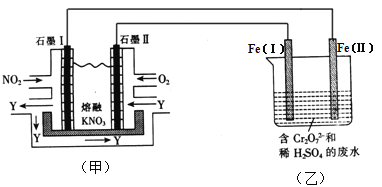
(1)甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用。则石墨Ⅱ是电池的 极;石墨Ⅰ附近发生的电极反应式为 。
(2)工作时,甲池内的NO3-离子向 极移动(填“石墨Ⅰ”或“石墨Ⅱ”);在相同条件下,消耗的O2和NO2的体积比为 。
(3)乙池中Fe(Ⅰ)棒上发生的电极反应为 。
(4)若溶液中减少了0.01 mol Cr2O72-,则电路中至少转移了 mol电子。
(5)向完全还原为Cr3+的乙池工业废水中滴加NaOH溶液,可将铬以Cr(OH)3沉淀的形式除去,已知Cr(OH)3存在以下溶解平衡:Cr(OH)3(s) ![]() Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应调至 。
Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应调至 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇耐高温、易存储热值高、节能环保,可做燃料,又是重要的化工原料。科学家用太阳能分解水生成的氢气在催化剂作用下与![]() 反应生成甲醇。已知:
反应生成甲醇。已知:![]() 、
、![]() 和
和![]() 的燃烧热H分别为
的燃烧热H分别为![]() 、
、![]() 和
和![]() 。请回答下列问题:
。请回答下列问题:
(1)用太阳能分解![]() 水消耗的能量是________
水消耗的能量是________![]() 。
。
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为________。
(3)![]() 催化加氢合成甲醇(反应Ⅱ)中伴随着反应Ⅰ的发生:
催化加氢合成甲醇(反应Ⅱ)中伴随着反应Ⅰ的发生:
反应Ⅰ:![]()
反应Ⅱ:![]()
在恒压、![]() 和
和![]() 的起始量一定的条件下,
的起始量一定的条件下,![]() 平衡转化率和平衡时
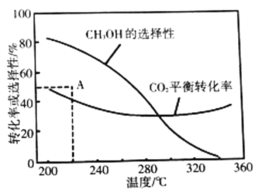
平衡转化率和平衡时![]() 的选择性随温度的变化如图。其中:
的选择性随温度的变化如图。其中:![]() 的选择性
的选择性![]()
①温度高于300℃,![]() 平衡转化率随温度升高而上升的原因是_________。
平衡转化率随温度升高而上升的原因是_________。
②220℃时,在催化剂作用下![]() 与
与![]() 反应一段时间后,测得
反应一段时间后,测得![]() 的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高
的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高![]() 选择性的措施有_________________(写出两点)。
选择性的措施有_________________(写出两点)。
(4)在体积为![]() 的密闭容器中充入
的密闭容器中充入![]() 和
和![]() 发生反应Ⅱ,到平衡时氢气的转化率为25%,求该反应的平衡常数K=________。(结果保留二位有效数字)
发生反应Ⅱ,到平衡时氢气的转化率为25%,求该反应的平衡常数K=________。(结果保留二位有效数字)
(5)研究证实,![]() 也可在硫酸溶液中用惰性电极电解生成甲醇,生成甲醇的电极反应式为__________,另一极电解产物是________________。
也可在硫酸溶液中用惰性电极电解生成甲醇,生成甲醇的电极反应式为__________,另一极电解产物是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬及其化合物在生产生活中具有十分广泛的用途。工业上以铬铁矿(主要成分是Fe(CrO2)2,Cr元素为+3价。含少量MgCO3、Al2O3、SiO2等杂质)为原料制取铬酸钠(Na2CrO4)晶体,其工艺流程如图:
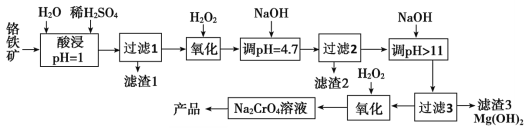
已知:+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO![]() 形式存在且易被氧化。
形式存在且易被氧化。
(1)如Na2SiO3可写成Na2O·SiO2,则Fe(CrO2)2可写成__。
(2)若省略“过滤2”步骤,产品中可能混有__(写化学式)。
(3)流程中两次使用了H2O2进行氧化,第二次氧化时反应的离子方程式为__。
(4)制取铬酸钠后的酸性废水中含有Cr2O![]() ,必须经过处理与净化才能排放。在废水中加入焦炭和铁屑,与酸性Cr2O
,必须经过处理与净化才能排放。在废水中加入焦炭和铁屑,与酸性Cr2O![]() 溶液形成原电池,使Cr2O
溶液形成原电池,使Cr2O![]() 转化为Cr3+,再用石灰乳对Cr3+进行沉降。该电池的正极反应式为__;沉降Cr3+的离子方程式为__,该反应的K=__(列出计算式)。(已知Ksp[Ca(OH2)]=8×10-6,Ksp[Cr(OH)3]=6.3×10-31)
转化为Cr3+,再用石灰乳对Cr3+进行沉降。该电池的正极反应式为__;沉降Cr3+的离子方程式为__,该反应的K=__(列出计算式)。(已知Ksp[Ca(OH2)]=8×10-6,Ksp[Cr(OH)3]=6.3×10-31)
(5)产品铬酸钠可用如图所示方法冶炼铬。
![]()
②的化学方程式为__,在实验室中引发该反应用到的两种药品是__(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,N表示粒子数。下列叙述正确的是( )
A.6.0gSiO2晶体中含有共价键的个数为0.2NA
B.将1molCl2通入水中,则N(HClO)+N(Cl-)+N(ClO-)=2NA
C.3.0g含甲醛(HCHO)的冰醋酸中含有的原子总数为0.4NA
D.将CO2通过Na2O2使其质量增加ag时,反应转移的电子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物是日常生活中的常用调味品。回答下列问题:
(1)五种元素中,原子半径最大的是________,非金属性最强的是________(填元素符号)。
(2)由A分别和B、D、E所形成的共价型化合物中,热稳定性最差的是__________(用化学式表示)。
(3)A、B、E形成的离子化合物电子式为____________,其中存在的化学键类型为____________。
(4)D最高价氧化物的水化物的化学式为________________。
(5)单质D在充足的单质E中燃烧,反应的化学方程式为__________________;D在不充足的E中燃烧,生成的主要产物的化学式为__________。
(6)单质E与水反应的离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压时烯烃与氢气混合不反应,高温时反应很慢,但在适当的催化剂存在时可与氢气反应生成烷烃,一般认为加氢反应是在催化剂表面进行。反应过程的示意图如下:
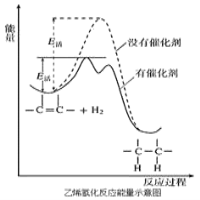

下列说法中正确的是( )
A.乙烯和H2生成乙烷的反应是放热反应
B.加入催化剂,可减小反应的热效应
C.催化剂能改变平衡转化率,不能改变化学平衡常数
D.催化加氢过程中金属氢化物的一个氢原子和双键碳原子先结合,得到中间体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将两种浓度均为![]() 的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
A.![]() 混合溶液(pH=10.30):
混合溶液(pH=10.30):![]()
B.氨水-NH4Cl混合溶液(pH=9.25):![]()
C.![]() 混合溶液(pH=4.76):
混合溶液(pH=4.76): ![]()
D.![]() 混合溶液(pH=1.68,H2C2O4为二元弱酸):
混合溶液(pH=1.68,H2C2O4为二元弱酸): ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com