
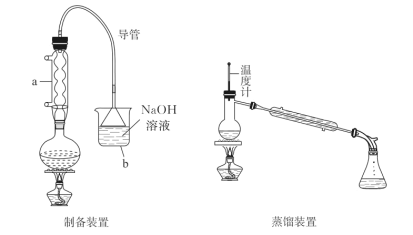
����Ŀ�����嶡����ϡ��Ԫ����ȡ���ܼ����л��ϳɵ��м��壬���Ʊ���ͼ(�г�װ����)��
��֪��i.NaBr+H2SO4(Ũ)=HBr��+NaHSO4
ii.CH3CH2CH2CH2OHʮHBr��CH3CH2CH2CH2Br+H2O
iii.2HBr+H2SO4![]() Br2+SO2+2H2O
Br2+SO2+2H2O
iv.���嶡���ܶȣ�1.27g��mL-1��Ũ�����ܶȣ�1.84g��mL-1
��ش��������⣺
(1)���嶡��ֲ�Ʒ���Ʊ���
������a��������__����Բ����ƿ������ҩƷ˳����ȷ����__(����ȷѡ����ĸ)��
A��ŨH2SO4������ˮ�����������廯�Ʒ�ĩ
B������ˮ��ŨH2SO4�����������廯�Ʒ�ĩ
C������ˮ����������ŨH2SO4���廯�Ʒ�ĩ
D������ˮ�����������廯�Ʒ�ĩ��ŨH2SO4
��װ��b��װ��NaOH��Һ��Ŀ����__��
�ۼ��Ȼ������ڴ��ڼ�Ҫ���ϵ�ҡ����Ӧװ�ã���ԭ��Ϊ__����ȴ���Ϊ����װ�ã����������嶡��Ĵ�Ʒ��
(2)���嶡����ᴿ��
�ٰ����嶡���Ʒ�����Һ©���У���������ˮϴ�ӣ��ֳ��л��㣻
������һ����ķ�Һ©���У�����Ũ����ϴȥ�л�����������δ��Ӧ�����������������__(ѡ�����Ͽ��������¿���)�ֳ��л��㣻
���л���������������ˮ��Ũ���ᡢˮ������NaHCO3��Һ��ˮϴ�ӣ�����ˮCaCl2�������������ˮϴ�Ӽ�Ϊһ����ˮϴ���Ƿ��������˵������__��
(3)����ϴ�Ӻ�����к�ɫ��˵�������嵥�ʣ�Ӧ���������ı���NaHSO3��Һϴ�ӣ����嵥��ȫ����ȥ���䷴Ӧ�����ӷ���ʽΪ__��
����Ͷ��������11.84g���õ�����12.50g������������ת����Ϊ__(������λС��)��
���𰸡����������� B ����β������ֹ��Ⱦ���� ʹ��Ӧ���ֽӴ�����ַ�Ӧ��������嶡��IJ��� �Ͽ� ����������һ��ˮϴ��ȥHBr�����������ڶ��γ�ȥ�ֵ�H2SO4�������γ�ȥNaHCO3������ˮϴ�ɼ����Լ������� Br2+HSO3-+H2O==2Br-+SO42-+3H+ 57.03%
��������
(1)������a�������ܣ���Բ����ƿ������ҩƷʱ��ˮӦ��Ũ����֮ǰ���룬������Ӧ��Ũ����֮����룬��Ϊ����Ũ����֮ǰ���룬��Ũ�������ú���ȣ�ʹ�����������ӷ������ʧ���廯�����ȼ��룬�����Ũ���ᷴӦ�ų����壬�����˷�ԭ�ϣ�������Ⱦ������
��װ��b��װ��NaOH��Һ����Ҫ��Ϊ�����շ�Ӧ���
�ۼ��Ȼ������ڴ��ڼ�Ҫ���ϵ�ҡ����Ӧװ�ã��ӷ�Ӧ��ij�ֽӴ������ԭ�������ʽǶȷ���ԭ��
(2)������һ����ķ�Һ©���У�����Ũ����ϴȥ�л�����������δ��Ӧ�����������������Ϊ�л����ܶȱ�Ũ����С��������Һ����ϲ㣬�ɴ�ȷ�����뷽����
���л���������������ˮϴ�ӣ���ϴȥHBr����������Ũ����ϴ�ӣ���ϴȥδ��ˮϴ��������������ˮϴ����ϴȥŨ�������NaHCO3��Һϴȥ�����ˮϴ�ӣ�ϴȥ���µ��������ᣬ����ˮCaCl2����ȥˮ������������ˮϴ�Ӽ�Ϊһ����ˮϴ�Ӳ���������Ϊ��Ӵ��Լ�������
(3)����ϴ�Ӻ�����к�ɫ��˵�������嵥�ʣ�Ӧ���������ı���NaHSO3��Һϴ�ӣ����嵥��ȫ����ȥ��ͬʱHSO3-������ΪSO42-��ͬʱ����H+��
���ɲ�������12.50g���������������ʵ�����Ҳ�͵��ڷ�Ӧ��ı仯������Ͷ��������11.84g�����������������ʼ�����Ӷ������������ת���ʡ�
(1)������a�����������ܣ���Բ����ƿ������ҩƷʱ��ˮӦ��Ũ����֮ǰ���룬������Ӧ��Ũ����֮����룬��Ϊ����Ũ����֮ǰ���룬��Ũ�������ú���ȣ�ʹ�����������ӷ������ʧ���廯�����ȼ��룬�����Ũ���ᷴӦ�ų����壬�����˷�ԭ�ϣ�������Ⱦ�������ɴ˵ó���Բ����ƿ������ҩƷ˳����ȷ����B����Ϊ�����������ܣ�B��
��װ��b��װ��NaOH��Һ����Ŀ����Ҫ��Ϊ������β������ֹ��Ⱦ��������Ϊ������β������ֹ��Ⱦ������
�ۼ��Ȼ������ڴ��ڼ�Ҫ���ϵ�ҡ����Ӧװ�ã���ԭ��Ϊʹ��Ӧ���ֽӴ�����ַ�Ӧ��������嶡��IJ��ʡ���Ϊ��ʹ��Ӧ���ֽӴ�����ַ�Ӧ��������嶡��IJ��ʣ�
(2)������һ����ķ�Һ©���У�����Ũ����ϴȥ�л�����������δ��Ӧ�����������������Ϊ�л����ܶȱ�Ũ����С��������Һ����ϲ㣬Ӧ���Ͽڷֳ��л��㡣��Ϊ���Ͽڣ�
���л���������������ˮϴ�ӣ���ϴȥHBr����������Ũ����ϴ�ӣ���ϴȥδ��ˮϴ��������������ˮϴ����ϴȥŨ�������NaHCO3��Һϴȥ�����ˮϴ�ӣ�ϴȥ���µ��������ᣬ����ˮCaCl2����ȥˮ������������ˮϴ�Ӽ�Ϊһ����ˮϴ�Ӳ���������Ϊ��Ӵ��Լ���������Ϊ������������һ��ˮϴ��ȥHBr�����������ڶ��γ�ȥ�ֵ�H2SO4�������γ�ȥNaHCO3������ˮϴ�ɼ����Լ���������
(3)����ϴ�Ӻ�����к�ɫ��˵�������嵥�ʣ�Ӧ���������ı���NaHSO3��Һϴ�ӣ����嵥��ȫ����ȥ��ͬʱHSO3-������ΪSO42-��ͬʱ����H+����Ӧ�����ӷ���ʽΪBr2+HSO3-+H2O=2Br-+SO42-+3H+����Ϊ��Br2+HSO3-+H2O=2Br-+SO42-+3H+��
������������ʼͶ����Ϊn(������)=![]() =0.16mol�����嶡�����ʵ���Ϊ
=0.16mol�����嶡�����ʵ���Ϊ![]() =0.09124mol����μӷ�Ӧ�������������ʵ���Ϊ0.09124mol���Ӷ������������ת����Ϊ
=0.09124mol����μӷ�Ӧ�������������ʵ���Ϊ0.09124mol���Ӷ������������ת����Ϊ![]() = 57.03%����Ϊ��57.03%��
= 57.03%������57.03%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС���о���������������ʱ���ı��ܱ�������ijһ������X2 (g)+3Y2 (g)=2XY3(g)��ѧƽ��״̬��Ӱ�죬�õ���ͼ��ʾ�����ߣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ������������ж���ȷ����
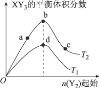
A.��T2>T1��������Ӧһ���Ƿ��ȷ�Ӧ
B.T2��n (X2)���䣬�ﵽƽ��ʱ��XY3�����ʵ�����c>b>a
C.T2��n(X2)���䣬�ﵽƽ��ʱ��X2��ת����:b>a>c
D.��T2>T1���ﵽƽ��ʱb��d�������Ӧ����:v(d)>v (b)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵������ȷ���ǣ� ��
A.����������1molCl2��Ȼ�գ�����ת�Ƶ�����Ϊ2NA
B.��50g��������Ϊ46%���Ҵ�ˮ��Һ�У�����ԭ������Ϊ6NA
C.5NH4NO3![]() 2HNO3+4N2��+9H2O��Ӧ�У�����28gN2ʱ��ת�Ƶĵ�����ĿΪ3.75NA
2HNO3+4N2��+9H2O��Ӧ�У�����28gN2ʱ��ת�Ƶĵ�����ĿΪ3.75NA
D.1L1mol/LNaF��Һ��F-����ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С���������ữ�ĸ��������Һ�������Һ��Ӧ�ⶨ��λʱ��������CO2������̽��Ӱ�췴Ӧ���ʵ����ء����ʵ�鷽�������
ʵ����� | A��Һ | B��Һ |
�� | 20mL0.1mol��L-1H2C2O4��Һ | 30mL0.02mol��L-1����KMnO4��Һ |
�� | 20mL0.2mol��L-1H2C2O4��Һ | 30mL0.02mol��L-1����KMnO4��Һ |
��1��ͼ1װ����ʢ��A��Һ������������_____��������ͼ1װ�������Եķ���Ϊ_____��

��2�������ữ�ĸ��������Һ�������Һ��Ӧ�Ļ�ѧ��Ӧ����ʽΪ_____��
��3����ʵ��̽������_____���ضԻ�ѧ��Ӧ���ʵ�Ӱ�죬��ʵ�����40sĩ�ռ���22.4mLCO2(��״����)������40s�ڣ�v(MnO4-)=_____(������Һ���ǰ������ı仯)��
��4��С��ͬѧ��ͼ1�������ռ�װ�ø�Ϊͼ2��ʵ�������ȴ����ʱ����������Һ����ڸ����Һ�棬Ϊ�õ�ȷ���ݣ���ȡ�IJ����ǣ�____��
��5������ͨ���ⶨ��λʱ��������CO2��������ȽϷ�Ӧ���ʣ���ʵ�黹����ͨ���ⶨ____���Ƚϻ�ѧ��Ӧ���ʡ�
��6��ͬѧ����ʵ���з��ַ�Ӧ����������ͼ3��ʾ��̽��t1��t2ʱ�������ʱ�����Ҫԭ������ǣ�____��
A.�÷�Ӧ���� B.���ɵ�Mn2+������� C.K2SO4Ũ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ķ����в��ϣ��ش�����С��
��һ�����������������ˮ��Ͽ��Ƶ����ᡣ������һ����Ҫ�Ļ���ԭ�ϣ���;ʮ�ֹ㷺�������ڻ�ѧ��ҵ�⣬���dz��㷺Ӧ���ڷ��ϡ��Ǽ�������������Ʒ���������Ӽ���ըҩ������ȷ��档
��1������Ũ�����˵����ȷ����
A.�ӷ�
B.����ֽ�
C.�ܶȱ�ˮ��С
D.��������ʹ��Ƭ�ۻ���Ũ������������
��2��ϡ�����������ʵ��������������Ӧ����ʽΪZn+H2SO4=ZnSO4+H2�����÷�Ӧ�ķ�Ӧ����˵����ȷ����
A.���Ϸ�ӦB.���ֽⷴӦC.�û���ӦD.�ֽⷴӦ
��3���������������������£������������п��Ӧ�������������ʣ����Բ��õĴ�ʩ��
A.ѡ�ÿ��������п��
B.���߷�Ӧ�¶�
C.��98%Ũ����������ϡ���ᷴӦ
D.�����������Һ
��4�����з�Ӧ�У����������������ڷ�Ӧ������������
A.S+O2![]() SO2
SO2
B.CaO+H2O=Ca(OH)2
C.C+CO2![]() 2CO
2CO
D.Zn+H2SO4=ZnSO4+H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����
A.MgO(s)��C(s)=CO(g)��Mg(g)���������Է����У���÷�Ӧ��H��0����S��0
B.�����µ����ʵ���Ũ�ȵ�CH3COOH��Һ��HCl��Һ�У�ˮ�ĵ���̶���ͬ
C.0.1 mol��L��1 NH4Cl��Һ��ˮϡ�ͣ�![]() ��ֵ����
��ֵ����
D.���ڷ�Ӧ2SO2��O22SO3��ʹ�ô����ܼӿ췴Ӧ���ʲ����SO2��ƽ��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ݻ���Ϊ2 L�ļס��Һ����ܱ�����������г���1.5 mol CO2��3 mol H2�����г���2 mol CO2��3 mol H2��һ�������½�������Ӧ��CO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g),ʵ���÷�Ӧ��ϵ��CO2��ƽ��ת�������¶ȵĹ�ϵ������ͼ��ʾ������˵����ȷ����
CH3OH(g)��H2O(g),ʵ���÷�Ӧ��ϵ��CO2��ƽ��ת�������¶ȵĹ�ϵ������ͼ��ʾ������˵����ȷ����

A.�÷�Ӧ����H��0
B.��������ʾ��������CO2��ƽ��ת�������¶ȵĹ�ϵ
C.500 Kʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ200
D.700 Kʱ�����������ܱ������г���0.9 mol CO2��1.2 mol H2��0.1 mol CH3OH��0.1mol H2O����ﵽƽ��ʱ��H2�������������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NH3��NOx��SO2������������ɻ�����Ⱦ���������Щ����������þͿ��Ա��Ϊ�����ȼ����˶Ի�������Ⱦ���ֽ���˲�����ԴΣ�����⡣
��l�����᳧���ô���ԭ��������β����CH4�ڴ������¿��Խ�NO2��ԭΪN2����֪��
![]() ��
��
![]() ��
��
��Ӧ![]() ��1����H=_______
��1����H=_______
��2����ҵ�����ð������������ᣨHCN���ķ�ӦΪ��
����һ���¶������£���2L�����ܱ������м���2 mol CH4��2 mol NH3��ƽ��ʱNH3�������Ϊ30%������ʱ��Ϊ10 min�����ʱ�������CH4��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ______ mol��L-l��min-1�����¶���ƽ�ⳣ��K= ___���������¶Ȳ��䣬���������м���CH4��H2��1 mol�����ʱv�� ___������>����=������<����v�� ��
����������һ�����ﵽƽ��ʱNH3ת�������������X�仯�Ĺ�ϵ��ͼ1��ʾ��X���� ___������ĸ���ţ���
A �¶� B ѹǿ C ԭ����CH4��NH3�������
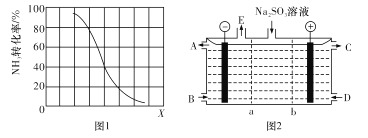
��3��ij�о�С����NaOH��Һ����β���еĶ��������õ���Na2SO3���е���������ᣬ����������Ĥ��ϵ��װ����ͼ2��ʾ���缫����Ϊʯī��A--E�ֱ���������е�ԭ�ϻ��Ʒ��b��ʾ____�����������������������ӽ���Ĥ�������ĵ缫��ӦʽΪ_______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.Ǧ���طŵ�ʱ�������������ᣬ��������
B.����CH3COONa��Һ���¶ȣ���ˮ�����ӻ�������pH������
C.CH3CH=CHCH3�����е��ĸ�̼ԭ�Ӷ���һ��ֱ����
D.������Ksp(AgBr)=5.0��10-13��Ksp(AgCl)=1.8��10-10����S(AgBr)>S(AgCl)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com