
| A、电解NaCl溶液时,阴极产生1 mol Cl2的同时阳极产生l molH2 |
| B、0.1 mol?L-1AlCl3溶液中Al3+的浓度为0.1 mol?L-1 |
| C、7 g 14C中所含中子数为4 NA(设NA为阿伏加德罗常数的值) |
| D、2.24 L氯气与足量NaOH稀溶液反应,转移0.1 mol电子 |
| m |
| M |
| 7g |
| 14g/mol |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、常温下,1molCl2与足量NaOH溶液完全反应,转移的电子数2NA |
| B、常温常压下,32g氧气和臭氧混合气体中所含有的氧原子数为2NA |
| C、标准状况下,22.4L水所含原子数为3NA |
| D、同温同压下,NA个NO2与NA个N2和O2的混合气体的体积不相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
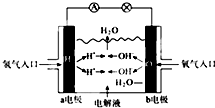
| A、a电极是负极 |
| B、b电极的电极反应为O2+4e-+2H2O=4OH- |
| C、工作时,溶液中阴离子向正极移动,阳离子向负极移动 |
| D、此电池能将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸馏时,通入冷凝管的水从其上口流进,下口流出 |
| B、一束平行光照射CuSO4溶液时,从侧面可看到光亮的通路 |
| C、电解质溶液导电的原因是因为有自由移动的离子 |
| D、将饱和的FeCl3溶液滴入沸腾的NaOH溶液中可制得氢氧化铁胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金刚石和石墨互为同素异形体 | ||||
| B、1H、2H和3H互为同位素 | ||||
| C、18O和16O是两种不同的核素 | ||||
D、氡的放射性同位素
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2L氯仿中含有的C-Cl键的数目为1.5NA |
| B、标准状况下,30g NO和16g O2混合所生成的气体分子数为NA |
| C、某温度时,1L pH=6的纯水中含有1.0×10-6NA个H+ |
| D、28g铁粉与足量Cl2反应时转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,向A中充入1mol X和1mol Y,向B中充入2mol X和2mol Y,起始VA=VB=a L,在相同温度和有催化剂的条件下,两容器中各自发生下列反应X(g)+Y(g)?2N(g)+W(g),△H>0达到平衡时,v(A)=1.2aL,则下列说法错误的是( )
如图所示,向A中充入1mol X和1mol Y,向B中充入2mol X和2mol Y,起始VA=VB=a L,在相同温度和有催化剂的条件下,两容器中各自发生下列反应X(g)+Y(g)?2N(g)+W(g),△H>0达到平衡时,v(A)=1.2aL,则下列说法错误的是( )| A、反应开始时,B容器中化学反应速率快 |
| B、A容器中X的转化率为40%,且比B中X的转化率小 |
| C、打开K一段时间,达到新平衡时,A的体积为2.6aL(两边通管中气体体积不计) |
| D、打开K达新平衡后,升高B容器温度,A容器体积会增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com