
 ��ͼ��ʾ����A�г���1mol X��1mol Y����B�г���2mol X��2mol Y����ʼVA=VB=a L������ͬ�¶Ⱥ��д����������£��������и��Է������з�ӦX��g��+Y��g��?2N��g��+W��g������H��0�ﵽƽ��ʱ��v��A��=1.2aL��������˵��������ǣ�������
��ͼ��ʾ����A�г���1mol X��1mol Y����B�г���2mol X��2mol Y����ʼVA=VB=a L������ͬ�¶Ⱥ��д����������£��������и��Է������з�ӦX��g��+Y��g��?2N��g��+W��g������H��0�ﵽƽ��ʱ��v��A��=1.2aL��������˵��������ǣ�������| A����Ӧ��ʼʱ��B�����л�ѧ��Ӧ���ʿ� |
| B��A������X��ת����Ϊ40%���ұ�B��X��ת����С |
| C����Kһ��ʱ�䣬�ﵽ��ƽ��ʱ��A�����Ϊ2.6aL������ͨ��������������ƣ� |
| D����K����ƽ�������B�����¶ȣ�A������������� |
| 0.4mol |
| 1mol |


 �����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д�
�����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д� �����ҵ�����������ѧ���ӳ�����ϵ�д�
�����ҵ�����������ѧ���ӳ�����ϵ�д� ����ѧ��Ӯ�����ϵ�д�
����ѧ��Ӯ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����NaCl��Һʱ����������1 mol Cl2��ͬʱ��������l molH2 |
| B��0.1 mol?L-1AlCl3��Һ��Al3+��Ũ��Ϊ0.1 mol?L-1 |
| C��7 g 14C������������Ϊ4 NA����NAΪ�����ӵ�������ֵ�� |
| D��2.24 L����������NaOHϡ��Һ��Ӧ��ת��0.1 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
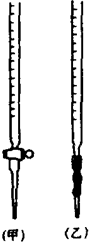 ij��ѧ��ȤС��Ϊ�˲ⶨ����Ũ�ȼ������ữ�ĸ��������Һ����ᣨH2C2O4����Һ��Ӧ�Ļ�ѧ��Ӧ���ʴ�С����֤���ӷ�Ӧ�ı��ʣ����������ʵ�飮��ѧ��Ӧ���£�KMnO4+H2C2O4+H2SO4-K2SO4+MnSO4+CO2��+H2O ʵ����Ҫ�������£�����0.1000mol?L-1���Ը��������Һ�ζ�δ֪Ũ�ȵ�H2C2O4��Һ�ⶨ��ѧ��Ӧ���ʣ�����֤�Ϻ�ɫ��MnO4-���ӣ���ش�
ij��ѧ��ȤС��Ϊ�˲ⶨ����Ũ�ȼ������ữ�ĸ��������Һ����ᣨH2C2O4����Һ��Ӧ�Ļ�ѧ��Ӧ���ʴ�С����֤���ӷ�Ӧ�ı��ʣ����������ʵ�飮��ѧ��Ӧ���£�KMnO4+H2C2O4+H2SO4-K2SO4+MnSO4+CO2��+H2O ʵ����Ҫ�������£�����0.1000mol?L-1���Ը��������Һ�ζ�δ֪Ũ�ȵ�H2C2O4��Һ�ⶨ��ѧ��Ӧ���ʣ�����֤�Ϻ�ɫ��MnO4-���ӣ���ش�| �ζ����� | H2C2O4��� | �ζ�ǰKMnO4��� | �յ�ʱKMnO4��� |
| 1 | 25.00mL | 0.00mL | 21.40mL |
| 2 | 25.00mL | 0.02mL | 21.44mL |
| 3 | 25.00mL | 0.04mL | 22.46mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
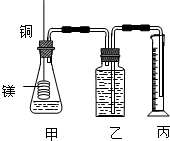 ij�о���ѧϰС��Ϊ֤����ͬ��ͬѹ�£���ͬŨ����ͬ����IJ�ͬǿ�ȵ�һԪ��������þ����Ӧʱ�����������������ͬ����Ӧ���ʲ�ͬ��ͬʱ�ⶨʵ���������µ�����Ħ�������Ƶļ���ʵ��װ��ͼ����ʵ�����Ҫ�����������£�
ij�о���ѧϰС��Ϊ֤����ͬ��ͬѹ�£���ͬŨ����ͬ����IJ�ͬǿ�ȵ�һԪ��������þ����Ӧʱ�����������������ͬ����Ӧ���ʲ�ͬ��ͬʱ�ⶨʵ���������µ�����Ħ�������Ƶļ���ʵ��װ��ͼ����ʵ�����Ҫ�����������£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ ��ϡ� | �� | �� | �� | ���������� | ���������� |
| A | ���� | ���� | �ռ� | ������ | ������̼ |
| B | �ռ� | ���� | ʳ�� | ����þ | һ����̼ |
| C | ������ | ���� | ̼��� | �������� | �������� |
| D | ���Լ� | ���� | С�մ� | ������ | �������� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2 molA+1 molB |
| B��2 molA+1 molB+3 molC+1 molD |
| C��3 molC+1 molD |
| D��3 molC+1 molD+1 molB |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com