
【题目】氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图所示。下列叙述错误的是( )

A.H3BO3在水溶液中发生H3BO3+H2O![]() H++[B(OH4)],可知H3BO3是一元弱酸
H++[B(OH4)],可知H3BO3是一元弱酸
B.六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,立方氮化硼晶胞中含有4个氮原子、4个硼原子
C.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,lmolNH4BF4含有配位键的数目为NA
D.由B2O3可制备晶体硼,晶体硼的熔点2573K,沸点2823K,硬度大,属于共价晶体
【答案】C
【解析】
A.由H3BO3在水溶液中的电离方程式H3BO3+H2O![]() H++[B(OH4)]可知,H3BO3是一元弱酸,故A正确;
H++[B(OH4)]可知,H3BO3是一元弱酸,故A正确;
B.描述晶体结构的基本单元叫做晶胞,金刚石晶胞是立方体,其中8个顶点有8个碳原子,6个面各有6个碳原子,立方体内部还有4个碳原子,金刚石的一个晶胞中含有的碳原子数8×![]() +6×
+6×![]() +4=8,则立方氮化硼晶胞中应该含有4个N和4个B原子,故B正确;
+4=8,则立方氮化硼晶胞中应该含有4个N和4个B原子,故B正确;
C.NH4BF4中,NH4+中含有氮氢配位键,BF4—中含有硼氟配位键,则lmolNH4BF4含有配位键的数目为2NA,个C错误;
D.共价晶体具有很高的熔沸点和很大的硬度,晶体硼的熔点2573K,沸点2823K,硬度大说明晶体硼属于共价晶体,故D正确;
故选C。


科目:高中化学 来源: 题型:
【题目】乙烯是重要的化工原料,目前主要通过石油炼化制备。随着化石燃料资源日益减少,科研工作者正在探索和研发制备乙烯的新方法。
Ⅰ.甲烷在一定条件下脱氢可生成乙烯:2CH4(g)![]() C2H4(g)+2H2(g)△H>0
C2H4(g)+2H2(g)△H>0
(1)活化能Ea正____Ea逆(填“>”、“=”或“<”,下同);k正、k逆表示速率常数,当升高温度时,k正增大的倍数____k逆增大的倍数。
Ⅱ.利用生物无水乙醇催化脱水制备乙烯
主反应 i:C2H5OH(g)![]() C2H4(g)+H2O(g)△H1=+45.5 kJ/mol
C2H4(g)+H2O(g)△H1=+45.5 kJ/mol
副反应 ii:2C2H5OH(g)![]() C2H5OC2H5(g)+H2O(g)△H2=﹣19.0 kJ/mol
C2H5OC2H5(g)+H2O(g)△H2=﹣19.0 kJ/mol
副反应 iii:C2H5OC2H5(g)![]() 2C2H4(g)+H2O(g)△H3
2C2H4(g)+H2O(g)△H3
(2)求△H3=____。
(3)在 2L 恒容密闭容器中充入2mol C2H5OH(g)和一定量的催化剂进行反应,平衡体系中含碳组分的物质的量分数随温度的变化如图所示:
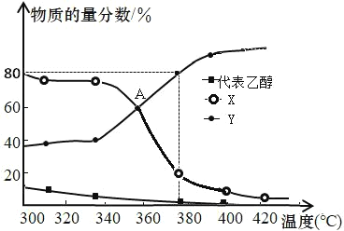
①图中 Y 代表____(填“C2H4”或“C2H5OC2H5”),请解释原因____。
②主反应 i 在 A 点达到平衡状态的标志为____。
a.乙烯浓度不再变化 b.容器内压强不随时间变化
c.混合气体的密度不随时间变化 d.△H 不再变化
③380℃时,假设乙醇完全反应,则反应 iii 的平衡常数 K=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会密切相关,下列说法正确的是 ( )
A.通信光缆的主要成分是晶体Si,太阳能电池的材料主要是SiO2
B.高锰酸钾溶液、酒精、双氧水都能杀菌消毒,都利用了强氧化性
C.“光化学烟雾”、“臭氧空洞”的形成都与氮氧化合物有关
D.以“地沟油”为原料生产的生物柴油与以“石油”为原料生产的柴油化学成分相似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W,已知X的某种氢化物可使溴的四氯化碳溶液褪色,X原子电子占据2个电子层;Y广泛作电池材料且单位质量的金属提供电子数目最多;实验室可用Z的简单氢化物的浓溶液和KMnO4固体在常温下制备Z的单质:向含W元素的钠盐溶液中通入x的氧化物,观察到沉淀质量(m)与X的氧化物体积(V)关系如图所示。下列说法正确的是( )
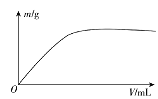
A.Y的单质在空气中燃烧生成过氧化物和氮化物
B.W一定位于周期表中第三周期IIIA族
C.X的含氧酸的酸性可能比Z的含氧酸的酸性强
D.Z和W组成的化合物可能是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高碘酸钾(KIO4)溶于热水,微溶于冷水和氢氧化钾溶液,可用作有机物的氧化剂。制备高碘酸钾的装置图如下(夹持和加热装置省略)。回答下列问题:
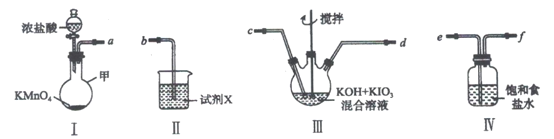
(1)装置I中盛放浓盐酸的仪器名称是___________。
(2)装置I中浓盐酸与KMnO4混合后发生反应的离子方程式是___________。
(3)装置Ⅱ中的试剂X的作用___________。
(4)上述炭置按气流由左至右各接口顺序为___________(用字母表示)。
(5)装置连接好后,将装置Ⅲ水浴加热,通入氯气一段时间,冷却析岀高碘酸钾晶体,经过滤,洗涤,干燥等步骤得到产品。
①写出装置Ⅲ中发生反应的化学方程式:___________。
②洗涤时,与选用热水相比,选用冷水洗涤晶体的优点是___________。
③上述制备的产品中含少量的KIO3,其他杂质忽略,现称取a g该产品配制成溶液,然后加入稍过量的用醋酸酸化的KI溶液,充分反应后,加入几滴淀粉溶液,然后用1.0mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液的平均体积为b L。
已知:KIO3+5KI+6CH3COOH===3I2+6CH3COOK+3H2O;KIO4+7KI+8CH3 COOH===4I2+8CH3COOK+4H2O;I2+2Na2S2O3===2NaI+N2S4O6则该产品中KIO4的百分含量是___________(Mr(KIO3)=214,Mr(KIO4)=230,列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管桩,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是( )
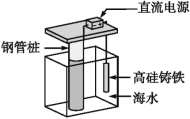
A.通电后外电路电子被强制从高硅铸铁流向钢管桩
B.高硅铸铁的作用是作为损耗阳极材料和传递电流
C.通入保护电流使钢管桩表面腐蚀电流接近于零
D.通入的保护电流应该根据环境条件变化进行调整
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、D、E、G、J在周期表中的位置如下:
A | |||||||
B | D | ||||||
E | G | J |
根据上表回答问题:
(1)![]() 在周期表中的位置是______,D的原子结构示意图_____。
在周期表中的位置是______,D的原子结构示意图_____。
(2)![]() 、B、E、G的原子半径由大到小的顺序是_____
、B、E、G的原子半径由大到小的顺序是_____![]() 填元素符号
填元素符号![]() 。
。
(3)![]() 、D的气态氢化物的稳定性关系为______
、D的气态氢化物的稳定性关系为______![]() 填化学式
填化学式![]() ,它们都属于______
,它们都属于______![]() 离子化合物或共价化合物
离子化合物或共价化合物![]() 。
。
(4)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的化学方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
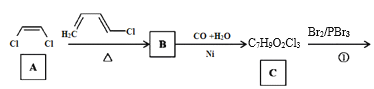
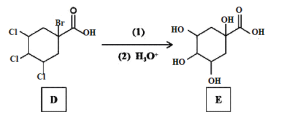
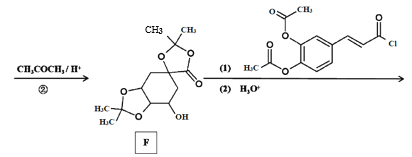
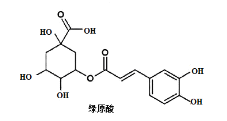
【题目】传统中药“金银花”中抗菌杀毒的有效成分是“绿原酸”。某高中化学创新兴趣小组运用所学知识并参考相关文献,设计了一种“绿原酸”的合成路线如图:
已知:① ;
;
②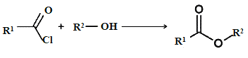 。
。
回答下列问题:
(1)有机物A的名称是___,A→B的反应类型___。
(2)C的结构简式___,有机物F中官能团的名称是___。
(3)若碳原子上连有4个不同的原子或基团时,该碳原子称为手性碳。用星号(*)标出E中的手性碳: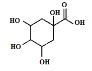 ___。
___。
(4)反应②的目的是__,写出D→E中第(1)步的反应方程式___。
(5)绿原酸在碱性条件下完全水解后,再酸化,得到的芳香族化合物的同分异构体有多种,满足以下条件的有___种(不考虑立体异构,任写一种)。
a.含有苯环
b.1mol该物质能与2molNaHCO3反应
写出核磁共振氢谱显示峰面积之比为3:2:2:1的结构简式为__。
(6)参照上述合成方法,设计由丙酸为原料制备高吸水性树脂聚丙烯酸钠的合成路线___(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯是一种食用香料,其结构简式如图,有关柠檬烯的分析正确的是
![]()
A.一定条件下,它分别可以发生加成、取代、氧化、还原等反应
B.它的分子式为C10H18
C.它的分子中所有的碳原子一定在同一平面上
D.它和丁基苯(![]() C4H9)互为同分异构体
C4H9)互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com