
【题目】已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为________,该元素的符号是________。
(2)Y元素原子的价层电子的轨道表示式为________,该元素的名称是________。
(3)X与Z可形成化合物XZ3,该化合物的空间构型为________。
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是________________________________。
(5)比较X的氢化物与同族第二、三周期元素所形成的氢化物稳定性、沸点高低并说明理由_______。
【答案】 1s22s22p63s23p63d104s24p3 As 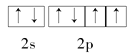 氧 三角锥形 As2O3+6Zn+6H2SO4===2AsH3↑+6ZnSO4+3H2O 稳定性:NH3>PH3>AsH3,因为元素非金属性越强其简单氢化物越稳定;沸点:NH3> AsH3>PH3,因为NH3 分子间存在氢键,沸点最高,AsH3相对分子质量大于PH3,因而范德华力较大,沸点高于PH3
氧 三角锥形 As2O3+6Zn+6H2SO4===2AsH3↑+6ZnSO4+3H2O 稳定性:NH3>PH3>AsH3,因为元素非金属性越强其简单氢化物越稳定;沸点:NH3> AsH3>PH3,因为NH3 分子间存在氢键,沸点最高,AsH3相对分子质量大于PH3,因而范德华力较大,沸点高于PH3
【解析】试题分析: X元素原子的4p轨道上有3个未成对电子,则X为33号元素As元素;Y元素原子的最外层2p轨道上有2个未成对电子,则Y可能为6号的C或8号的O。X跟Y可形成化合物X2Y3,则Y的非金属性强于X、Y显-2价、X显+3价,故Y为8号O元素;X、Y和Z三种元素的原子序数之和等于42,Z元素可以形成负一价离子,则Z为1号H元素。综上所述,X、Y和Z三种元素分别为As、O、H。
(1)X元素原子基态时的电子排布式为1s22s22p63s23p63d104s24p3,该元素的符号是As。
(2)Y元素原子的价层电子的轨道表示式为 ,该元素是氧。
,该元素是氧。
(3)X与Z可形成化合物AsH3,其空间构型与NH3相似,为三角锥形。
(4)化合物As2O3在稀硫酸溶液中可被金属锌还原为AsH3,产物还有ZnSO4和H2O,该反应的化学方程式是As2O3+6Zn+6H2SO4===2AsH3↑+6ZnSO4+3H2O。
(5)N、P、As三种元素的非金属性依次减弱,因为元素非金属性越强其简单氢化物越稳定,所以As的氢化物与同族第二、三周期元素所形成的氢化物稳定性由强到弱的顺序为NH3>PH3>AsH3,因为NH3分子间存在氢键,沸点最高,AsH3相对分子质量大于PH3,因而范德华力较大,沸点高于PH3,所以X的氢化物与同族第二、三周期元素所形成的氢化物沸点由高到低的顺序为NH3> AsH3>PH3。


科目:高中化学 来源: 题型:
【题目】实验室中以Zn、CrCl3溶液、CH3COONa溶液和盐酸为主要原料制备醋酸亚铬晶体,其装置如下图所示。仪器2中已预先加入锌粒,仪器3中已加人CH3COONa溶液。

资料卡:
①醋酸亚铬晶体[[Cr(CH3COO)2]22H2O;深红色晶体,不溶于冷水,是常用的氧气吸收剂。
②Cr2+不稳定,极易被氧气氧化,不与锌反应。
③部分相关的化学反应:
2CrCl3+Zn═2CrCl2+ZnCl2
2Cr2++4CH3COO-+2H2O═[Cr(CH3COO)2]22H2O
④Ksp[Cr(OH)3]=6.3×10-31,![]() ≈4,lg2≈0.3
≈4,lg2≈0.3
回答下列问题:
(1)仪器1的名称是_______________。
(2)实验时先往仪器2中加盐酸,一段时间后再加CrCl3溶液,目的是_________。
(3)为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应关闭阀门_______,打开阀门_______。
(4)本实验中锌粒要过量,其原因除了使产生的H2将CrCl2溶液压入装置3与CH3COONa溶液反应外,另一个作用是_______________。
(5)铬的离子会污染水资源。常温下要除去上述实验中多余的Cr2+,①先向废液中通入足量的______,将Cr2+转变为Cr3+,反应的离子方程式为_______;②再加入碱液,调节pH至少为_____才能使Cr3+沉淀完全[c(Cr3+)<10-5mol/L]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 烷烃的通式为 CnH2n+2,随 n 值增大,碳元素的质量百分含量逐渐减小
B. 乙炔与苯的实验式为 CH,是含碳量最高的物质
C. 1 摩尔苯恰好与 3 摩尔氢气完全加成,说明一个苯分子中有三个碳碳双键
D. n=7,主链上有 5 个碳原子的烷烃共有五种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数, A的原子半径小于B,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。
(1)基态E原子的价电子排布图_______________。
(2)B、C、D三元素第一电离能由大到小的顺序为(用元素符号表示)______________。
(3)BD![]() 中心原子杂化轨道的类型为______杂化;CA
中心原子杂化轨道的类型为______杂化;CA![]() 的空间构型为_______(用文字描述)。
的空间构型为_______(用文字描述)。
(4)1 mol BC-中含有π键的数目为______。
(5)比较D、E元素最简单氢化物的稳定性_______(填化学式,用“>”连接),理由是_______________。
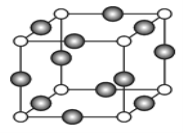
(6)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是____,C原子的配位数是_____。若相邻C原子和F原子间的距离为anm,阿伏伽德罗常数为NA,则该晶体的密度为______g/cm3(用含a、NA的符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各反应中,盐酸既表现出酸性又表现出氧化性的是
A. HCI+NaOH===NaCl+H2O B. Zn+2HCl===ZnCl2+H2↑
C. HCl+AgNO3==AgCl↓+HNO3 D. MnO2+4HCl(浓) ![]() MnCl2+C12↑+2H2O
MnCl2+C12↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有BaCl2和NaCl的混合溶液VL,将它分成两等份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀。反应中消耗amolH2SO4、bmolAgNO3。则原混合溶液中的c(Na+)为
A. ![]() mol/L B.
mol/L B. ![]() mol/L C.
mol/L C. ![]() mol/L D.
mol/L D. ![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量Fe、FeO、Fe2O3的混合物中,加入50mL1mol·L-1硫酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的混合物,能得到铁的质量为
A. 11.2g B. 2.8g C. 5.62g D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国古代文物不仅彰显了民族和文化自信,还蕴含许多化学知识。下列说法不正确的是
A. 两代“四羊方尊”属于青铜制品,青铜是一种铜锡合金
B. 宋代《莲塘乳鸭图》缂丝中使用的丝,主要成分是蛋白质
C. 清代乾隆“瓷母”是指各种釉彩大瓶,主要成分是二氧化硅
D. 东晋《洛神赋图》中的绿色颜料铜绿,主要成分是碱式碳酸铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com