
【题目】钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1 mol/L的下列五种钠盐溶液的pH如表所示:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
上述几种钠盐的阴离子,结合氢离子能力最强的是______(填离子符号),根据表中数据,将浓度均为0.01mol/L的下列四种溶液分别稀释100倍,pH变化最大的是______.(填字母)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)已知几种离子开始沉淀时溶液的pH如下表所示:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含有相同浓度的Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时,________(填离子符号)先沉淀;Ksp[Fe(OH)2]______(填“>”“=”或“<”)Ksp[Mg(OH)2];要使0.2 mol/L的硫酸铜溶液中铜离子沉淀较为完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液使溶液pH=_______。{Cu(OH)2的Ksp=2×10-20。}
【答案】CO32- C Cu2+ < 6
【解析】
(1)阴离子越容易水解的盐,越容易结合氢离子,相同浓度的钠盐溶液,溶液的pH越大,则盐的水解程度越大,浓度相同的酸稀释相同的倍数后,酸性越强的酸其pH变化越大;
(2)开始沉淀时pH小的离子先沉淀,溶度积常数越小的物质越先沉淀;0.2mol/L的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使c(Cu2+)=0.0002mol/L,根据Ksp计算pH。
(1)这五种盐都是强碱弱酸盐,形成该盐的酸性越弱,则弱酸根越容易水解,越容易结合氢离子,相同浓度的钠盐溶液,其pH就越大,根据酸的电离平衡常数大小可知:最易水解的盐是碳酸钠,所以最容易结合氢离子的阴离子是CO32-;浓度相同的酸稀释相同的倍数后,酸性越强的酸其pH变化越大,HCN、HClO、CH3COOH、H2CO3四种酸的酸性大小顺序是CH3COOH>H2CO3>HClO>HCN,所以溶液的pH变化最大的是醋酸,故合理选项是C;
(2)Fe(OH)2、Cu(OH)2、Mg(OH)2的组成相似,对于组成相似的难溶性物质来说,形成沉淀的pH小的离子先沉淀,溶度积常数越小的物质越先沉淀,由几种离子开始沉淀时溶液的pH大小关系可知:Cu2+先形成沉淀,形成沉淀的溶液的pH越大,则其Ksp就越大,根据表格数据可知Ksp[Fe(OH)2]<Ksp[Mg(OH)2];要使0.2mol/L的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使c(Cu2+)=0.0002mol/L,c(OH-)=![]() =10-8mol/L,所以c(H+)=(10-14÷10-8)mol/L=10-6mol/L,所以溶液的pH=6。
=10-8mol/L,所以c(H+)=(10-14÷10-8)mol/L=10-6mol/L,所以溶液的pH=6。


科目:高中化学 来源: 题型:
【题目】汽车剧烈碰撞时,安全气囊中发生反应 10NaN3+2KNO3 =K2O+5X+16N2↑,下列说 法不正确的是( )
A.X 的化学式为 Na2O
B.上述反应中 NaN3 被氧化,KNO3 发生还原反应
C.每生成 1.6molN2,则转移的电子为 3 mol
D.若被氧化的 N 原子的物质的量为 3mol,则氧化产物比还原产物多 1.4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法正确的是
A.12.0gNaHSO4溶于1L水中,溶液中氢离子的浓度为0.1mol/L
B.25℃时气体的摩尔体积大于22.4L/mol
C.阿伏加德罗常数近似为6.02×1023
D.氦气的摩尔质量是4g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是有机合成中间体,可合成高聚物。G合成线路图如下:
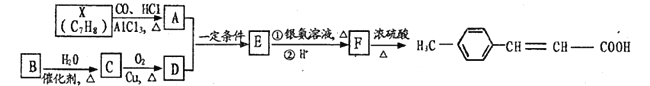
已知:①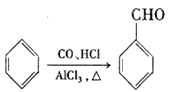 ,A的苯环上一氯代物只有2种。
,A的苯环上一氯代物只有2种。
②有机物B是最简单的单烯烃。
③ (R1、R2为烃基或氢原子)。
(R1、R2为烃基或氢原子)。
回答下列问题:
(1)X的化学名称为________。
(2)写出有机反应类型:F→G________。
(3)碳原子上连有4个不同的原子或原子团时,该碳原子称为手性碳原子。写出F的结构简式,用星号(*)标出F中的手性碳________。
(4)写出C→D的化学方程式_______________________。
(5)写出A的两种能发生银镜反应芳香族同分异构体的结构简式____________。
(6)参照上述合成路线图,设计由苯合成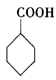 (的路线图(无机试剂任选)。_______________________。
(的路线图(无机试剂任选)。_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PbO2、KMnO4、Cl2、FeCl3、CuCl2的氧化性依次减弱。下列反应不可能发生的是
A. Cu+2Fe3+==Cu2++2Fe2+ B. 10Cl-+2MnO![]() +16H+=2Mn2++5Cl2↑+8H2O
+16H+=2Mn2++5Cl2↑+8H2O
C. Cu+Cl2![]() CuCl2 D. 5Pb2++2MnO
CuCl2 D. 5Pb2++2MnO![]() +2H2O=5PbO2↓+2Mn2++4H+
+2H2O=5PbO2↓+2Mn2++4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液里Ca2+的浓度一般采用mg·cm-3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
(配制KMnO4标准溶液)如图是配制50mL KMnO4标准溶液的过程示意图。
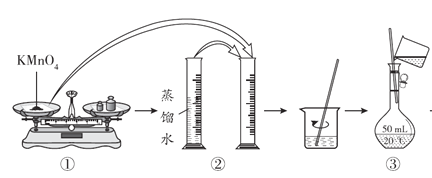
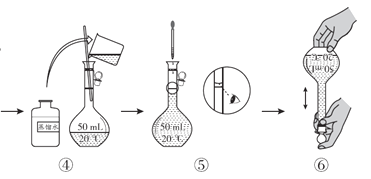
(1)请你观察图示判断,其中不正确的操作有__________(填序号)。
(2)如果用图示的操作配制溶液,所配制的溶液浓度将__________(填“偏大”或“偏小”)。
(测定血液样品中Ca2+的浓度)抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol·L-1 KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。
(3)已知草酸跟KMnO4溶液反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mnx++10CO2↑+8H2O则方程式中的x=__________。
(4)经过计算,血液样品中Ca2+的浓度为__________mg·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂以硝酸为原料生产亚硝酸钠,其工艺流程如图:
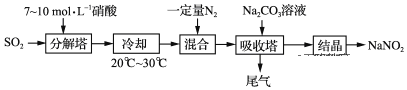
已知:Na2CO3+NO+NO2=2NaNO2+CO2
(1)“分解塔”中SO2从塔底进入,硝酸从塔顶喷淋,其目的是____。
(2)“分解塔”中的温度不宜过高,其原因是____。
(3)按一定计量比在“分解塔”中通SO2和喷入硝酸,若反应后生成的NO与NO2物质的量之比恰好1:1,则“分解塔”中发生反应的化学方程式为____。
(4)为提高氮氧化物的转化率,可向“尾气”中通入一定量的____气体,再通入“吸收塔”中,实现循环吸收。
(5)“吸收塔”所得溶液中除含有NaNO2、NaNO3和少量Na2CO3外,还含有的溶质为___(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某含有SO![]() 、SiO
、SiO![]() 、CO
、CO![]() 、Br-、Na+的溶液中缓慢通入Cl2直至过量,下列对该反应过程的判断不正确的是( )
、Br-、Na+的溶液中缓慢通入Cl2直至过量,下列对该反应过程的判断不正确的是( )
A. 整个过程共发生2个氧化还原反应
B. 所有阴离子的浓度都发生了变化
C. 溶液的颜色发生了变化
D. 反应过程中既有气体产生,也有沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)反式2 -丁烯的结构简式____________________。
(2)与H2加成生成2,5 - 二甲基己烷的炔烃的系统命名____________________。
(3)![]() 的系统命名____________________。
的系统命名____________________。
(4)某烃的分子量为72,跟氯气反应生成的一氯代物只有一种,该烃的结构简式为_______。
(5)写出由丙烯制备聚丙烯的化学反应方程式____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com