
【题目】以下说法正确的是
A.12.0gNaHSO4溶于1L水中,溶液中氢离子的浓度为0.1mol/L
B.25℃时气体的摩尔体积大于22.4L/mol
C.阿伏加德罗常数近似为6.02×1023
D.氦气的摩尔质量是4g/mol
【答案】D
【解析】
A. NaHSO4为强电解质,在溶液中完全电离,电离方程式为:NaHSO4=Na++H++ SO42-,12.0gNaHSO4的物质的量为![]() ,溶于1L水中,所得溶液的体积不是1L,则溶液中氢离子浓度不是0.1mol/L,故A错误;
,溶于1L水中,所得溶液的体积不是1L,则溶液中氢离子浓度不是0.1mol/L,故A错误;
B. 标况即0℃、101 KP时,气体摩尔体积为22.4L/mol,25℃时,因压强不定,所以此时气体的摩尔体积不确定,故B错误;
C. 阿伏伽德罗常数的单位为mol-1,即阿伏伽德罗常数近似为6.02×1023 mol-1,故C错误;
D. 氦原子的相对原子质量为4,而氦气为单原子分子,分子摩尔质量在数值上等于该物质的相对分子质量,故氦气的摩尔质量为4g/mol,故D正确。
答案选D。


科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为![]() ,下列关于该物质的说法中不正确的是
,下列关于该物质的说法中不正确的是
A. 该物质不能发生消去反应,但能在一定条件下发生加聚反应
B. 该物质不能和AgNO3溶液反应产生AgBr沉淀
C. 该物质在NaOH的醇溶液中加热可转化为醇类
D. 该物质可使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的合成氨的方法如图所示,下列说法正确的是
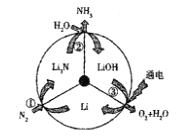
A. 反应①属于“氮的固定”B. 反应②属于氧化还原反应
C. 反应③可通过电解![]() 水溶液实现D. 上述三步循环的总结果为:
水溶液实现D. 上述三步循环的总结果为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:
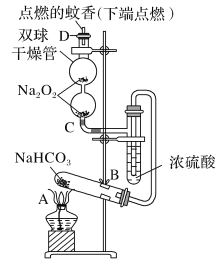
(1)在A试管内发生反应的化学方程式是_____。
(2)B装置的作用是_____。
(3)在双球干燥管内发生反应的化学方程式为____。
(4)双球干燥管内及D处观察到的实验现象是_____。
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内及D处观察到的实验现象是:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象能得出相应结论的是
选项 | 实验操作 | 现象 | 结论 |
A |
| 溶液红色褪去 |
|
B | 向1mL 2mol/L | 先生成白色沉淀,后生成红褐色沉淀 |
|
C | 将 | 溶液变为红色 | 样品已部分或全部变质 |
D | 无水乙醇中加入浓硫酸,加热,产生的气体Y通入酸性 | 溶液紫色褪去 | 气体Y中含有乙烯 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离KNO3和Ba(NO3)2两种固体混合物试回答下列问题
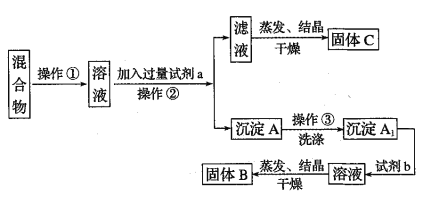
供选试剂:Na2SO4溶液、Na2CO3溶液、K2CO3溶液、K2SO4溶液、硫酸、硝酸
(1)试剂a是_______加入试剂b所发生反应的离子方程式为___________________________
(2)该方案能否达到实验目的:__________________________(填能或不能)若不能,应如何改进?__________________________(若能此问不用回答)
(3)若要测定原混合物中Ba(NO3)2的质量分数,除了要准确称量混合物的质量外至少还要获得的数据是__________的质量
(4)用所制备的KNO3固体配制0.1 mol/L KNO3溶液450mL,回答下列问题:
①配制过程中需要用到的玻璃仪器有烧杯、量筒、胶头滴管、______________
②需要用托盘天平称量_______g KNO3固体)
③下列情况会使所配溶液浓度偏低的是________
A.称量固体时,砝码与药品的位置放反了,即“左码右物”
B.使用有少量蒸馏水的容量瓶
C.定容时俯视刻度线观察液面
D.洗涤和转移时有液体外溅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】机动车排放的污染物主要有碳氢化合物、一氧化碳和氮氧化物等。汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。
(1)已知:![]()
![]()
![]()
![]()
![]()
![]()
则反应![]()
![]() __________。
__________。
(2)科学家研究出了一种高效催化剂,可以将![]() 和
和![]() 发生反应生成
发生反应生成![]() (g)和
(g)和![]() (g)。在T℃下,向某恒容密闭容器中通入a mol/L
(g)。在T℃下,向某恒容密闭容器中通入a mol/L![]() 、b mol/L
、b mol/L![]() ,使其发生上述反应,测得
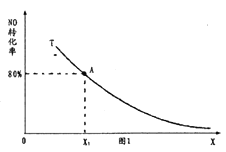
,使其发生上述反应,测得![]() 的平衡转化率与投料比X(表示a、b两者的比值)的关系如图1中曲线所示。若
的平衡转化率与投料比X(表示a、b两者的比值)的关系如图1中曲线所示。若![]() 、
、![]() ,反应开始到达到平衡所用时间是2min,则反应发生2min内
,反应开始到达到平衡所用时间是2min,则反应发生2min内![]() 的平均反应速率v(
的平均反应速率v(![]() )=________,平衡态A点的平衡常数K=________。
)=________,平衡态A点的平衡常数K=________。
(3)柴油燃油车是通过尿素-选择性催化还原(Urea-SCR)法处理氮氧化物。Urea-SCR的工作原理为:尿素[![]() ]水溶液通过喷嘴喷入排气管中,当温度高于160℃时尿素水解产生
]水溶液通过喷嘴喷入排气管中,当温度高于160℃时尿素水解产生![]() ,生成的
,生成的![]() 与尾气混合后,加入适合的催化剂,使氮氧化物得以处理。图2为在不同投料比[
与尾气混合后,加入适合的催化剂,使氮氧化物得以处理。图2为在不同投料比[![]() ]时
]时![]() 转化效率随温度变化的曲线。
转化效率随温度变化的曲线。
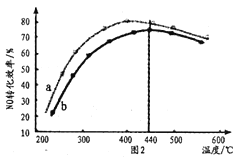
①尿素与![]() 物质的量比a_____b(填“>”、“=”或“<”)。
物质的量比a_____b(填“>”、“=”或“<”)。
②由图可知,下列说法错误的是____
A.400℃以下,随着温度升高,尿素水解释放氨气的速率加快,![]() 转化效率升高
转化效率升高
B.400℃以下,温度升高,反应活化能降低,导致化学反应速率加快
C.440℃以上,温度过高,可能使催化剂活性降低,导致![]() 转化效率下降
转化效率下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1 mol/L的下列五种钠盐溶液的pH如表所示:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
上述几种钠盐的阴离子,结合氢离子能力最强的是______(填离子符号),根据表中数据,将浓度均为0.01mol/L的下列四种溶液分别稀释100倍,pH变化最大的是______.(填字母)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)已知几种离子开始沉淀时溶液的pH如下表所示:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含有相同浓度的Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时,________(填离子符号)先沉淀;Ksp[Fe(OH)2]______(填“>”“=”或“<”)Ksp[Mg(OH)2];要使0.2 mol/L的硫酸铜溶液中铜离子沉淀较为完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液使溶液pH=_______。{Cu(OH)2的Ksp=2×10-20。}
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】36.5gHCl溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为w,物质的量浓度为cmol/L,NA表示阿伏加德罗常数的值,则下列叙述中正确的是( )
A. 所得溶液的物质的量浓度:c=1mol/LB. 所得溶液中含有NA个HCl分子
C. 36.5gHCl气体占有的体积为22.4LD. 所得溶液的质量分数w=![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com