
【题目】36.5gHCl溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为w,物质的量浓度为cmol/L,NA表示阿伏加德罗常数的值,则下列叙述中正确的是( )
A. 所得溶液的物质的量浓度:c=1mol/LB. 所得溶液中含有NA个HCl分子
C. 36.5gHCl气体占有的体积为22.4LD. 所得溶液的质量分数w=![]()
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某学习小组查阅资料可知高温下,FeCl2与O2反应一定生成Fe2O3,可能生成FeC13或Cl2。该小组同学利用如下装置对该反应进行探究。回答下列问题:
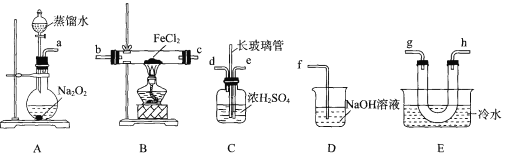
查阅资料:FeCl2固体呈绿色,熔点为674℃,沸点为1023℃;FeC13在100℃左右升华。
(l)装置A中盛放蒸馏水的仪器名称为____。
(2)按气流从左到右的顺序,上述装置合理的连接顺序为____(填仪器接口的小写字母)。
(3)装置C中浓硫酸的作用为 ___,长玻璃管的作用为 ___ 。
(4)实验结束后,用D中所得溶液设计实验证明此反应无Cl2生成 ___。
(5)实验过程中,B处硬质玻璃管中的现象为 ___;装置E中冷水的作用为 ____。
(6)由上述实验可知:高温下,FeCl2与O2反应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从粗铜精炼的阳极泥(主要含有Cu2Te)中提取粗碲的一种工艺流程如图:(已知TeO2微溶于水,易溶于强酸和强碱) 下列有关说法正确的是

A. “氧化浸出”时为使碲元素沉淀充分,应加入过量的硫酸
B. “过滤”用到的玻璃仪器:分液漏斗、烧杯、玻璃棒
C. “还原”时发生的离子方程式为2SO32-+Te4++4OH-=Te↓+2SO42-+2H2O
D. 判断粗碲洗净的方法:取少量最后一次洗涤液,加入BaCl2溶液,没有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室需要0.5mol·L-1硫酸溶液450 mL。根据溶液的配制情况回答下列问题:

(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(2)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是______________。
(3)在配制过程中,其他操作都准确,下列操作中错误的是________(填代号,下同),能引起误差偏高的有________。
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓硫酸
④定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至刻度线
⑦定容时,俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、M的原子序数依次增大,其中X、Y、Z三种元素中,可形成含二种元素的10电子微粒m、n、p、q,且有反应m+n![]() p↑+q;M的最高价氧化物对应的水化物为最强酸。则下列说法不正确是
p↑+q;M的最高价氧化物对应的水化物为最强酸。则下列说法不正确是
A. 简单离子半径X<Z<Y<M
B. 由X、Y、Z三种元素组成的化合物可以是离子化合物
C. X、Y、Z三种元素组成的化合物的水溶液一定呈酸性
D. MZ2可用于自来水的杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A. 化学反应必然伴随发生能量变化
B. 化学变化中的能量变化主要是由化学键变化引起的
C. 能量变化是化学反应的基本特征之一
D. 化学反应中能量变化的大小与反应物的质量多少无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作①的名称是________,操作②的名称是____________。
(2)试剂a是____________(填化学式,下同),试剂b是__________,固体B是____________。
(3)加入试剂a所发生反应的化学方程式为__________________________________。
加入试剂b所发生反应的化学方程式为____________________________________。
(4)该方案能否达到实验目的:__________________________(填“能”或“不能”)。若不能,应如何改进?(若能,此问不用回答)__________。
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是____的质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子中的中心原子杂化轨道的类型相同的是( )
A. CO2与SO2 B. CH4与NH3 C. BeCl2与BF3 D. C2H2与C2H4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com