
下列说法中正确的是 ( )
| A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大 |
B.AgCl悬浊液中存在平衡:AgCl(s) Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 |
| C.AgCl悬浊液中加入KI溶液,白色沉淀变成黄色,证明此条件下Ksp(AgCl)>Ksp(AgI) |
| D.硬水中含有较多的 Ca2+、Mg2+、HCO3—、SO42—,加热煮沸可以完全除去其中的Ca2+、Mg2+ |
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:单选题
关于室温下下列溶液的说法不正确的是
| A.水的电离程度:①=②=③=④ |
| B.分别加水稀释10倍,溶液的pH:①>②>③>④ |
C.①、③两溶液等体积混合: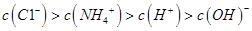 |
D.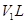 溶液②与 溶液②与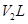 溶液③混合,若 溶液③混合,若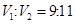 ,则混合溶液pH=4(忽略溶液体积变化) ,则混合溶液pH=4(忽略溶液体积变化) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是( )
| A.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7 |
| B.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| C.常温下,向NH4Cl溶液中加入氨水至溶液的pH=7,此时溶液中c(NH4+)>c(C1-) |
| D.0.1mol·L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
H2SO3是二元弱酸,NaHSO3溶液呈酸性。在0.1 mol·L-1 NaHSO3溶液中,下列关系正确的是( )
| A.c(HSO3-)>c(SO32-)>c(H2SO3) |
| B.c(Na+)=c(HSO3-)+2c(SO32-)+c(H2SO3) |
| C.c(Na+)=c(HSO3-)>c(H+)>c(OH-) |
| D.c(Na+)+c(H+)=c(HSO3-)+c(OH-)+c(SO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是 ( )
| A.一般认为沉淀离子浓度小于10-4 mol/L时,则认为已经沉淀完全 |
| B.反应AgCl+NaBr=AgBr+NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水 |
C.Al(OH)3(s) Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3 Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3 Al3++3OH-表示水解平衡 Al3++3OH-表示水解平衡 |
| D.只有反应速率很高的化学反应才能应用于工业生产 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度。下列有关叙述正确的是 ( )
A.HY-水解方程式为:HY-+ H2O H3O++ Y2- H3O++ Y2- |
| B.在该盐的溶液中离子浓度大小关系为:c(Na+) >c(Y2-) >c(HY-) >c(OH-) >c(H+) |
C.H2Y的电离方程式为:H2Y+H2O HY-+H3O+ HY-+H3O+ |
| D.在该盐的溶液中:c(Na+) >c(HY-) >c(Y2-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知相同条件下,HClO的电离常数小于H2CO3的一级电离常数(Ka)。为了提高氯水中HClO的浓度,可加入( )
| A.NaCl(s) | B.CaCO3(s) | C.H2O | D.NaOH(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于常温下pH均为4的三种溶液:①盐酸,②CH3COOH溶液,③NH4Cl溶液,下列说法中正确的是( )
| A.溶液中由水电离出的c(H+):②>③ |
| B.稀释100倍后溶液的pH:①<③ |
| C.中和相同体积的上述溶液消耗NaOH溶液的体积:①<② |
| D.②和③等体积混合后的溶液:c(CH3COO-)+c(Cl-)=c(NH) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在t°C时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如下图所示。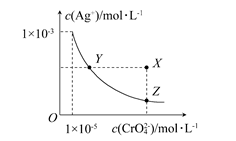
又知AgCl的Ksp=1.8×10-10。
下列说法不正确的是 ( )
| A.t°C时,Ag2CrO4的Ksp为1×10-8 |
| B.在饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点 |
| C.t°C时,Y点和Z点的Ag2CrO4的Ksp相等 |
| D.t°C时,将0.01 mol·L-1 AgNO3溶液滴入20 mL 0.01 mol·L-1 KCl和0.01 mol·L-1 K2CrO4的混合溶液中,Cl-先沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com