
关于室温下下列溶液的说法不正确的是
| A.水的电离程度:①=②=③=④ |
| B.分别加水稀释10倍,溶液的pH:①>②>③>④ |
C.①、③两溶液等体积混合: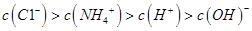 |
D.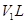 溶液②与 溶液②与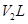 溶液③混合,若 溶液③混合,若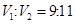 ,则混合溶液pH=4(忽略溶液体积变化) ,则混合溶液pH=4(忽略溶液体积变化) |
C
解析试题分析:A、氨水、NaOH溶液的pH为11,则OH?浓度为10-3mol?L?1,pH=3的盐酸和醋酸溶液中H+浓度为10-3mol?L?1,对水的电离影响相同,正确;B、加水稀释,弱电解质的电离平衡向右移动,所以溶液的pH:①>②>③>④,正确;C、①、③两溶液等体积混合,氨水大量过量,溶液溶质为NH3?H2O和NH4Cl,溶液显碱性,离子浓度大小顺序为:c(NH4+) > c(Cl?)>c(OH?)>c(H+),错误;D、HCl过量,混合溶液c(H+)=(V2?10-3mol—V1?10-3mol)/( V1+ V2)= 10-4mol?L?1,所以pH=4,正确。
考点:本题考查酸碱中和反应、离子浓度比较、水的电离、pH的计算。


 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:单选题
给试管中某红色溶液加热,溶液颜色逐渐变浅,则原溶液可能是
①滴有石蕊的NH4Cl溶液 ②滴有酚酞的氨水溶液 ③滴有石蕊的H2SO4溶液 ④滴有酚酞的饱和氢氧化钙溶液 ⑤滴有酚酞的Na2CO3溶液 ⑥溶有SO2的品红溶液
| A.②④ | B.①③⑤ | C.①④⑥ | D.②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
| A.难溶电解质作比较时,Ksp小的,溶解度一定小 |
| B.Ksp大小取决于难溶电解质的量,所以离子浓度改变时,沉淀溶解平衡会发生移动 |
| C.所谓沉淀完全就是用沉淀剂将溶液中某一离子完全除去 |
| D.温度一定,当溶液中Ag+和Cl-浓度的乘积等于Ksp时,溶液为AgCl的饱和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
室温下,某溶液中由水电离产生的c(H+)等于10-13 mol·L-1,该溶液的溶质不可能是( )
| A.NaHSO4 | B.NaCl | C.HCl | D.Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
 2H++S
2H++S查看答案和解析>>
科目:高中化学 来源: 题型:单选题
标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图中曲线所示。下列分析正确的是( )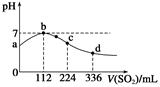
| A.原H2S溶液的物质的量浓度为0.05 mol·L-1 |
| B.氢硫酸的酸性比亚硫酸的酸性强 |
| C.b点水的电离程度比c点水的电离程度大 |
| D.a点对应溶液的导电性比d点强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中正确的是 ( )
| A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大 |
B.AgCl悬浊液中存在平衡:AgCl(s) Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 |
| C.AgCl悬浊液中加入KI溶液,白色沉淀变成黄色,证明此条件下Ksp(AgCl)>Ksp(AgI) |
| D.硬水中含有较多的 Ca2+、Mg2+、HCO3—、SO42—,加热煮沸可以完全除去其中的Ca2+、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关电解质溶液的说法正确的是 ( )。
| A.在蒸馏水中滴加浓H2SO4,KW不变 |
| B.CaCO3难溶于稀硫酸,也难溶于醋酸 |
| C.在Na2S稀溶液中,c(H+)=c(OH-)-2c(H2S)-c(HS-) |
| D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com