
标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图中曲线所示。下列分析正确的是( )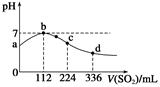
| A.原H2S溶液的物质的量浓度为0.05 mol·L-1 |
| B.氢硫酸的酸性比亚硫酸的酸性强 |
| C.b点水的电离程度比c点水的电离程度大 |
| D.a点对应溶液的导电性比d点强 |
科目:高中化学 来源: 题型:单选题
关于室温下下列溶液的说法不正确的是
| A.水的电离程度:①=②=③=④ |
| B.分别加水稀释10倍,溶液的pH:①>②>③>④ |
C.①、③两溶液等体积混合: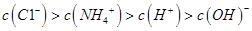 |
D.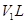 溶液②与 溶液②与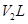 溶液③混合,若 溶液③混合,若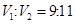 ,则混合溶液pH=4(忽略溶液体积变化) ,则混合溶液pH=4(忽略溶液体积变化) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将氯化铝溶液蒸干并灼烧后得到纯净的固体A,将A在高温下熔融后用铂电极进行电解,下列有关电极产物的判断正确的是
| A.阴极产物是氢气 | B.阳极产物是氧气 |
| C.阴极产物是铝和氧气 | D.阳极产物只有氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
现有常温下的五种溶液(如下表)。
| | ① | ② | ③ | ④ | ⑤ |
| 溶液 | 氨水 | 氢氧化钠 | 醋酸 | 盐酸 | 醋酸钠 |
| pH | 11 | 11 | 3 | 3 | 8.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,柠檬酸水溶液的pH是3,食用醋的pH是2,可乐的pH是6,三种物质的溶液中c(OH-)分别是( )
| A.1×10-11 mol·L-1,1×10-12 mol·L-1,1×10-8 mol·L-1 |
| B.1×10-11 mol·L-1,1×10-8 mol·L-1,1×10-12 mol·L-1 |
| C.2×10-11 mol·L-1,1×10-10 mol·L-1,1×10-8 mol·L-1 |
| D.1×10-8 mol·L-1,1×10-11 mol·L-1,1×10-12 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
测得醋酸甲的pH:a,醋酸乙的pH:a+1。下列推断中正确的是( )
| A.醋酸甲中H+的物质的量是醋酸乙中的10倍 |
| B.醋酸乙的电离程度比醋酸甲大 |
| C.中和等物质的量的NaOH溶液需甲、乙两酸的体积之比为10∶1 |
| D.甲、乙溶液加水稀释,当pH相等时甲需加更多的水 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于电离常数的说法正确的是( )
| A.电离常数随着弱电解质的浓度增大而增大 |
| B.CH3COOH的电离常数表达式为Ka= |
| C.CH3COOH溶液中加入少量CH3COONa溶液,电离常数减小 |
| D.电离常数只与温度有关,与浓度无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在0.1 mol·L-1的NH4HSO4溶液中,下列微粒的物质的量浓度关系不正确的是 ( )
| A.c(H+)>c(SO42-)>c(NH4+) |
| B.c(NH4+)+c(H+)=2c(SO42-)+c(OH-) |
| C.c(H+)=c(NH4+)+c(NH3·H2O)+c(OH-) |
| D.室温下滴加NaOH溶液至中性后:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是 ( )
| A.一般认为沉淀离子浓度小于10-4 mol/L时,则认为已经沉淀完全 |
| B.反应AgCl+NaBr=AgBr+NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水 |
C.Al(OH)3(s) Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3 Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3 Al3++3OH-表示水解平衡 Al3++3OH-表示水解平衡 |
| D.只有反应速率很高的化学反应才能应用于工业生产 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com