
【题目】将11.5 g钠投入到89 g水中(足量),充分反应后所得溶液的密度为1.25 g·cm-3。
计算:(1)生成H2的体积(标准状况下) _______ 。
(2)所得溶液中溶质的物质的量浓度为多少________ ?
【答案】5.6 L 6.25 mol·L-1
【解析】
根据n=m÷M计算11.5g Na的物质的量,根据2Na+2H2O=2NaOH+H2↑,计算生成氢气、NaOH的物质的量,根据V=nVm计算氢气的体积;根据m=nM计算氢气的质量,溶液质量=m(Na)+m(水)-m(氢气),再根据V=m÷ρ计算溶液的体积,根据c=n÷V计算所得溶液物质的量浓度.
11.5g Na的物质的量:n(Na)=11.5g÷23g·mol-1=0.5mol,

n(NaOH)=![]() =0.5mol
=0.5mol
n(H2)=![]() =0.25mol
=0.25mol
(1)标况下生成氢气的体积:V(H2)=0.25mol×22.4L·mol-1=5.6L;
(2)生成氢气的质量m((H2)=0.25mol×2g·mol-1=0.5g,
溶液质量=11.5g+89g-0.5g=100g,
溶液的体积=![]() =80mL,
=80mL,
溶液的物质的量浓度=![]() =6.25mol·L-1。
=6.25mol·L-1。


 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】合成氨和制硫酸是中学阶段重要的化工生产反应。
(1)硫酸工业生产中接触室内发生的反应方程式为___;在实际生产过程中,操作温度选定400-500摄氏度,压强采用常压的原因分别是___。
(2)合成氨反应生成的氨气可用于工业制纯碱,写出以氨气、氯化钠、二氧化碳、水为原料制备纯碱的化学方程式___、___。
(3)合成氨每生成1g液氨,放出QkJ的热量,写出热化学反应方程式___。
(4)常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),还生成一种无色无味的单质气体,写出此反应的化学方程式并标出电子转移的方向和数目____,该反应中被还原的是___,还原产物是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.碳酸氢钠溶液与少量石灰水反应HCO3﹣+Ca2++OH﹣=CaCO3↓+H2O
B.氯化铵与氢氧化钠两种浓溶液混合加热OH﹣+NH4+![]() H2O+NH3↑
H2O+NH3↑
C.氢氧化铁与稀硫酸反应H++OH﹣=H2O
D.单质铜与稀硝酸反应Cu+2H++2NO3﹣=Cu2++2NO↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种从电镍含钴废渣(主要成分有Co(OH)3、Ni(OH)3、Fe(OH)3及少量Ca(OH)2、Mg(OH)2等杂质)中提取氧化钴(Co2O3)的工艺流程如下:
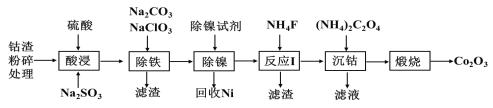
已知:Ksp(CaF2)=3.45×10-11,Ksp(MgF2)=7.42×10-11,Ksp[Co(OH)3]=2×10-44。
(1)在还原剂Na2SO3存在的条件下,钴渣易溶于酸中,请写出酸浸时Co(OH)3与Na2SO3反应的离子方程式______,该步操作中硫酸不宜过量太多的主要原因是 ____。
(2)除铁操作中Fe3+以黄钠铁矾Na2Fe6(SO4)4(OH)12形式从溶液中沉淀析出。中学检验Fe3+的溶液中混有Fe2+的常用试剂是________。
(3)反应Ⅰ中加入NH4F的目的______。
(4)沉钴操作发生的反应为(NH4)2C2O4+CoCl2![]() CoC2O4↓+2NH4Cl,也可用Na2C2O4代替(NH4)2C2O4,若要得到较为纯净的CoC2O4,则合理的加料方式是______(填字母)。
CoC2O4↓+2NH4Cl,也可用Na2C2O4代替(NH4)2C2O4,若要得到较为纯净的CoC2O4,则合理的加料方式是______(填字母)。
a.将Na2C2O4溶液与反应Ⅰ滤液同时加入到反应容器中
b.将Na2C2O4溶液缓慢加入到盛有反应Ⅰ滤液的反应容器中
c.将反应Ⅰ滤液缓慢加入到盛有Na2C2O4溶液的反应容器中
(5)450℃在空气中煅烧发生的化学反应方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用Na2O2与H2O反应快速制取少量O2.用下面装置制取O2并演示Na在O2中的燃烧实验.
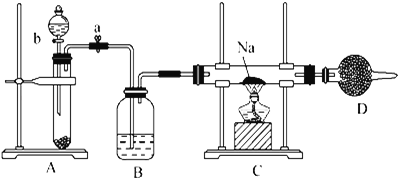
请回答下列问题:
(1)写出A装置中反应的化学方程式_____.
(2)B装置中盛放的试剂是_____.
(3)D装置中盛放的试剂是_____,其作用是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4NH3(g)+5O2(g)== 4NO(g)+6H2O(g),该反应在5L的密闭容器中进行,半分钟后,NO物质的量增加了0.3mol,则此反应的平均速率为 ( )
A. V(O2)=0.01molL-1s-1B. V(NO)=0.008 molL-1s-1
C. V(H2O)=0.003 molL-1s-1D. V(NH3) =0.003 molL-1s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.6molX气体和0.4molY气体混合于容积为2L的容器中,使其发生如下反应:3X(g)+Y(g)![]() nZ(g)+2W(g)。5min末生成0.2molW,若测知以Z浓度变化表示的平均反应速率为0.01mol/( L· min),则n的值为
nZ(g)+2W(g)。5min末生成0.2molW,若测知以Z浓度变化表示的平均反应速率为0.01mol/( L· min),则n的值为
A. 1B. 2C. 3D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置进行有关Cl2的实验。下列说法不正确的是( )
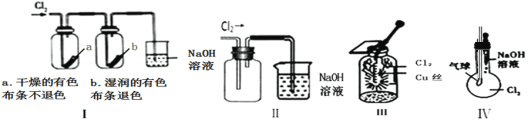
A.图I中:实验现象证明氯气无漂白作用,氯水有漂白作用
B.图II中:收集氯气
C.图IV中:若气球干瘪,证明可与NaOH溶液反应
D.图III中:生成棕黄色的烟,加少量水溶解得到蓝绿色溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500mL含有BaCl2和KCl的混合溶液分成2等份,取一份加入含a mol 硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol 硝酸银的溶液,恰好使氯离子完全沉淀。则该溶液中钾离子浓度为:
A.0.1(b-2a)mol/LB.10(b-2a)mol/L
C.10(2a-b)mol/LD.4(b-2a)mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com