

 �����������ڼ����������ܷ���ˮ�ⷴӦ��
�����������ڼ����������ܷ���ˮ�ⷴӦ�� ��
�� ��
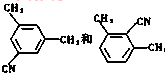
�� �����������ڼ����������ܷ���ˮ�ⷴӦ����Ӧ����ʽΪ
�����������ڼ����������ܷ���ˮ�ⷴӦ����Ӧ����ʽΪ ��
�� ��
�� ��
�� ��
��


 Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ı�ȼ����Ϊ-890.3kJ?mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=-890.3 kJ?mol-1 | ||||
B��500�桢30 MPa�£���0.5 mol N2��1.5 mol H2�����ܱ������г�ַ�Ӧ����NH3��g��������19.3 kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��
| ||||
| C���Ȼ�þ��Һ�백ˮ��Ӧ��Mg2++2OH-�TMg��OH��2�� | ||||
| D������������NaOH��Һ��Al2O3+2OH-+3H2O�T2Al��OH��4- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶� | ʱ��/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n��CH4�� | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n��CH4�� | 0.50 | 0.30 | 0.18 | �� | 0.15 |
| A��10 min�ڣ�T1ʱCH4�Ļ�ѧ��Ӧ���ʱ�T2ʱС |
| B���¶ȣ�T1��T2 |
| C��a��0 |
| D��ƽ�ⳣ����K��T1����K��T2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ����� | ̽���Ͼ������ȷֽ����Ҫ����Ϊ�������Ļ���� |
| �������� | ��CuO�ܽ���������CO2��H2O �ڼױ��ɱ�����KMnO4��Һ����Ϊ���ᣬ�����������ڱ� |
| ʵ����� |  |
| ʵ���¼ | ����ͼ����װ�ã���������ǿ��װ��A�е��Թܣ�����װ���ڿ�����Ӱ�죩һ��ʱ��ɹ۲쵽�������� ��Bװ���Թ�����Һ̬�������� ��C����ˮ����ɫ��dz ��E�к�ɫ����ͭ��� ��F����ˮ����ͭ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��x=2 |
| B��ƽ��ʱM��c��A��=0.6mol/L |
| C��y��0.8 |
| D��M��B��ת������N��C��ת����֮��Ϊ1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��������Ϊ146��������Ϊ92 ���ˣ�U��ԭ��
| ||
| B��CO2�ĵ���ʽ��O����C����O | ||
C���Ҵ����ӵı���ģ�ͣ� | ||
| D����������ˮ�ĵ��뷽��ʽ��CH3COOH?H++CH2COOH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����һ���������ϣ��㷺Ӧ�������ϡ�ҽҩ��Ⱦ�ϼ�ũҩ����ҵ����ͼ�ǹ�ҵ���Ա�Ϊ��Ҫԭ�ϣ���������ȩ��һ�ֺϳ�·�ߣ����ַ�Ӧ����������������ȥ����
����һ���������ϣ��㷺Ӧ�������ϡ�ҽҩ��Ⱦ�ϼ�ũҩ����ҵ����ͼ�ǹ�ҵ���Ա�Ϊ��Ҫԭ�ϣ���������ȩ��һ�ֺϳ�·�ߣ����ַ�Ӧ����������������ȥ����
 ���˴Ź�����������
���˴Ź����������� ��д����1-����Ϊԭ���Ʊ�������������ĺϳ�·������ͼ�����Լ����ã���
��д����1-����Ϊԭ���Ʊ�������������ĺϳ�·������ͼ�����Լ����ã���| 500�� |
| Ũ���� |
| 170�� |
| Br2 |

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com