
| A、x=2 |
| B、平衡时M中c(A)=0.6mol/L |
| C、y<0.8 |
| D、M中B的转化率与N中C的转化率之和为1 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3mol |
| 2L |
| 2 |
| 3 |
| 3mol |
| 2L |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
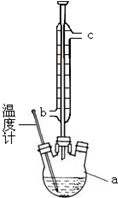 阿司匹林(乙酰水杨酸)已应用百年,成为医药史上三大经典药物之一,至今它仍是世界上应用最广泛的解热、镇痛和抗炎药,也是作为比较和评价其他药物的标准制剂.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成该物质,设计的合成路线为:
阿司匹林(乙酰水杨酸)已应用百年,成为医药史上三大经典药物之一,至今它仍是世界上应用最广泛的解热、镇痛和抗炎药,也是作为比较和评价其他药物的标准制剂.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成该物质,设计的合成路线为:| 浓硫酸摇匀 |
| 85~90℃ |
| 10min |
| 冷却 |
| 15min |
| 抽滤 |
| 洗涤 |
| 加入A |
| 充分搅拌 |
| 抽滤 |
| 盐酸 |
| 冷却 |
| 抽滤 |
| 洗涤 |
| 乙酸乙酯 |
| 沸石 |
| 加热 |
| 回流 |
| 趁热过滤 |
| 冷却 |
| 抽滤 |
| 洗涤 |
| 干燥 |
| 名称 | 相对分子质量 | 熔点或沸点(0C) | 水 | 醇 | 醚 |
| 水杨酸 | 138 | 158(熔点) | 微溶 | 易溶 | 易溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 反应 | 可溶 | 易溶 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 | 可溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Ba2+、Cl-、NO3- |
| B、Na+、Fe3+、I-、NO3- |
| C、NH4+、Al3+、Br-、SO42- |
| D、K+、Na+、HCO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com