
【题目】元素的性质随着原子序数的递增呈现周期性的变化的根本原因是( )
A. 元素相对原子质量的递增,量变引起质变
B. 元素的金属性和非金属性呈周期性变化
C. 元素化合价呈周期性变化
D. 元素原子核外电子排布呈周期性变化
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.焰色反应为黄色,说明该物质中肯定含有钠元素
B.某物质的焰色反应不显紫色(未透过蓝色钴玻璃),说明该物质中肯定没有钾元素
C.焰色反应不能用于物质的鉴别
D.焰色反应是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,溶液中由水电离出氢离子的浓度为1×10-12mol·L-1,下列说法正确的是( )
A.该溶液pH=12B.该溶液pH=2
C.该溶液pH=12或2D.不能确定溶液pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)如图中的A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色。请填空:

(1)电源A的a为____极。
(2)滤纸B上发生的总反应方程式为___________________。
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为_____________,电极f上发生的反应为____,槽中盛放的电镀液可以是____(只要求填一种电解质溶液)。
(Ⅱ)电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。
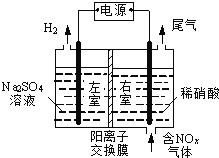
若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式_____________________。
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂(Li)是世界上最轻的金属,它属于碱金属的一种。下列说法正确的是( )
A. 碱金属单质在氧气中燃烧,都生成过氧化物 B. Li是碱金属原子中半径最小的原子
C. Li、Na、K、Rb+ 的最外层都只有一个电子 D. Na+ 比Li多一个电子层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g)![]() 2C(g)+ D(g),经2minB的浓度减少0.6mol/L。对此反应速率的表示正确的是
2C(g)+ D(g),经2minB的浓度减少0.6mol/L。对此反应速率的表示正确的是
A. 用A表示的反应速率是0.4 mol/(L·min)
B. 分别用B、C、D表示的反应速率其比值是3:2:1
C. 在2min末的反应速率,用B表示是0.3mol/(L·min)
D. 在这2min内用B和C表示的反应速率的值都是逐渐减小的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色稀溶液X中,可能含有下表所列离子中的某几种。
阴离子 | CO |
阳离子 | Al3+、Fe3+、Mg2+、NH、Na+ |
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。
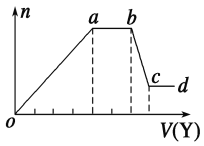
(1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是___,ab段发生反应的离子是______________,bc段发生反应的离子方程式为______________。
(2)若Y是NaOH溶液,则X中一定含有的离子是___________________。ab段反应的离子方程式为_______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com