
��֪�Ȼ�ѧ����ʽ(Q1��Q2��Ϊ��ֵ)��
C(s)��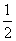 O2(g) = CO(g) ��H����Q1 kJ��mol��1��
O2(g) = CO(g) ��H����Q1 kJ��mol��1��
C(s)��O2(g) = CO2(g) ��H����Q2 kJ��mol��1��
�й�������Ӧ�������������
A��Q1<Q2 B�������������������ڷ�Ӧ��������
C����1 mol C��Ӧ����1 mol CO����ʱ�ų�Q1 kJ������
D��1 mol CO2������е���������1 mol�ɱ����е�����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���š�pM2.5�����������������������Ұ����������Խ��Խ�������ǵ����ӣ�����������֮�����˼������κͻ����ദ����Ӧ����ʶ��Ӧ��ѧһЩʵ�á��õ��ķ�����Ϊ����������Ŀǰ�ҹ��Ļ����������������Ϊȼú���飬����ȼúΪ���ĵ�����������ɵĻ�����Ⱦ����Լ������ҵ��չ��һ����Ҫ���أ����з۳����������NOx��������������ú��վ�����������ص㡣
��1������SO2����Ⱦ�����Ϊ�����ҹ�����̽����һ����������CO��ԭSO2�õ�������ķ�������ȥSO2����д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��2��ȼú��������ķ����ܶ࣬��ʯ��ʯ��ʯ�෨����ˮ���ȡ�����ʯ��ʯ-ʯ�෨�����ԭ����һ����SO2+Ca(OH)2=CaSO3+H2O��Ȼ���ٽ����������Ƴ�ʯ��,д���÷�Ӧ�Ļ�ѧ����ʽ ��
��3��ȼú���������ɲ��ð���NH3����Ϊ��ԭ���ʣ��ڴ������ڵ������£���������(NOx)�뻹ԭ��������Ӧ���������ʣ�д�����������백��Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
25�桢101kPa �£���2Na(s)��1/2O2(g)=Na2O(s) ��H1=��414KJ/mol
��2Na(s)��O2(g)=Na2O2(s) ��H2=��511KJ/mol
����˵����ȷ����
A���ٺ͢ڲ�����������Ӹ����Ȳ����
B���ٺ͢����ɵ����ʵ����IJ��ת�Ƶ�������ͬ
C��������Na������O2��Ӧ����Na2O�����¶���������Na2O�������ӿ�
D��25�桢101kPa �£�Na2O2��s��+2 Na��s��= 2Na2O��s�� ��H=��317kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ϊ�ᴿ�������ʣ�����������Ϊ���ʣ�����ѡ�õ��Լ��ͷ��뷽����ȷ���ǣ�������
| ���� | �����Լ� | ���뷽�� | |
| A | ����ͭ��Һ���������� | ͭ�� | �ᾧ |
| B | NaCl��Һ��CuCl2�� | NaOH��Һ | ��ȡ |
| C | �Ҵ���ˮ�� | ________ | ��Һ |
| D | ͭ�ۣ����ۣ� | ϡ���� | ���� |
| �� | A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪XΪFeO��CuO�Ļ���ȡ���ݵ�������X��Ʒ�����ˢ١��ڡ��۲�ʵ�飬��ϵ��ͼ�����й���D������ϡ���ᣩ��
��1��д������D�Ļ�ѧʽ��������
��2�������ù���D������Ϊ32g����ҺE��ֻ��һ�ֽ������ӣ�����F�ڱ�״�������Ϊ5.6L���Լ���X��FeO��CuO�������ȣ�д��������̣���������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪2SO2(g) + O2(g) 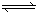 2SO3(g) (����Ӧ����)������500��ʹ����������£��÷�Ӧ���ݻ��̶����ܱ������н��У������й�˵������ȷ����
2SO3(g) (����Ӧ����)������500��ʹ����������£��÷�Ӧ���ݻ��̶����ܱ������н��У������й�˵������ȷ����
A���������¶ȣ����Լ�����Ӧ����
B��������Ȼ�ܼӿ컯ѧ��Ӧ���ʣ����������SO2��ת����
C����������ʱ��SO2������ȫת��ΪSO3
D���ﵽƽ��ʱ��SO2��SO3��Ũ��һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������10 mL c(H+)=10-3 mol��L��1�Ĵ�����Һ�м�ˮϡ�ͺ�����˵����ȷ����
A����Һ�е������ӵ���Ŀ����
B����Һ��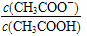 ��С
��С
C������ĵ���̶�����c(OH-)������
D���ټ���10 mL c(OH-)=10-3 mol��L��1��NaOH��Һ��������NaOHǡ����ȫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и�ԭ�������У�����ӦԪ��ԭ�����γ�XY2 ���ۻ��������
A��3��8 B��1��16 C��12��17 D��6��8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ʵ�顱���м��ס����㡢��Լ����ɫ���ŵ㣬�۲������ĸ������ʵ�顱���г�װ��δ���������ж�����˵����ȷ����
A.����ʱ�����ϲ��㼯�˹���NH4Cl��˵��NH4Cl�����ȶ��ԱȽϺ�
B.����ʱ���ڡ�����Һ����죬��ȴ���ֶ���Ϊ��ɫ
C.���У���������ˮ�е�������������ɫ��������ڱ�ˮ�е�������������ɫ��dz
D.�ĸ������ʵ�顱���������Ļ�ѧ��Ӧ���ǿ��淴Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com