
2012年8月24日,武汉市一家有色金属制造厂发生氨气泄露事故。已知在一定温度下,合成氨工业原料气H2制备涉及下面的两个反应:
C(s)+H2O(g) CO(g)+H2(g);
CO(g)+H2(g);
CO(g)+H2O(g) H2(g)+CO2(g)。
H2(g)+CO2(g)。
(1)判断反应CO(g)+H2O(g) CO2(g)+H2(g)达到化学平衡状态的依据是________。(多选、漏选、错选均不得分)
CO2(g)+H2(g)达到化学平衡状态的依据是________。(多选、漏选、错选均不得分)
A.容器内压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(2)在2 L定容密闭容器中通入1 mol N2(g)和3 mol H2(g),发生反应:3H2(g)+N2(g)  2NH3(g),ΔH<0,测得压强-时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
2NH3(g),ΔH<0,测得压强-时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
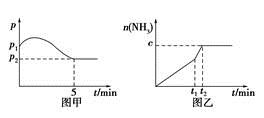
①若图中c=1.6 mol,则改变的条件是________(填字母);
②若图中c<1.6 mol,则改变的条件是__________(填字母);此时该反应的平衡常数____________。(填字母)(填“增大”、“减小”、“不变”)
A.升温 B.降温 C.加压 D.减压 E.加催化剂
(3)如(2)题中图甲,平衡时氢气的转化率为________。
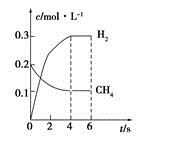
(4)工业上可利用如下反应:H2O (g)+CH4 (g) 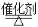 CO(g)+3H2(g)制备CO和H2。在一定条件下1 L的密闭容器中充入0.3 mol H2O和0.2 mol CH4,测得H2(g)和CH4(g)的物质的量浓度随时间变化曲线如右图所示:0~4 s内,用CO(g)表示的反应速率为____________。
CO(g)+3H2(g)制备CO和H2。在一定条件下1 L的密闭容器中充入0.3 mol H2O和0.2 mol CH4,测得H2(g)和CH4(g)的物质的量浓度随时间变化曲线如右图所示:0~4 s内,用CO(g)表示的反应速率为____________。
(1)BC (2) ①E ②A 减小
(3)80% (4)0.025 mol/(L·s)
【解析】(1)该反应前后气体物质的量不变,故压强不能用来判断是否达到平衡状态的标志,选项B、C由平衡状态特征及本质可知可作为判断反应达到化学平衡状态的依据;选项D与平衡状态无直接关系;
(2) 3H2(g) +N2(g) 2NH3(g),
2NH3(g),
投料 3 mol 1 mol 0
转化量 3x x 2x
平衡量 3-3x 1-x 2x
反应前后的压强比等于物质的量比即(4-2x)∶4=0.6,x=0.8, c=1.6 mol,平衡没移动,但速率加快,所以改变的条件是使用催化剂;c<1.6 mol,逆向移动,且速率加快,只能升高温度。
(3)由(2)可以求出氢气的转化率为80%。
(4)0~4 s内,v(CO)=v(CH4)=0.025 mol/(L·s)。


科目:高中化学 来源:2014高考名师推荐化学Vm与它的推论应用(解析版) 题型:选择题
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是:
A.甲的分子数比乙的分子数多
B.甲的物质的量比乙的物质的量少
C.甲的摩尔体积比乙的摩尔体积小
D.甲的相对分子质量比乙的相对分子质量小
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学CB计算法(解析版) 题型:选择题
下列溶液中NO3?-的浓度与500 mL 0.4 mol·L-1 KNO3溶液中NO3-的浓度相等的是
A.50 mL 4 mol·L-1的KNO3溶液
B.1 L 0.2 mol·L-1的KNO3溶液
C.100 mL 0.2 mol·L-1的Ba(NO3)2溶液
D.500 mL 0.4 mol·L-1的Ba(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测8 题型:选择题
已知某物质X能发生如下转化:
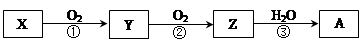
下列有关上述转化关系中物质及其反应的叙述错误的是
A若X??N2或NH3(催化氧化),则A为硝酸
B若X为S 或H2S(完全燃烧),则A为硫酸
C若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y
D反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测8 题型:选择题
下列各组离子在指定溶液中一定能大量共存的是
A.含有Fe3+的溶液中:Na+、AlO2一、C6H5-、I-
B.含有大量NO3-的溶液中:H+、Na+、Fe3+、Cl-
C.加入Al能放出H2的溶液中:Cl-、NO3-、SO42-、K+
D.由水电离出的c(OH—)=l×10—13mol?L—1的溶液中:Na+、Ba2+、Cl-、NH4+
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测7 题型:简答题
【物质结构与性质】
过渡元素具有较多的空轨道,所以第四周期的Cr、Fe、Co、Ni、Cu、Zn等多种金属能形成配合物。
(1)基态Cu原子的核外电子排布式为 ;
(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:
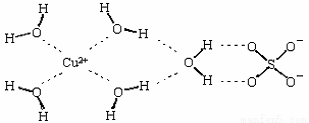
图中虚线表示的作用力为 ;
(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4·H2O晶体。在Cu(NH3)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团是 ,其中心原子的杂化轨道类型是 ;
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型。试推测四羰基镍的晶体类型是 , Ni(CO)4 易溶于下列 。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(5)元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子最外层电子数是其内层的3倍。X与Y所形成化合物晶体的晶胞如图所示,该化合物的化学式为 。
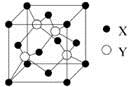
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测7 题型:选择题
下列说法或表述正确的是
A由水电离产生的c(H+)=1×10-2mol?L-1溶液中,可能存在:CO32-、NH4+、Cl- 、Na+
B某醋酸稀溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b
C Ba(OH)2溶液中加人过量的Al2(SO4)3溶液,其离子方程式为:3Ba2++6OH- +2Al3+ +3SO42-=3BaSO4↓+2Al(OH)3↓
D物质的量浓度均为1 mol?L-1的NaCl和MgCl2混合液中,含有Cl-的数目为3NA (NA表示阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测6 题型:选择题
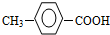 有多种同分异构体,其中符合属于酯类并含含苯环的同分异构体有多少种(不考虑立异构)
有多种同分异构体,其中符合属于酯类并含含苯环的同分异构体有多少种(不考虑立异构)
A.6 B.5 C.4 D.3
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测4 题型:选择题
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子 层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是
层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是
A.Y元素最高价氧化物对应的水化物化学式H2YO4
B.原子半径由大到小的顺序为:Z>Y> W
C.X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定
D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1︰2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com